ADSORPTION
Article modifié le
Adsorption sur les liquides
La surface d'un liquide est, par nature, homogène ; mais sa forme ou son étendue sont facilement modifiées sous l'action de contraintes. La résistance qu'elle oppose est une mesure de la tension superficielle du liquide. La présence d'un film adsorbé provoque une modification de cette tension superficielle, dont les manifestations pratiques sont extrêmement variées.
Les différents comportements d'une substance au contact de la surface d'un liquide présentent des analogies intéressantes avec les situations rencontrées sur les solides lorsque la substance est insoluble dans le liquide. Ce sont, par exemple, des composés organiques insolubles dans l'eau, de masse molaire assez grande et non volatils. On peut en déposer de très faibles quantités à la surface de l'eau à partir de solutions diluées dans un solvant volatil. On observe alors, suivant la nature de la goutte déposée, un des trois comportements typiques suivants :
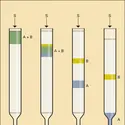
– elle reste entièrement sous forme de lentille à la surface, sans étalement ;
– elle s'étale sur toute la surface en un film mince, suffisamment épais pourtant pour montrer souvent des couleurs d'interférence ;
– ou bien elle laisse une petite partie du liquide s'étendre sous forme d'une couche monomoléculaire dense, l'excès restant sous forme de lentille.
Le premier cas traduit une forte cohésion des molécules du liquide par rapport à leur interaction avec la surface de l'eau. Celle-ci peut, tout au plus, être recouverte par une couche diluée de molécules mobiles d'adsorbat, analogue à un gaz 2 D. La lentille est d'autant plus aplatie qu'elle est sollicitée radialement à sa périphérie par les molécules d'eau et que sa tension superficielle, qui tend à lui donner une forme sphérique, est moins forte. On observe cette évolution en passant des hydrocarbures lourds (huile de paraffine) à de plus légers (essence).
Cette situation est analogue à celle de l'adsorption d'un gaz sur un solide, lorsque, à la pression P0 en équilibre avec la phase 3 D de l'adsorbat, la couche adsorbée n'est encore constituée que d'un gaz 2 D.
Dans le deuxième cas, l'interaction entre la surface de l'eau et les molécules de la goutte l'emporte sur les forces de cohésion des molécules du liquide (cas de certains alcools par exemple), et la goutte s'étale complètement : les premières couches sont retenues à la surface par adsorption multimoléculaire ; au-delà, c'est la gravité qui est responsable de l'uniformité d'épaisseur du film.
Le troisième cas est celui des molécules constituées d'une longue chaîne hydrocarbonée terminée par un groupement tel que − COOH ou − OH. Ces groupements « hydrophiles » sont caractérisés par de fortes interactions avec l'eau par liaison hydrogène, mais le caractère hydrophobe de la chaîne hydrocarbonée est suffisant pour que la substance soit insoluble. Les interactions avec la surface sont au mieux satisfaites par une orientation des molécules perpendiculairement à celle-ci, les extrémités hydrophiles étant en contact avec l'eau et les chaînes hydrocarbonées pointant vers l'extérieur. En présence d'un excès de substance déposé sous forme d'une goutte, il va donc se former à la surface de l'eau une couche monomoléculaire compacte de molécules ainsi orientées. Mais il n'y aura pas d'adsorption multimoléculaire, car les interactions adsorbant-adsorbat imposent au film adsorbé une structure telle que les interactions entre molécules d'adsorbat sont mieux satisfaites dans le liquide 3 D que dans une deuxième ou une troisième couche où le substrat n'attire presque plus. On retrouve donc un cas analogue à celui que l'on rencontre en physisorption sur les solides, lorsque le nombre de couches adsorbées à saturation est limité. Ces films qui ne sont pas mouillés par[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Xavier DUVAL : professeur à l'université de Nancy-I
Classification
Médias
Autres références
-
ABSORPTION VÉGÉTALE
- Écrit par René HELLER et Jean-Pierre RONA
- 4 441 mots
- 6 médias
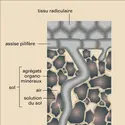
...ions ainsi constituée, est un facteur très important dans la nutrition des plantes : alors que les ions dissous risquent d'être entraînés par les pluies, les ions adsorbés résistent au lessivage et ne sont libérés qu'au fur et à mesure des besoins de la plante. Les anions, comme NO3—, qui ne... -
ANALYTIQUE CHIMIE
- Écrit par Alain BERTHOD et Jérôme RANDON
- 8 890 mots
- 4 médias
Une phase solide peut être utilisée pour séparer un soluté d'une phase liquide. L'extraction liquide-solide utilise la réaction physico-chimiqued'adsorption. Le soluté se fixe alors sur la surface solide de l'adsorbant. Le charbon actif, ou noir de carbone, est très utilisé pour extraire... -
CATALYSE
- Écrit par Henri Jean-Marie DOU et Jean-Eugène GERMAIN
- 8 396 mots
- 7 médias
...semblable à lui-même, capable de poursuivre indéfiniment le même effet. » Ce point de vue était opposé à l'explication dite « physique » de la catalyse par l' adsorption dans les pores du solide, qui provoquerait une concentration locale élevée de réactifs. Nous savons maintenant que les phénomènes d'adsorption... -
CHROMATOGRAPHIE
- Écrit par Robert ROSSET , Louis SAVIDAN et Alain TCHAPLA
- 17 046 mots
- 8 médias
...l'espace le plus restreint possible. Soient respectivement α et β les fractions de A et B qui se trouvent en phase liquide à la température de l'expérience. Celles qui sont adsorbées sur la phase stationnaire sont alors 1 — α et 1 — β. Pour que A soit séparé de B, il faut que les rapports de distribution 1 — α/α... - Afficher les 14 références
Voir aussi