ALCOOLS
Article modifié le
Préparations et modes de formation
Fermentation
La fermentation alcoolique des jus sucrés sous l'action de micro-organismes tels que les levures et les bactéries est une source d'alcools. L'éthanol est fabriqué industriellement par fermentation, sous l'action du complexe enzymatique zymase, présent dans la levure de bière, de mono- et disaccharides comme le glucose, le fructose, le saccharose, etc. provenant de l'hydrolyse de polysaccharides tels que l'amidon, la fécule et la cellulose ou de jus sucrés naturels comme le sucre de canne et les mélasses de sucrerie. Le butanol-1 est obtenu en mélange avec l'acétone par fermentation de sucres en C6 tels que le glucose et le fructose, en C5 (xylose), de disaccharides comme le saccharose et le lactose ou de polysaccharides (amidon), en présence d'une bactérie, le Clostridium acetobutylicum.
Synthèses industrielles
Le méthanol, qui est l'une des plus importantes matières premières industrielles de synthèse, est fabriqué par hydrogénation catalytique du monoxyde de carbone : le gaz de synthèse (CO + 2H2) obtenu soit par oxydation du méthane, soit par gazéification du charbon est traité à 250 0C et sous 50 bars par un catalyseur à base de CuO, ZnO, Al2O3 :

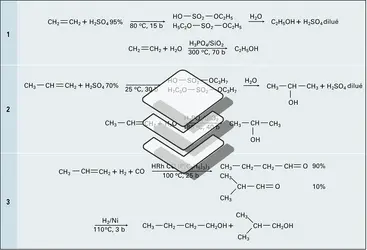
L'éthanol est fabriqué industriellement par hydratation de l'éthylène, soit indirectement par absorption par l'acide sulfurique à 95 p. 100 puis hydrolyse des esters sulfuriques d'éthyle, soit directement par passage du mélange gazeux d'éthylène et d'eau sur un catalyseur d'acide phosphorique sur silice (réactions 1).
L'hydratation indirecte du propylène par l'acide sulfurique à 75 p. 100, puis hydrolyse, ou directe sur acide phosphorique, conduit à l'isopropanol (réactions 2).
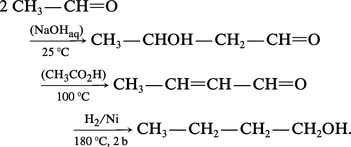
Le butane-1-ol est fabriqué par deux voies : soit l' hydroformylation du propène ou synthèse OXO sur catalyseur au cobalt ou au rhodium, suivie de l'hydrogénation du butanal, avec coproduction d'isobutanol (réaction 3) ; soit l'aldolisation de l'éthanal, la crotonisation de l'aldol puis l'hydrogénation du crotonaldéhyde :
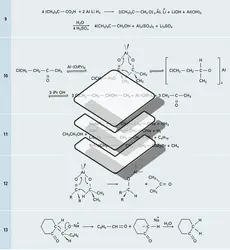
Deux séries d'alcools supérieurs sont fabriquées : un premier groupe d'alcools primaires en C6-C9 utilisé pour la synthèse de plastifiants (esters) et un second en C12 et plus pour la fabrication de détergents. Un procédé général appelé Aldox est utilisé pour la synthèse des alcools du premier groupe : il fait intervenir l'hydroformylation d'une α-oléfine, l'aldolisation de l'aldéhyde obtenu (doublement de la chaîne carbonée), sa crotonisation et une hydrogénation :

Un second procédé permet la synthèse d'alcools primaires à chaîne linéaire à partir d'éthylène : il réalise l'oligomérisation de l'éthylène sur catalyseur de triéthylaluminium, l'oxydation du trialkylaluminium puis l'hydrolyse de l'alcoolate. Le mélange d'alcools obtenus peut contenir des chaînes de C4 à C16 avec un maximum de population en C12 :

Des alcools à longue chaîne ou alcools gras sont obtenus par méthanolyse de corps gras naturels tels que les graisses animales ou végétales puis hydrogénolyse des esters méthyliques des acides gras (réaction 7).
Synthèses de laboratoire
Hydrolyse de dérivés fonctionnels monovalents
L'eau, réactif nucléophile, ou sa base conjuguée HO- qui est présente dans des bases alcalines NaOH et KOH, réagit sur les substrats porteurs de groupements fonctionnels comme les halogénures et les esters. La réaction est une substitution nucléophile, généralement bimoléculaire (SN2), sauf dans le cas des halogénures tertiaires et des esters d'alcools tertiaires où le mécanisme peut être unimoléculaire (SN1). Dans le cas où le réactif est une base forte, la substitution peut être accompagnée d'une élimination et conduire à un éthylénique. Ce mode de préparation ne présente d'intérêt que si le dérivé fonctionnel, soumis à l'hydrolyse, n'est pas lui-même issu de l'alcool. C'est ainsi que l'on prépare industriellement l'alcool allylique par hydrolyse à la soude du chlorure d'allyle, obtenu par chloration radicalaire du propène :

La saponification d'esters d'alcools gras naturels, présents dans les cires, libère l'alcool en formant un sel alcalin de l'acide gras (savon). Par exemple, le traitement par la soude du palmitate de cétyle, principal constituant du blanc de baleine, soustrait l'alcool cétylique et forme le palmitate de sodium :

L'alcoolyse des esters, en catalyse acide, permet de libérer l'alcool de l'ester :

L'hydrolyse des esters sulfuriques d'alkyle, obtenus par addition de l'acide sur un alcène, est une réaction de ce type.
Hydratation des alcènes
Cette réaction, pratiquée industriellement pour la fabrication des alcools en C2, C3 et C4, conduit essentiellement aux alcools secondaires et tertiaires (sauf pour l'éthanol) du fait de l'orientation de l'addition. L'hydratation indirecte d'un alcène terminal par la suite de réactions d'hydroboration, d'oxydation et d'hydrolyse permet d'obtenir l'alcool primaire (réaction 8).
Hydrogénation de dérivés carbonylés
La réduction des aldéhydes et des cétones en alcools primaires et secondaires peut être réalisée par l'action de l'hydrogène en présence de catalyseur métallique comme le platine Pt et le nickel Ni :

Lorsque la chaîne du dérivé carbonylé comporte un groupe réductible par l'hydrogène moléculaire, une liaison éthylénique par exemple, la réduction de la seule fonction carbonyle peut être réalisée par l'action d'un hydrure métallique complexe comme LiAlH4, qui est soluble dans l'éther et décomposé par l'eau, NaBH4 soluble dans l'eau sans décomposition. La réaction suivante montre, sur l'exemple du crotonaldéhyde, l'hydrogénation sélective de la fonction carbonyle, avec conservation de la fonction éthylénique, pour former l'alcool crotylique alors que l'hydrogénation catalytique sur nickel du même aldéhyde insaturé conduit au butanol-1 :

L'hydrure complexe de lithium et d'aluminium est susceptible de réduire en alcools primaires les acides carboxyliques qui résistent à la plupart des agents d'hydrogénation : l'acide pivalique est ainsi transformé en alcool néopentylique (réaction 9). Les esters sont également réduits en alcools par AlLiH4 ou par action d'un excès de sodium en présence d'éthanol absolu ( Bouveault et Blanc) : ce dernier cas est appliqué aux cétones, les aldéhydes étant sensibles aux milieux basiques :

Les esters d'acides gras sont réduits industriellement en alcools gras par l'hydrogène sur catalyseur de chromite de cuivre Cr2O3, CuO (Adkins) : la réaction suivante est l'exemple du laurate de méthyle (obtenu par méthanolyse de la laurine, ou trilaurate de glycérol, extraite de la noix de coco) qui est transformé en alcool laurique :

Une autre réaction spécifique de l'hydrogénation des fonctions carbonyle est l'échange fonctionnel carbonyle-alcool, de Meerwein, Ponndorf, Verley : le dérivé carbonylé à réduire est traité par un alcool secondaire, l'isopropanol, en présence d'une quantité catalytique d'isopropylate d'aluminium. L'échange fonctionnel est réversible et l'équilibre est déplacé vers la formation de l'alcool recherché par élimination de l'acétone formée, qui est le constituant le plus volatil. Cette méthode respecte les autres fonctions réductibles (halogène, nitro, double liaison) [réaction 10].
Addition d'organométalliques sur les fonctions carbonyle
Les organomagnésiens s'additionnent sur le méthanal ou sur un aldéhyde ou encore sur une cétone pour donner respectivement des alcools primaire, secondaire et tertiaire. Cette méthode de préparation est très générale.
Les chlorures d'acides et les esters réagissent sur les organomagnésiens en donnant des cétones, non isolées, qui sont transformées en alcools tertiaires. L'oxyde d'éthylène conduit aux alcools primaires.

L'acétylène s'additionne sur les aldéhydes et les cétones par catalyse basique ou en présence d'acétylure de cuivre et d'argent. Cette réaction est appliquée industriellement à la préparation du butyne-1,4-diol qui, par hydrogénation, conduit au butane-1,4-diol :

Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Médias
Autres références
-
ACÉTALS
- Écrit par Jacques METZGER
- 866 mots
- 1 média
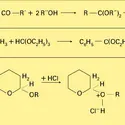
Les acétals sont les composés gem-dialcoxylés c'est-à-dire qui portent sur le même atome de carbone tétracoordiné de la chaîne deux fonction éther-oxyde. Ils dérivent formellement de l'élimination d'une molécule d'eau entre un dérivé carbonylé et deux molécules d'alcool (réaction 1). On distingue...
-
ACIDES-ALCOOLS
- Écrit par Jacques METZGER
- 1 300 mots
- 1 média
Un acide-alcool est une molécule renfermant au moins une fonction acide carboxylique et une fonction alcool.
La nature nous en fournit de nombreux exemples : acides lactique du lait aigri, malique des pommes avant maturité (diacide-monoalcool), tartrique du tartre des vins (diacide-diacool), citrique...
-
ALCÈNES ou OLÉFINES
- Écrit par Jacques METZGER
- 3 642 mots
- 4 médias
Lesalcools tertiaires sont facilement déshydratés par un chauffage modéré en présence d'un catalyseur acide fort. Le mécanisme de cette élimination est normalement unimoléculaire E1 : le catalyseur acide transforme le mauvais groupe partant HO- en bon groupe partant H2O et permet ainsi... -
ALCOOL ÉTHYLIQUE ou ÉTHANOL
- Écrit par Fernand COUSSEMANT
- 694 mots
Alcool primaire, liquide incolore, d'odeur agréable, miscible à l'eau en toutes proportions, miscible à de nombreux solvants organiques, l'éthanol ou alcool éthylique, CH3—CH2OH, a les caractéristiques suivantes :
Masse moléculaire : 46,07 g
Masse spécifique : 0,789 3...
- Afficher les 20 références
Voir aussi
- HYDROLYSE
- HYDROGÈNE LIAISON
- ORGANOMAGNÉSIENS COMPOSÉS
- SOLUBILITÉ
- HYDROXYLE ou OXHYDRYLE
- HYDRATATION
- HYDROGÉNATION
- CÉTONES
- ADDITION, chimie
- DÉSHYDROGÉNATION
- ALDÉHYDES
- POLARISATION, chimie
- OXYDATION
- DÉSHYDRATATION
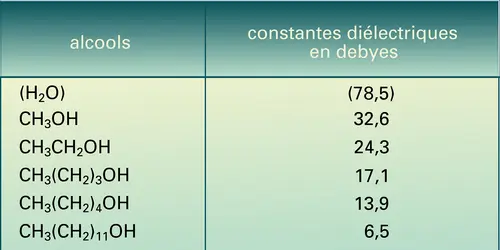
- CONSTANTE DIÉLECTRIQUE
- SAPONIFICATION
- ESTÉRIFICATION
- ALCOOLYSE
- MEERWEIN-PONNDORF-VERLEY RÉACTION DE
- BOUVEAULT & BLANC RÉACTION DE
- ALCOOLATES
- ÉLECTRONIQUE STRUCTURE
- NOMENCLATURE, chimie
- RÉDUCTION, chimie
- BUTANOL
- ISOPROPANOL
- ALCOOLIQUE FERMENTATION
- TEMPÉRATURE D'ÉBULLITION
- HALOGÉNURES D'ALKYLE
- HYDROFORMYLATION ou RÉACTION OXO