AMIDES
Article modifié le
Applications
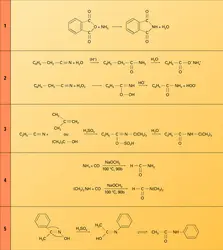
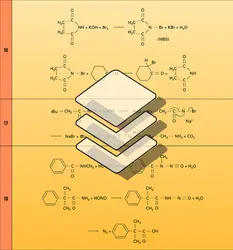
La fonction amide permet un nombre limité de synthèses pratiques : la dégradation de Hofmann qui donne les amines primaires ; la synthèse d'acides encombrés par diazo-hydrolyse des amides primaires, obtenus par hydratation des nitriles encombrés, d'accès facile ; la synthèse organomagnésienne des aldéhydes, à partir du diéthylformamide. Toutefois, l'acétylation des arylamines constitue une assez bonne protection de cette fonction contre l'oxydation et souvent on opère certaines substitutions aromatiques sur le dérivé acétylé de l'arylamine. L'hydrolyse régénère la fonction amine ainsi protégée (nitration de l'aniline).
L' acétamide est employé comme solvant polaire dans l'industrie (colorants). Son caractère amphotère et sa neutralité en font un additif antiacide précieux des laques, cosmétiques, explosifs. Le diméthylformamide et la N-méthylpyrrolidone sont des solvants industriels utilisés dans l'extraction sélective de l'acétylène des fractions de craquage en C2, du butadiène des coupes en C4 et dans la séparation des aromatiques et des aliphatiques par distillation extractive.
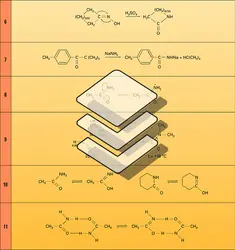
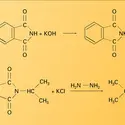
Certains lactames sont les monomères dont la polymérisation donne des résines de hautes qualités (Nylons 6 et 12).
Certains polyimides sont des polymères remarquablement stables vis-à-vis de la température (formule 21).
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Médias
Autres références
-
ACÉTAMIDE (éthanamide)
- Écrit par Dina SURDIN
- 328 mots
CH3—CO—NH2
Masse moléculaire : 59,07 g
Masse spécifique : 1,16 g/cm3
Point de fusion : 82 0C
Point d'ébullition : 222 0C.
Monoamide primaire se présentant en cristaux blancs hexagonaux ou rhomboédriques. La structure cristalline de l'acétamide déterminée par les rayons X (méthode du...
-
AMINES
- Écrit par Jacques METZGER
- 3 235 mots
- 4 médias
-
CARBOXYLIQUES ACIDES
- Écrit par Jacques METZGER
- 5 506 mots
- 6 médias
Formation d'un amide. Le nucléophile est l'ammoniac ou encore une amine primaire ou secondaire. On chauffe le sel d'ammonium ou d'aminium qui se déshydrate en amide. En fait, le sel est en équilibre avec l'acide et l'ammoniac, et c'est la réaction entre ces deux partenaires qui conduit, par une... -
NITRILES
- Écrit par Jacques METZGER
- 1 794 mots
- 1 média
Voir aussi