AMIDES
Article modifié le
Bibliographie
N. L. Allinger, Chimie organique, 3 vol., McGraw-Hill, 1976
H. Beyer & W. Walter, Lehrbuch der Organischen Chemie, Hirzel, Stuttgart, 20e éd. 1984
F. A. Carey, Organic Chemistry, Dubuque, 6e éd. 2006
F. A. Carey & J. Sundberg, Advanced Organic Chemistry, Plenum Press, New York, 4e éd. 2000-2001
A. Chauvel, G. Lefebvre & L. Castex, Procédés de pétrochimie, Technip, Paris, 2e éd. 1985
D. Barton & W. D. Ollis, Comprehensive Organic Chemistry, vol. II, Pergamon Press, Oxford, 1979
J. March, Advanced Organic Chemistry, Wiley & Sons, New York, 3e éd. 1985
J. McMurry, Organic Chemistry, Brooks-Cole Publishing Company, Belmont, 6e éd. 2004
T. W. G. Solomons, Organic Chemistry, J. Wiley & Sons, 9e éd. 2006
A. Streitwieser Jr. & C. H. Heathcock, Introduction à la chimie organique, Ellipses-Marketing, Paris, 1986
K. Weissermel & H. J. Arpe, Chimie organique industrielle, De Boeck Université, Paris-Bruxelles, trad. de la 3e éd. angl., 2000.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Médias
Autres références
-
ACÉTAMIDE (éthanamide)
- Écrit par Dina SURDIN
- 328 mots
CH3—CO—NH2
Masse moléculaire : 59,07 g
Masse spécifique : 1,16 g/cm3
Point de fusion : 82 0C
Point d'ébullition : 222 0C.
Monoamide primaire se présentant en cristaux blancs hexagonaux ou rhomboédriques. La structure cristalline de l'acétamide déterminée par les rayons X (méthode du...
-
AMINES
- Écrit par Jacques METZGER
- 3 235 mots
- 4 médias
-
CARBOXYLIQUES ACIDES
- Écrit par Jacques METZGER
- 5 506 mots
- 6 médias
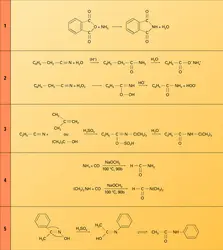
Formation d'un amide. Le nucléophile est l'ammoniac ou encore une amine primaire ou secondaire. On chauffe le sel d'ammonium ou d'aminium qui se déshydrate en amide. En fait, le sel est en équilibre avec l'acide et l'ammoniac, et c'est la réaction entre ces deux partenaires qui conduit, par une... -
NITRILES
- Écrit par Jacques METZGER
- 1 794 mots
- 1 média
Voir aussi