ANTIBIORÉSISTANCE
Article modifié le
Les nouvelles technologies au service de la lutte contre l’antibiorésistance
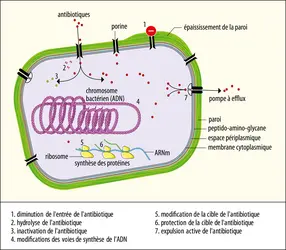
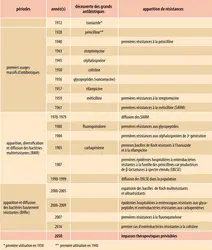
Pour continuer la lutte contre l’antibiorésistance, le microbiologiste est en première ligne dans les laboratoires pour isoler les bactéries pathogènes, détecter et interpréter les éventuels mécanismes de résistance associés. C’est un métier en perpétuelle évolution qui doit s’adapter et évoluer aussi rapidement que l’antibiorésistance. L’apport des nouvelles technologies dans le suivi et la détection quasi quotidienne des mécanismes de résistance permettent de poursuivre la recherche et continuer le combat contre les infections bactériennes. Le développement de cette lutte s’opère à trois niveaux.
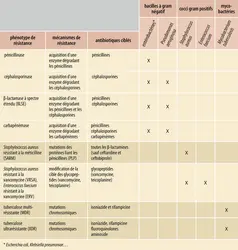
Le premier niveau est l’amplification du suivi classique de l’antibiorésistance. Le nombre de tests de détection des résistances au laboratoire est en perpétuelle augmentation. Parmi les tests classiques, l’antibiogramme reste la technique de référence car elle est bien standardisée, facilement applicable et réalisée au quotidien, mais la nécessité d’une culture bactérienne pure et le temps de pousse des bactéries (de 18 à 24 heures) constituent des freins à la prise en charge des patients dans un délai optimal. C’est pourquoi des tests rapides ont été développés afin de pouvoir isoler beaucoup plus vite les patients dans le but d’empêcher leur dissémination et la survenue d’épidémies. Dans ce cadre, les tests phénotypiques permettent en quelques minutes de mettre en évidence la présence d’enzymes liées à la résistance (pénicillinases, carbapénémases…). Les tests génotypiques recherchent quant à eux la présence d’un gène d’intérêt (gène de résistance ou de virulence) dans la bactérie. Ils sont souvent utilisés pour identifier rapidement un micro-organisme spécifique et (ou) un phénotype de résistance particulier et sont aujourd’hui bien adaptés au diagnostic de routine. C’est le cas, par exemple, du test recherchant la tuberculose résistante à la rifampicine et de celui recherchant le Staphylococcus aureus résistant à la méticilline, menés directement à partir du prélèvement.
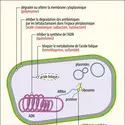
Le deuxième niveau est le développement du séquençage de l’ADN d’isolats et de prélèvements. L’essor de nouveaux outils technologiques permet aussi d’accéder rapidement à de plus grandes quantités d’informations, en recherche, pour mieux comprendre la dissémination des gènes de résistance. Par exemple, le séquençage haut débit de l’ADN est un outil particulièrement efficace pour mettre en évidence la composition en gènes de résistance (dont l’ensemble est encore appelé « résistome ») d’un échantillon complexe, sans avoir besoin d’isoler au préalable les bactéries. Il peut s’appliquer à de nombreuses situations comme l’analyse du contenu génomique d’une souche bactérienne, d’un échantillon clinique ou environnemental (effluent, sol…). Le séquençage a par exemple permis d’améliorer la compréhension des supports des gènes de résistance et de virulence, d’établir des relations phylogéniques entre isolats du monde entier, de retracer l’apparition et la dissémination d’une épidémie ou d’un gène de résistance donné. Outre le séquençage haut débit, d’autres techniques ciblant l’ARN des bactéries (transcriptomique), les protéines exprimées à partir de ces ARN (protéomique) ou les métabolites (métabolomique) sont utilisées en recherche. L’ensemble de ces techniques permet de dessiner en un moment précis le paysage des résistances d’un échantillon, et d’en suivre l’évolution.
Enfin, le troisième niveau est l’intégration dans un réseau d’information. Outre ces technologies, l’amélioration des outils informatiques de surveillance et de communication ainsi que la création de nouveaux réseaux et de comités de surveillance permettent une coordination étroite afin de lutter[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Aurélie CHABAUD : pharmacienne-biologiste spécialisée, laboratoire de bactériologie virologie hygiène, CHU de Limoges
- Sylvain MEYER : assistant hospitalo-universitaire, laboratoire de bactériologie virologie hygiène, CHU de Limoges
- Marie-Cécile PLOY : professeure des Universités, praticienne hospitalière, laboratoire de bactériologie virologie hygiène, CHU de Limoges
Classification
Médias
Autres références
-
ALIMENTATION (Aliments) - Risques alimentaires
- Écrit par Jean-Pierre RUASSE
- 4 759 mots
- 1 média
...thérapeutique anti-infectieuse d'une part, accélération de la croissance d'autre part. Mais cette utilisation entraîne trois ordres de conséquences néfastes : augmentation de la résistance des germes pathogènes, transformation en pathogènes de variétés jusque-là saprophytes, enfin création chez le consommateur... -
ANTIBIOTIQUES
- Écrit par Aurélie CHABAUD , Sylvain MEYER et Marie-Cécile PLOY
- 6 760 mots
- 6 médias
Larésistance aux antibiotiques constitue une menace mondiale, accentuée par le mésusage de ces médicaments. Une utilisation raisonnée et raisonnable des antibiotiques est nécessaire pour limiter son apparition et sa diffusion. Pour cela, la prescription d’antibiotiques s’appuiera sur la règle de « médecine... -
ANTIBIOTIQUES - (repères chronologiques)
- Écrit par Paul MAZLIAK
- 461 mots
1903 Découverte du Trypan Röd (premier antibiotique anti-parasitaire) par Paul Ehrlich (1854-1915).
1909 Découverte du Salvarsan (606), puissant anti-syphilitique par Paul Ehrlich.
1921 Synthèse du Stovarsol (anti-microbien peu toxique dérivé de l'arsenic) par Ernest Fourneau (1872-1949)....
-
BACTÉRIES
- Écrit par Jean-Michel ALONSO , Jacques BEJOT et Patrick FORTERRE
- 11 055 mots
- 3 médias
...gluante très riche en eau, les biofilms forment des biomasses épaisses au sein desquelles les micro-organismes acquièrent des propriétés particulières telles qu'une résistance très élevée aux antibiotiques. Les biofilms formés par des bactéries pathogènes sont particulièrement difficiles à éliminer et représentent... - Afficher les 17 références
Voir aussi
- VIRULENCE, microbiologie
- ENZYMES
- MICRO-ORGANISME
- GÉNOTYPE
- INFECTION
- SÉQUENÇAGE, génétique moléculaire
- RÉSISTANCE, biologie
- EAUX USÉES
- ENTÉROBACTÉRIES
- RIFAMPICINE
- RISQUES SANITAIRES
- SANTÉ DANS LE MONDE
- CHROMOSOMES
- RÉSISTANCE BACTÉRIENNE
- PÉNICILLINE
- ÉPIDÉMIES
- CONJUGAISON BACTÉRIENNE
- ISONIAZIDE
- TRANSPOSON
- SIRTURO ou BEDAQUILINE
- ÉLEVAGE INDUSTRIEL
- MICROBIOTES
- COLISTINE