ANTICORPS MONOCLONAUX
Article modifié le
Molécules thérapeutiques
À l'origine, la grande majorité des essais cliniques ont donné des résultats décevants, à l'exception de l'anticorps OKT3, utilisé dans la prévention du rejet aigu des allogreffes. Plusieurs facteurs furent à l'origine de cette désillusion : choix hâtifs d'anticorps aux propriétés mal contrôlées (affinité médiocre, spécificité douteuse, faible capacité à recruter les cellules effectrices du système immunitaire), modes d'administration empiriques et surtout origine non humaine des anticorps. Les anticorps de première génération ont donc constitué des outils remarquables pour la recherche, mais décevants pour l'immuno-intervention thérapeutique.
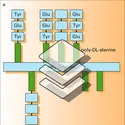
Les connaissances sur la structure des anticorps et les progrès de la biologie moléculaire ont permis d'améliorer progressivement l'utilisation thérapeutique des immunoglobines. Un anticorps est constitué de deux chaînes, une chaîne lourde et une chaîne légère, chacune possédant une région variable, responsable de la fixation à l'antigène, et une région constante, assurant les interactions avec des molécules « tueuses » (les molécules du complément) ou avec des cellules de l'immunité (exprimant des récepteurs pour ces régions constantes, ou RFc), telles que les macrophages, les polynucléaires ou les cellules natural killer...).
Ces deux régions étant codées par des gènes différents, les chercheurs ont fabriqué des anticorps chimériques homme-souris en associant les gènes humains des régions constantes aux gènes de souris des régions variables de l'anticorps monoclonal initial. Les anticorps chimériques sont beaucoup moins immunogènes, étant composés à près de 80 p. 100 de séquences d'origine humaine, et, la région constante étant désormais humaine, leurs propriétés effectrices sont fortement améliorées. Certains anticorps chimériques ont donné des résultats cliniques encourageants, ce qui a conduit à leur approbation par la Food and Drug Administration américaine et à l'obtention d'autorisations européennes de mise sur le marché (anticorps anti-HER2/Neu, un récepteur de facteur de croissance pour le traitement de cancers du sein métastatiques, anticorps anti-CD20 – CD20 étant une molécule exprimée à la surface des lymphocytes B – pour le traitement de lymphomes non hodgkiniens folliculaires, anticorps anti-plaquettaire pour le traitement des complications thrombotiques lors d'interventions chirurgicales coronariennes...).
De nouvelles générations d'anticorps sont actuellement en cours d'évaluation : grâce aux techniques de modélisation moléculaire, d'analyse par mutations, de cristallographie aux rayons X et de spectrométrie de masse, il est en effet possible de détailler parfaitement l'interaction d'un anticorps avec son antigène, ce qui permet de fabriquer des anticorps humanisés, ne contenant plus que les régions de l'anticorps de souris directement responsables de la fixation à l'antigène. Cependant, l'affinité des anticorps humanisés est souvent plus faible que celle des anticorps parentaux, voire perdue. Il est possible de restaurer cette affinité par modification des régions entourant le site de fixation à l'antigène, mais ces manipulations restent complexes, onéreuses, avec un résultat aléatoire.
En fait, il ne sera sans doute plus nécessaire de modifier des anticorps de souris. En effet, des lignées de souris transgéniques produisant des anticorps humains ont été créées au prix d'efforts techniques et financiers considérables. Il a fallu d'abord inactiver chez ces souris la plupart des gènes responsables de la production des anticorps, puis introduire les gènes humains correspondants. Plus de trois quarts des gènes codant les immunoglobulines humaines ont été ainsi transférés dans le génome de ces souris[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Michel MAUGRAS : maître de conférences à l'université de Nancy-I
- Jean-Luc TEILLAUD : directeur de recherche à l'Institut national de la santé et de la recherche médicale
Classification
Autres références
-
ANTIGÈNES
- Écrit par Joseph ALOUF
- 7 384 mots
- 5 médias
...des lymphocytes T stéréospécifiquement complémentaires de ces entités. Ainsi, l'analyse par diffraction aux rayons X de la zone de contact entre le paratope d'un anticorps monoclonal antilysozyme d'œuf de poule et le lysozyme dans le complexe cristallisé a montré que l'épitope majeur impliqué dans... -
BIOLOGIE - La biologie moléculaire
- Écrit par Gabriel GACHELIN
- 7 405 mots
- 8 médias
La biologie moléculaire n'est pas en elle-même une discipline, c'est une expression commode pour désigner la « molécularisation » de la biologie, autrement dit le rôle central de l'approche moléculariste dans l'étude de la vie. Chacun y met à peu près le même contenu : la traduction des phénomènes du...
-
CANCER - Cancer et santé publique
- Écrit par Maurice TUBIANA
- 14 762 mots
- 8 médias
D'autres méthodes fondées sur la recherche sont déjà entrées dans les traitements, notammentl'usage d'anticorps monoclonaux se fixant sur les récepteurs membranaires de facteurs de croissance ou d'autres récepteurs présents sur les cellules malignes, sur lesquels on peut fixer soit des... -
FIÈVRES HÉMORRAGIQUES VIRALES
- Écrit par Yannick SIMONIN
- 4 744 mots
- 2 médias
...convalescents a été utilisé avec succès chez certains patients atteints de fièvre hémorragique argentine (Junin). En Chine, une injection intraveineuse unique d’anticorps monoclonaux (mAbs pour monoclonal antibodies) murins contre un hantavirus a été développée et appliquée chez des volontaires en bonne santé.... - Afficher les 14 références
Voir aussi
- IMMUNOTHÉRAPIE
- PURIFICATION, physico-chimie
- ADN RECOMBINANT
- ANTICORPS CHIMÉRIQUES
- ANTICORPS INTRACELLULAIRES
- ANTICORPS HUMANISÉS
- PHAGE DISPLAY
- DOSAGE, biologie et médecine
- ANTICORPS
- CLONE
- IMMUNOGLOBULINES
- LYMPHOCYTES
- ÉPITOPES ou DÉTERMINANTS ANTIGÉNIQUES
- FUSIONS CELLULAIRES
- RECONNAISSANCE, immunologie
- HYBRIDOMES
- HYBRIDATION CELLULAIRE
- MONOCLONAL
- PROTÉINES
- TRANSGENÈSE
- LYMPHOCYTES B
- ANIMAUX TRANSGÉNIQUES