BISMUTH
Article modifié le
Le bismuth, de symbole Bi, est l'élément chimique de numéro atomique 83. C'est le plus lourd du groupe Vb de la classification périodique. Il vient après l'azote, le phosphore, l'arsenic et l'antimoine, mais, contrairement à ceux-ci, son caractère métallique est net. Signalé par Basile Valentin au xve siècle, il fut distingué comme un métal particulier par Agricola en 1558 et appelé bismutum ou cinereum plumbum. En 1737, Hellot prépare, à partir d'un minerai de bismuth et de cobalt, un bouton de « véritable bismuth ». C'est seulement à cette époque qu'il apparaît définitivement à tous comme un métal pur, différent du plomb et de l'étain, et non comme un mélange.
L'étymologie du mot bismuth n'est pas connue. Parmi plusieurs hypothèses proposées, on retient généralement une origine germanique, bismuth dérivant de « wis mat » pour weisse Masse (masse blanche) dans le langage des mineurs.
Le bismuth, métal cher et peu abondant, est un sous-produit des métallurgies du cuivre et surtout du plomb. Il est utilisé avant tout pour ses propriétés physiques à l'état métallique dans des alliages très facilement fusibles et pour ses propriétés thérapeutiques à l'état de composés de Bi3+. La production mondiale est de l'ordre de 2 000 tonnes par an.
Propriétés physiques
Le bismuth est un solide cristallisé blanc avec quelques reflets rougeâtres. Dur, fragile, cassant, facilement pulvérisable, il donne des vapeurs d'un bleu verdâtre et présente, comme l'antimoine, le gallium et l'eau, la particularité d'être moins dense à l'état solide qu'à l'état liquide. Il est fortement thermoélectrique, surtout au contact de l'antimoine, et très diamagnétique, mais sa conductibilité thermique est cinquante fois plus faible que celle de l'argent. Sa répartition électronique se compose de couches K, L, M, N, et O comprenant respectivement 2, 8, 18, 32 et 18 électrons. La couche externe P incomplète comporte cinq électrons, 6 s2 et 6 p3, dont la perte fournit les ions Bi3+ et Bi5+.
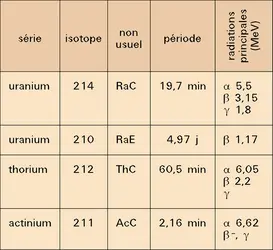
À côté de 209Bi, que l'on considère soit comme un isotope stable, soit comme un émetteur de rayonnement α de période extrêmement longue (3.1017 ans), de nombreux isotopes radioactifs sont connus. Dans les chaînes de désintégration, se forment les isotopes naturels 210, 211, 212 et 214. 213Bi appartient à la famille radioactive du neptunium ; sa période est de 46 minutes et ses radiations principales sont α 5,9 MeV et β 1,2 MeV. Les autres caractères du métal sont résumés dans le tableau.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Anne-Marie TRISTANT : pharmacien conseil à la Sécurité sociale
Classification
Médias
Autres références
-
AIMANTS
- Écrit par Roger FONTAINE
- 6 274 mots
- 13 médias
Le premier aimant fabriqué à partir de poudres a été élaboré en 1943, avant que la théorie des grains fins ne fasse son apparition.Il s'agit du composé intermétallique MnBi qui, cristallisant dans le système cubique, présente une anisotropie magnéto-cristalline très élevée. La préparation de... -
ARSENIC
- Écrit par Jean PERROTEY
- 4 499 mots
- 2 médias
-
MÉTAL ARTS DU
- Écrit par Catherine ARMINJON
- 11 110 mots
- 2 médias
...mais la qualité des alliages permet de fabriquer en toute sécurité des étains destinés à tous les usages. Proche de l'étain et un peu plus fusible, le bismuth est un métal blanc argentin, légèrement jaunâtre, utilisé en alliage avec d'autres métaux tels que le plomb et l'étain, dont il augmente la dureté.... -
POLONIUM
- Écrit par Georges BOUISSIÈRES et Encyclopædia Universalis
- 2 936 mots
- 2 médias
Des quantités pondérables (échelle du gramme) sont synthétisées à partir du bismuth que l'on soumet au flux neutronique intense d'un réacteur nucléaire. Le polonium 210 est formé suivant le processus :la section efficace de la capture des neutrons thermiques étant de 0,020 × 10...
Voir aussi