CHIMIE Chimie durable
Quelques exemples de chimie verte
Depuis 1990 environ, la chimie verte connaît un développement considérable dans la plupart des domaines de recherche et à un niveau mondial. Les exemples suivants sont représentatifs des efforts fournis en méthodologie de synthèse et en optimisation de procédés.
Une approche méthodologique : l'économie d'atomes
L' économie d'atomes est une méthodologie de synthèse qui consiste à maximiser le nombre d'atomes de réactifs transformés en produit (celui souhaité) au cours de la synthèse. Barry M. Trost (né en 1941), de l'université de Stanford (États-Unis), l'a introduite en 1991, et a défini le pourcentage d'économie d'atomes (PÉA) par la formule : PÉA = (masse molaire totale des atomes utilisés/masse molaire des réactants) ×100 p. 100.
Roger A. Sheldon (né en 1942), de l'université de Delft (Pays-Bas), a introduit en 1992 le pourcentage d'utilisation atomique (PUA), défini par : PUA = (masse molaire du produit désiré/masse totale des produits obtenus) ×100 p. 100.
Puisque, lors d'une réaction chimique, la masse molaire totale des produits obtenus est égale à la masse molaire totale des réactants, le PUA est égal au PÉA.
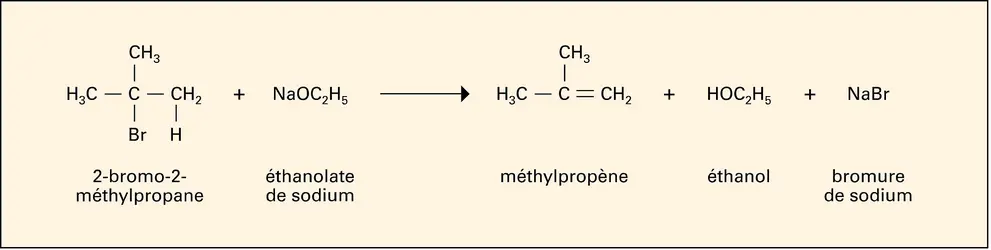
Par exemple, la réaction permettant d'obtenir du méthylpropène par déhydrohalogénation du 2-bromo-2-méthylpropane par l'éthanolate de sodium (fig. 1) a un pourcentage d'utilisation atomique de : PUA = M [méthylpropène]/ (M [méthylpropène] + M [éthanol] + M [bromure de sodium]) ×100 p. 100 = 56/(56 + 46 + 103) ×100 p. 100 = 27 p. 100.
Cela signifie que, même si le rendement de la réaction est de 100 p. 100, seuls 27 p. 100 en masse des atomes de réactifs sont incorporés dans le produit désiré. Les 73 p. 100 qui restent constituent des déchets qu'il faudra séparer, puis traiter pour les recycler ou les détruire, avec un impact environnemental et financier important. Un procédé sera donc d'autant plus efficace, au sens « durable », que son utilisation atomique sera proche de 100 p. 100.
Sheldon a également introduit deux autres indicateurs d'efficacité : le facteur E et le quotient environnemental QE. Le facteur E est le rapport de la masse totale des déchets sur la masse du produit désiré. Un procédé est d'autant plus « propre » que E est petit (les procédés de chimie pharmaceutique ont des facteurs E très élevés, compris entre 25 et 100). La valeur théorique de E, obtenue pour un rendement de 100 p. 100, est reliée au PUA par la relation PUA = 1/(1 + E). Pour tenir compte des conditions réelles de la synthèse (réactifs en excès, toxiques...), Sheldon introduit un facteur multiplicatif Q, supérieur à 1. Le produit QE est le quotient environnemental, qui mesure quantitativement l'impact du procédé réel sur l'environnement.
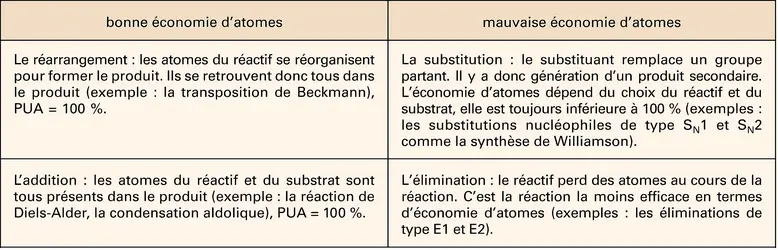
Ces concepts permettent pour la première fois d'apprécier l'efficacité d'une réaction, non seulement par son rendement, mais également par son impact environnemental. Les grandes familles de réactions sont désormais classées en fonction de leur économie d'atomes (cf. tableau), ce qui permet d'optimiser les schémas de synthèse dès leur conception : on privilégiera les réactions à forte économie d'atomes pour réduire la quantité de déchets produits, voire les supprimer totalement. Le quotient environnemental peut varier en fonction de la toxicité des réactifs : le facteur Q d'un produit toxique sera par exemple très élevé et on cherchera à le remplacer par un produit non toxique pour réduire QE.
La catalyse : pilier de la chimie verte
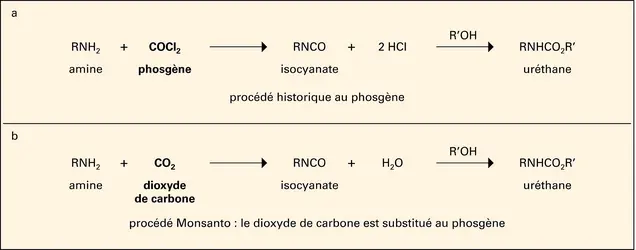
La catalyse joue un rôle central dans la chimie moderne et est considérée comme le pilier de la chimie verte. En effet, elle permet de réduire la consommation d'énergie, ce qui présente un intérêt économique et environnemental, de diminuer les efforts de[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Hagop DEMIRDJIAN : docteur en chimie théorique, professeur agrégé à l'École normale supérieure
Classification
Médias
Autres références
-
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 367 mots
- 7 médias
Un acide est un corps capable de céder un ou des protons (une particule fondamentale chargée d'électricité positive) et une base est un corps capable de capter un ou des protons. Chacun a ses caractéristiques. Les acides ont une saveur aigre (l'adjectif latin acidus signifie « aigre...
-
AIR, élément
- Écrit par Georges KAYAS
- 719 mots
- 1 média
Anaximène (~ 556-~ 480), à la différence de Thalès, enseignait que toute substance provient de l'air (pneuma) par raréfaction et condensation ; dilaté à l'extrême, cet air devient feu ; comprimé, il se transforme en vent ; il produit des nuages, qui donnent de l'eau lorsqu'ils sont...
-
ANALYSE ET SYNTHÈSE, chimie
- Écrit par Pierre LASZLO
- 1 526 mots
- 1 média
Ces deux notions, en principe complémentaires et réciproques, ne le sont pas en fait. Certes, les deux tendances à l'analyse et à la synthèse s'opposent, la première visant à couper les entités chimiques en petits morceaux et la seconde se donnant pour objectif la reconstruction des ensembles mis à...
-
ANALYTIQUE CHIMIE
- Écrit par Alain BERTHOD et Jérôme RANDON
- 8 890 mots
- 4 médias
« C'est dans les cas situés au-delà de la règle que le talent de l'analyste se manifeste. L'important, le principal est de savoir ce qu'il faut observer. » Edgar Allan Poe (Histoires extraordinaires, 1844)
La chimie analytique est la branche de la chimie qui a pour but l'identification,...
- Afficher les 82 références