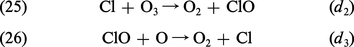CHLORE
Article modifié le
Le problème de l'équilibre chlore-soude
Jusque vers 1950, les besoins en soude du marché étaient normalement couverts par la soude de caustification du carbonate de sodium et la soude électrolytique. La progression rapide de la production du chlore a alors fait craindre que l'on ne dispose de trop de soude, d'où la préoccupation de fabriquer du chlore sans soude. Ce « problème » a donné lieu à une très abondante littérature, à divers essais, et à quelques rares réalisations : deux usines aux États-Unis traitant, l'une du chlorure de sodium, l'autre du chlorure de potassium par l'acide nitrique afin d'obtenir du chlore et des nitrates, et deux usines électrolysant de l'acide chlorhydrique. Notons toutefois que la mise au point des procédés d'oxychloration à partir de l'acide chlorhydrique est sans doute une conséquence de cette préoccupation.
Indiquons aussi que, compte tenu de ce problème, on a fermé les ateliers de caustification, on a étendu les utilisations du carbonate de sodium en le substituant autant que faire se pouvait à la soude, et on a même préparé du carbonate de sodium par... carbonatation de la soude.
En 1966, la caustification était pratiquement arrêtée en France, et un équilibre entre chlore et soude s'est maintenu jusqu'en 1971, où est apparue une pénurie de soude.
On se trouve en fait devant deux coproduits dont les productions liées l'une à l'autre répondent sensiblement aux besoins du marché ; des divergences peuvent toutefois apparaître et, s'il est aisé de répondre rapidement à une demande plus élevée en chlore, il n'est pas aussi facile de réaliser une surproduction de soude. Celle-ci constitue en fait le produit fatal car, si on peut la stocker, on ne peut pas stocker le chlore pour des raisons d'encombrement mais, surtout, de sécurité.
En France, 94,5 p. 100 du chlore produit proviennent de l'électrolyse de solutions aqueuses de NaCl, 3 p. 100 de solutions aqueuses de KCl et 2,5 p. 100 de l'électrolyse ignée de NaCl.
On doit également souligner que la fabrication de nombreux produits chlorés résulte très fréquemment de la chloration de composés carbonés, laquelle donne de l'acide chlorhydrique comme sous-produit. On est donc amené à développer de plus en plus l'obtention de chlore à partir de cet acide résiduaire, soit par électrolyse, soit de préférence par une adaptation originale de l'ancien procédé Deacon : l' oxychloration.
Les tentatives de modernisation de ce procédé avaient montré que, même en présence de catalyseurs actifs, il convenait de travailler à une température trop élevée pour que la réaction soit complète : d'où la nécessité de séparer le chlore de l'acide chlorhydrique et de recycler ce dernier.
En procédant à l'oxydation du chlorure d'hydrogène en présence d'éthylène qui fixe, sous forme de dichloréthane, le chlore formé extemporanément, on déplace complètement l'équilibre et la réaction devient complète ; c'est le principe de l'oxychloration.
Appliquée initialement par F. Raschig pour préparer le chlorobenzène, produit intermédiaire de la fabrication du phénol, elle s'est développée de plus en plus pour obtenir le dichloroéthane à partir duquel on prépare le chlorure de vinyle par craquage :
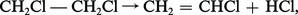
Il convient de noter que le chlore produit dans les procédés d'oxychloration (dont le procédé « Chloé »), et qui est transformé in situ, sans être isolé, n'est pas inclus dans les statistiques de production de chlore.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Henri GUÉRIN : ingénieur de l'École supérieure de physique et chimie industrielles, professeur honoraire de l'université de Paris-XI
Classification
Médias
Autres références
-
ARMES - Armes lourdes
- Écrit par Alain BRU
- 3 927 mots
- 2 médias
...avril 1915, près d'Ypres, la première attaque chimique massive ; elle fit environ dix mille morts ou hommes hors de combat. Il s'agissait de vapeur de chlore. La suite du conflit connut une « course » parallèle aux produits plus toxiques, mais aussi aux équipements protecteurs. Les effets létaux furent... -
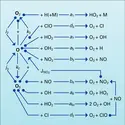
ATMOSPHÈRE - Chimie
- Écrit par Marcel NICOLET
- 3 554 mots
- 5 médias
-
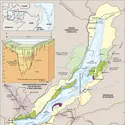
BAÏKAL LAC
- Écrit par Laure ARJAKOVSKY et Pierre CARRIÈRE
- 4 074 mots
- 2 médias
...la quantité des sulfates était passée de 330 000 tonnes par an en 1962 à 470 000 tonnes par an en 1992 ; pour la même période, le taux des dérivés du chlore a augmenté de 49 000 à 69 000 tonnes par an, et les matières organiques sont passées de 500 000 à 790 000 tonnes par an. S'agissant de la pollution... -
BERTHOLLET CLAUDE LOUIS (1748-1822)
- Écrit par Michelle GOUPIL-SADOUN
- 1 193 mots
...édition en 1804, l'ouvrage de Berthollet resta longtemps le manuel des ouvriers en teinture. Il découvrit aussi le procédé du blanchiment des toiles par le chlore. La chimie industrielle lui doit enfin des études importantes sur la fabrication et la nature des aciers, qu'il réalisa en 1786 avec Vandermonde... - Afficher les 23 références
Voir aussi
- SOUDE (hydroxyde de sodium)
- PHOSGÈNE (oxychlorure de carbone)
- BIOXYDE DE CHLORE
- MINÉRALE CHIMIE
- CHIMIQUES SUBSTANCES, écotoxicologie
- EAU DE JAVEL (hypochlorite de sodium)
- CHIMIQUES INDUSTRIES
- CHLORURE DE SODIUM
- CATHODE
- ANODE
- DISMUTATION, chimie
- LEBLANC PROCÉDÉ
- SEL GEMME
- HOOKER CELLULE
- GAZ DE COMBAT
- DEACON PROCÉDÉ
- DIAPHRAGME PROCÉDÉ AU
- MERCURE CELLULES À CATHODE DE
- PECHINEY CELLULE
- CHLORHYDRIQUE ACIDE
- FLUIDES FRIGORIGÈNES
- ÉLECTROLYSE
- CAOUTCHOUCS SYNTHÉTIQUES
- EAU APPROVISIONNEMENT ET TRAITEMENT DE L'