CHROMATOGRAPHIE
Article modifié le
Principes de séparation
Chromatographie en phase liquide
Chromatographie par adsorption
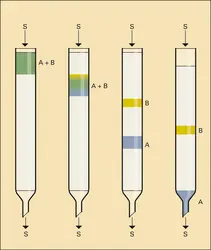
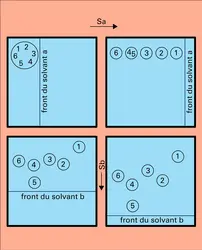
Les phases fixes adsorbantes (cf. adsorption) les plus employées sont l'alumine et le gel de silice, à des granulométries, porosités et activités adaptées au cas à résoudre. Le carbone poreux graphitisé, la magnésie, le zircone et le rutile poreux sont aussi utilisés. Il faut citer aussi le florisil (coprécipité de silice et magnésie) très employé en C.C.M. et chromatographie flash à colonne ouverte. Quand on met un tel solide en présence d'un gaz ou d'un liquide, il fixe sur sa surface les molécules de la phase fluide : elles y sont adsorbées. Ce phénomène est plus ou moins marqué suivant la nature des surfaces, suivant celle des corps en présence, et dépend de la température. Pour un adsorbant donné, l'adsorption d'un produit dissous dans un liquide solvant peut être caractérisée par le rapport x/m, où x est la masse de ce produit adsorbée et m celle du solide. Ce rapport, relié au coefficient de distribution, dépend de la température et de la concentration c, et la courbe obtenue en portant x/m en fonction de c à température constante est une isotherme d'adsorption. Pour deux solutés de structures moléculaires différentes (polarités différentes) dissous dans la phase mobile, ces courbes ne coïncident pas et, si leur concentration est égale, le plus polaire des deux est plus fortement adsorbé par le solide (excepté le cas du carbone poreux pour lequel la séparation se fait principalement en fonction du volume hydrocarboné des solutés). En plaçant une phase mobile pure au contact d'un solide qui supporte des composés adsorbés, chacun de ceux-ci s'y dissoudra plus ou moins suivant son affinité relative pour la phase mobile et pour le solide jusqu'à ce que l'équilibre s'établisse entre les deux phases. Un processus de compétition d'interactions moléculaires entre chacun des solutés et la phase stationnaire s'établit. Un cycle d'adsorption-désorption constitue le processus élémentaire de la chromatographie par adsorption. Il se répète à mesure que le fluide mobile passe le long du solide. Historiquement, ce mode de chromatographie a été appelé à polarité normale de phases (sigle anglais : N.P.L.C.) Sur ce principe, dans le cas des chromatographies en phase liquide et à fluide subcritique et supercritique, des échelles de force éluante des différents solvants purs puis en mélange ont été établies. Elles tiennent compte de la polarité relative de chacun d'entre eux et mesurent en fait leur affinité vis-à-vis de chaque adsorbant utilisé. Ces échelles expérimentales sont employées pour choisir la nature et la composition de la phase mobile. Ainsi, si un mélange est trop retenu par un adsorbant donné dans une phase mobile de composition donnée, pour obtenir une séparation dans des conditions correctes il suffira de choisir une autre phase mobile telle que les interactions moléculaires qu'elle développe avec la phase stationnaire soient plus voisines de celles que développent les solutés avec la même phase stationnaire (on prendra une phase mobile de force éluante plus grande, en fait plus polaire vis-à-vis de l'adsorbant utilisé).
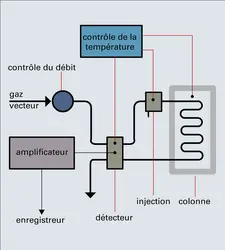
Dans le cas de la chromatographie en phase gazeuse, la seule possibilité sera d'augmenter la température d'analyse. Cette dernière technique est la mieux adaptée à l'analyse de composés gazeux ou très volatils. Les phases fixes adsorbantes sont relativement peu nombreuses ; leur choix sera fait principalement d'après leur porosité. On dispose par exemple, avec les tamis moléculaires (silicates poreux), de plusieurs qualités dont les pores ont des dimensions du même ordre que celles des molécules et permettent un tri suivant ces dimensions.
La chromatographie par adsorption a été perfectionnée en modifiant[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Robert ROSSET : docteur ès sciences, professeur à l'École supérieure de physique et de chimie industrielles, Paris, ingénieur, École supérieure de physique et de chimie industrielles
- Louis SAVIDAN : professeur de chimie organique à l'université d'Aix-Marseille-II
- Alain TCHAPLA : professeur des Universités, université de Paris-XI, I.U.T. d.Orsay
Classification
Médias
Autres références
-
ALCALOÏDES
- Écrit par Jacques E. POISSON
- 5 689 mots
- 5 médias
...successives en milieu acide à l'aide de solutions de pH décroissant, en pratiquant une séparation par contre-courant d'un solvant non miscible, et surtout par chromatographie. Les méthodes chromatographiques consistent à séparer les divers constituants d'un mélange en fonction de leur affinité pour un adsorbant... -
ANALYTIQUE CHIMIE
- Écrit par Alain BERTHOD et Jérôme RANDON
- 8 890 mots
- 4 médias
La chromatographie est une méthode de séparation des constituants d'un échantillon basée sur les différences d'affinités de ceux-ci pour chaque phase d'un système biphasique. La séparation s'effectue dans une colonne chromatographique à l'intérieur de laquelle est fixée une phase dite stationnaire.... -
BIOCHIMIE
- Écrit par Pierre KAMOUN
- 3 881 mots
- 5 médias
...cellulaires. Parmi ces méthodes, il faut indiquer l'électrophorèse, qui permet la séparation, dans un champ électrique, de molécules chargées, et la chromatographie. Cette dernière méthode, inventée en 1906 par le botaniste russe Mikhaïl Tswett, resta dans l'oubli jusqu'en 1931. Elle permet de séparer... -
CASSINI-HUYGENS (MISSION)
- Écrit par Athéna COUSTENIS
- 4 465 mots
- 9 médias
– un chromatographe et spectromètre de masse pour déterminer la composition atmosphérique (GCMS, Gas Chromatograph and Mass Spectrometer) ; - Afficher les 15 références
Voir aussi
- SPECTROCHIMIQUE ANALYSE
- IONS
- PLATEAU, génie chimique
- TRACES ANALYSE DE
- SOLUTÉ
- DIAGRAMME, thermodynamique
- POINT CRITIQUE
- NITRATE D'ARGENT
- ISOTHERME
- PARTAGE COEFFICIENT DE
- DOUBLE LIAISON ou LIAISON ÉTHYLÉNIQUE
- SÉPARATION, chimie
- CONCENTRATION, chimie
- ÉCHANGE CHIMIQUE
- DÉSORPTION
- ÉLECTRO-OSMOSE
- ÉLUTION
- COLONNE, génie chimique
- VOLATILITÉ
- GOPPELSRÖDER FRIEDRICH (1836-1919)
- MICROEXTRACTION EN PHASE SOLIDE (MEPS) ou SOLID-PHASE MICROEXTRACTION (SPME)
- CHROMATOGRAPHIE À CONTRE-COURANT
- CHROMATOGRAPHIE PLANAIRE
- CHROMATOGRAPHIE SUR COUCHE MINCE
- CHROMATOGRAPHIE SUR PAPIER
- CHROMATOGRAPHIE PAR ÉCHANGE DE LIGANDS
- CHROMATOGRAPHIE DE PARTAGE À POLARITÉ DE PHASES INVERSÉE
- CHROMATOGRAPHIE D'ÉCHANGE D'IONS
- CHROMATOGRAPHIE D'EXCLUSION ou CHROMATOGRAPHIE DE FILTRATION SUR GEL
- CHROMATOGRAPHIE D'AFFINITÉ
- FRACTIONNEMENT PAR COUPLAGE FLUX-FORCE
- FLUIDES SUPERCRITIQUES
- ÉLECTROPHORÈSE CAPILLAIRE DE ZONE
- ÉLECTROCHROMATOGRAPHIE CAPILLAIRE
- CHROMATOGRAPHIE PAR ADSORPTION
- ÉNANTIOMÈRES ou INVERSES OPTIQUES ou ANTIPODES OPTIQUES
- CHIMIE HISTOIRE DE LA
- SOLUTION, chimie
- HYDROPHOBICITÉ, chimie
- PHASES, physico-chimie
- SÉLECTIVITÉ, chimie
- CHROMATOGRAPHIE EN PHASE GAZEUSE
- CHROMATOGRAPHIE EN PHASE LIQUIDE
- CHROMATOGRAPHIE EN PHASE SUPERCRITIQUE
- POREUX MILIEU
- CARBONIQUE GAZ ou DIOXYDE DE CARBONE
- CHIMIE PHYSIQUE ou PHYSICO-CHIMIE