COMBUSTION
Article modifié le
La combustion recouvre des phénomènes très variés. La définition même du terme répond à deux tendances différentes. La première lui donne un sens très général. Elle englobe « combustion vive » et « combustion lente ». La combustion de l'air dans les poumons, celle de l'hydrogène dans une pile à combustibles et un grand nombre de réactions chimiques et biochimiques mettant en jeu l'oxygène sont considérées comme des combustions lentes. Un autre terme est employé depuis longtemps pour caractériser ces dernières réactions : il s'agit du mot « oxydation ». Sa signification a été d'ailleurs considérablement précisée depuis que les chimistes ont montré qu'il n'y a pas que l'oxygène qui soit capable de réaliser l'oxydation d'un corps. Finalement, on est arrivé à une définition à la fois très générale et très fondamentale : oxyder un corps, c'est lui prendre des électrons. Cette définition s'applique à toutes les oxydations et à toutes les combustions lentes.
La seconde tendance réserve le mot « combustion » uniquement aux seules combustions vives qui s'effectuent par l'intermédiaire d'une flamme. Il existe essentiellement deux types de flammes ou combustion : ce sont la déflagration et la détonation ; mais il est possible, avec certaines réserves, d'en considérer un troisième, l'explosion.
Combustibles et comburants
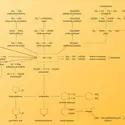
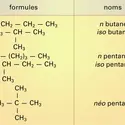
Les combustibles sont nombreux et bien connus : ce sont pratiquement tous les composés hydrocarbonés de la chimie organique. Une place spéciale doit être faite aux hydrocarbures, depuis le méthane (gaz naturel) jusqu'aux paraffines solides. La plupart des produits organiques naturels, tels le bois, les graisses, etc., sont aussi des combustibles. Tous ces corps sont essentiellement des porteurs d'hydrogène et la combustion de leur carbone ne doit être considérée qu'en second lieu au point de vue énergétique. On connaît d'ailleurs d'autres porteurs d'hydrogène susceptibles de brûler : l'ammoniac, les hydrures de bore, de nombreux hydrures métalliques, etc. Une autre catégorie de combustibles est constituée par les éléments à l'état non combiné, notamment le carbone et sa forme commune, le charbon. La combustion de l'hydrogène tend à prendre une grande importance dans la propulsion des fusées. La combustion du soufre permet de préparer l'anhydride sulfureux et tous les produits qui en découlent. La plupart des métaux brûlent quand ils se trouvent dans un état suffisamment divisé. Cette propriété est utilisée pour la propulsion de certaines fusées où l'on mélange différentes poudres métalliques aux propergols pour renforcer leur caractère énergétique.
Les comburants constituent une catégorie beaucoup plus restreinte de composés, mais leur nombre s'accroît régulièrement. À côté de l'oxygène, on trouve, à l'état élémentaire ou combiné, d'autres atomes électronégatifs : les halogènes (fluor, chlore, brome, iode), l'ozone, des acides très oxygénés (acides nitrique et perchlorique), les perchlorates, l'oxyde de fluor, enfin d'autres composés oxygénés plus inattendus tels que l'anhydride carbonique et la vapeur d'eau. Certains métaux comme le magnésium brûlent en effet dans la vapeur d'eau ou l'anhydride carbonique et ce mode de production d'énergie peut être envisagé sur les planètes dont l'atmosphère est riche en anhydride carbonique.
La proportion du combustible et du comburant joue un rôle considérable dans la combustion. Le mélange stœchiométrique est celui qui correspond à la combustion complète. Dans celle du méthane, par exemple,
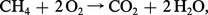
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Michel LUCQUIN : ingénieur diplômé de l'École nationale supérieure de chimie de Paris, professeur à l'université des sciences et techniques de Lille
Classification
Médias
Autres références
-
ACÉTYLÈNE
- Écrit par Henri GUÉRIN
- 5 094 mots
- 6 médias
...endothermique (ΔH = 226,5 kJ/mole) est instable ; cela explique la facilité avec laquelle il donne lieu à des réactions de synthèse et sa grande chaleur de combustion (58 000 kJ/m3) :et aussi les risques d'explosions, dès qu'il est en présence d'air ou même en l'absence de celui-ci, lorsqu'on le comprime....
-
ALCANES
- Écrit par Jacques METZGER
- 3 616 mots
- 11 médias
La combustion des alcanes à l'air est une réaction fortement exothermique (réaction 4) qui est abondamment exploitée pour la production de chaleur (chauffage industriel et domestique) et d'énergie mécanique (moteurs à combustion interne, réacteurs). La chaleur de combustion des alcanes à ... -
AUTOMOBILE - Technologie
- Écrit par Georges BRESSON , Jean-Pierre CAPET , François de CHARENTENAY , Encyclopædia Universalis , Thierry HALCONRUY , Frédéric RIVAS et Jean-Pierre VÉROLLET
- 15 882 mots
- 27 médias
Le succès de l'automobile a été assuré, et le demeure pour quelques décennies encore, par l'efficacité dumoteur thermique dit à combustion interne (cycle 4 temps) qui équipe plus de 98 p. 100 des voitures. Ce type de moteur transforme l'énergie chimique des carburants en énergie... -
BALISTIQUE
- Écrit par Jean GARNIER
- 2 102 mots
- 2 médias
...ou le mélange des trois. Cependant, en raison des difficultés de stockage, les propergols les plus employés sont solides ou liquides. Le contrôle de la combustion des propergols liquides s'effectue au moyen de mécanismes auxiliaires qui règlent la quantité de carburant admise dans la chambre de combustion.... - Afficher les 26 références
Voir aussi
- STŒCHIOMÉTRIE
- ONDE DE CHOC
- PRESSION, physique
- LIQUIDE ÉTAT
- ÉMISSION, physique
- CALORIFIQUE POUVOIR
- COMBUSTIBLES
- COMBURANTS
- VAPORISATION
- PLASMAS
- CALORIMÈTRE, thermique
- EXPLOSION
- GAZÉIFICATION
- INFLAMMATION, technologie
- OXYDATION
- DÉFLAGRATION
- DÉTONATION
- EXOTHERMIQUE RÉACTION
- EXTINCTEURS
- TEMPÉRATURE
- SOLIDES PHYSIQUE DES
- HYDROGÈNE CHALUMEAU À
- FLAMME
- BUNSEN BEC
- JUNKERS CALORIMÈTRE DE
- POUSSIÈRES
- CHALUMEAUX
- COUP DE POUSSIÈRES