COMPLEXES, chimie
Article modifié le
Principaux domaines d'application
L'intérêt suscité par la chimie des complexes provient de la diversité de leurs très nombreuses applications qui ne cessent de se développer dans tous les domaines de la chimie, débordant même sur la physique, la métallurgie, la chimie bio-inorganique.
L' importance industrielle réside tout d'abord dans la catalyse homogène où l'utilisation de catalyseurs organométalliques (composés à liaison(s) métal-carbone) ou de sels ou de complexes solubles de métaux de transition offre les avantages d'une plus grande efficacité, d'une bonne sélectivité et de conditions de réactions plus douces qu'en catalyse hétérogène. De plus, les mécanismes réactionnels peuvent être analysés (et donc améliorés) au moyen des techniques spectroscopiques et cinétiques modernes. Plus de vingt procédés industriels utilisent des complexes métalliques solubles comme catalyseurs dans des réactions d'hydrogénation et d'oxydation des hydrocarbures, de polymérisation des oléfines, de synthèses d'acides, d'aldéhydes et d'alcools (cf. catalyse Catalyse homogène).
De nombreux complexes utilisés comme précurseurs conduisent, après pyrolyse dans des atmosphères gazeuses appropriées, à l'obtention de phases solides (oxydes, sulfures, nitrures, carbures, etc.) finement divisées.
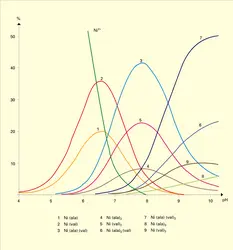
La chimie analytique met à profit l'insolubilité de certains complexes pour des dosages gravimétriques, leur coloration spécifique pour la détection ou le dosage absorptiométrique des ions métalliques, mais, surtout, elle dispose d'un très grand nombre de méthodes complexométriques pour doser et séparer les ions. Pour une utilisation rationnelle des complexes en chimie analytique, il importe alors de connaître non seulement les constantes de stabilité ionique définies ci-dessus, mais aussi les constantes « conditionnelles » tenant compte de l'influence de l'acidité de la solution, mais aussi des ions métalliques ou des coordinats parasites... (A. Ringbom, 1967).
Les agents complexants sont largement utilisés dans les opérations relatives à la chimie minérale. La détermination de la dureté de l' eau aussi bien que son adoucissement s'effectuent classiquement au moyen de séquestrants organiques ou minéraux, comme dans le cas du tripolyphosphate de sodium Na5P3O10. Des coordinats polymères sont utilisés pour éliminer les cations métalliques des eaux résiduaires par coagulation-floculation. En outre, les séparations très délicates des éléments du groupe des lanthanides et du groupe des actinides n'ont pu être réalisées commodément que selon deux techniques utilisées soit séparément, soit conjointement :
– le fractionnement sur échangeurs d'ions faisant appel aux séquestrants organiques comme agent d'élution ;
– l' extraction méthodique liquide-liquide fondée sur la formation de complexes solubles en milieu organique ; c'est ainsi que sont séparés industriellement les métaux des terres rares au moyen d'agents extractants à propriétés complexantes, chélatantes ou solvatantes tels que le tri(n-butyl)phosphate (TBP) ; le retraitement des combustibles nucléaires utilise aussi ces techniques.
La métallurgie emploie des complexes dans certaines opérations d'enrichissement de minerais (flottation) ou de séparation [procédé Mond de purification du nickel par formation de Ni(CO)4].
Les plus anciens teinturiers, faisant appel aux laques d'alizarine telles que le fameux rouge turc, ignoraient certes la nature de ces composés chélates mais en connaissaient bien la solidité. La chimie tinctoriale, devant satisfaire les exigences sans cesse croissantes imposées à ses colorants (variété, éclat, stabilité), développa les colorants à complexe métallique (ou métallifères) utilisés dans les opérations de métallisation.[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- René-Antoine PARIS : Professeur honoraire à l'Université Claude Bernard de Lyon-I
- Jean-Pierre SCHARFF : docteur ès sciences physiques, professeur des Universités
Classification
Médias
Autres références
-
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 367 mots
- 7 médias
Considérons les complexes d'un ion métallique M2+ accepteur, avec un donneur X— (ions Cl—, SCN—, par exemple).
-
ANALYTIQUE CHIMIE
- Écrit par Alain BERTHOD et Jérôme RANDON
- 8 890 mots
- 4 médias
...plusieurs doublets électroniques capables de former une ou plusieurs liaisons covalentes avec l'ion. Le produit formé (composé de coordination) est appelé complexe. Par exemple, la glycine est un acide aminé capable de former un complexe avec l'ion cuivre Cu2+, le glycinate de cuivre Cu(NH2CH2COO)... -
ARGENT, métal
- Écrit par Robert COLLONGUES
- 5 167 mots
- 6 médias
-
BORE
- Écrit par Jean CUEILLERON
- 5 305 mots
- 6 médias
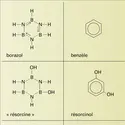
Avec les corps polyhydroxylés (glycérine, acides-alcools, acides-phénols...) l'acide borique donne de nombreuxcomplexes. En particulier, la glycérine et surtout le mannitol conduisent à la formation de complexes d'addition qui sont des acides beaucoup plus forts que l'acide borique pur ; avec cet... - Afficher les 27 références
Voir aussi
- IONS
- HYDROLYSE
- COORDINENCE ou NOMBRE DE COORDINATION
- COMPLEXOMÉTRIE
- COORDINATION LIAISON DE
- CATALYSE HOMOGÈNE
- MINÉRALE CHIMIE
- IONS MÉTALLIQUES
- COMPLEXES POLYNUCLÉAIRES
- ÉQUILIBRE, chimie
- CATALYSEURS
- TEINTURE
- CYCLIQUES COMPOSÉS
- ANIONS
- CATIONS
- ACTINIDES
- HUMIQUES ACIDES
- FULVIQUES ACIDES
- DOSAGE, chimie
- PI ORBITALE
- LIGAND ou COORDINAT, chimie
- CHÉLATES
- EXTRACTION, chimie
- POLYCHÉLATES
- SÉPARATION, chimie
- CLUSTER
- CHÉLATION
- TRANSITION MÉTAUX DE
- STABILITÉ, chimie
- EDTA (acide éthylène-diamine-tétracétique)
- CRYPTATES
- TERRES RARES
- CONSTANTE D'ÉQUILIBRE, chimie
- EAU APPROVISIONNEMENT ET TRAITEMENT DE L'
- DONNEUR, chimie
- ACCEPTEUR, chimie
- ÉTHER-COURONNE
- MACROCYCLIQUES COMPOSÉS
- COORDINATION COMPOSÉS DE