CONTRÔLE CENTRAL DE L'APPÉTIT
Article modifié le
Signaux circulant régulateurs de la satiété
On peut considérer que les mécanismes de contrôle de la prise alimentaire décrits jusqu’à ce point sont locaux et concernent l’axe cerveau-intestin. Cependant, ce contrôle s’exerce dans le cadre plus vaste de la physiologie générale d’un organisme, celui du contrôle hormonal et celui de la perception des propriétés des macronutriments (sensorialité buccale et viscérale).
Quelques acteurs de type hormonal
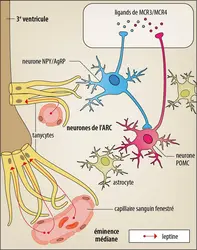
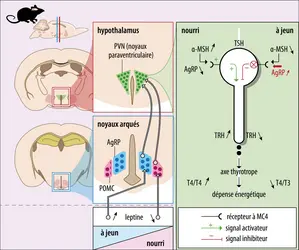
Certains signaux de cette intégration dans la physiologie générale sont de type hormonal. La théorie « lipostatique » propose qu’un signal circulant émanant du tissu adipeux peut directement contrôler le « point de consigne métabolique » et participer à l’orchestration de la balance entre apports et dépenses d’énergie. En effet, le tissu adipeux en sa qualité de tissu de stockage offre un très bon reflet de l’énergie disponible. Dans les années 1990, en recherchant les causes génétiques de l’obésité des souris porteuses de la mutation ob (pour obesity) – les homozygotes ob/ob peuvent peser deux fois le poids d’une souris normale –, on a identifié le gène codant pour une hormone, la leptine, produite par le tissu adipeux en proportion de sa masse. La mutation ou la dysfonction du gène ob se traduisent chez l’homme comme chez l’animal par une obésité massive avec augmentation de la taille des adipocytes associée à une hyperphagie et une baisse du métabolisme. D’un point de vue physiologique, le développement du tissu adipeux se traduit par une production et une libération croissante de leptine par ce dernier. La leptine est en cela une « adipokine » (hormone sécrétée par le tissu adipeux) dont les effets majeurs sont de réduire l’alimentation (effet satiétogène ou anorexigène) et de promouvoir une augmentation de la dépense énergétique. Elle a donc un effet de rétrocontrôle sur la prise alimentaire. L’absence de leptine a les effets inverses. Pour agir, la leptine doit atteindre des cibles neuronales spécifiques dans l’hypothalamus. Là, elle inhibe les neurones NPY/AgRP et active les neurones POMC et la libération de MSH qui va, via MCR4, réduire la prise alimentaire et augmenter la dépense énergétique ; ce qui, en retour, va initier une cascade d’événements synaptiques aboutissant à ces réponses adaptatives. En outre, la leptine a un effet majeur sur le métabolisme glucidique et le fonctionnement de la voie insulinique, ce qui contribue également aux réponses adaptatives.
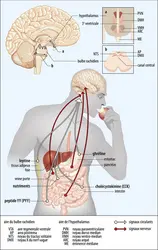
Précisément, une autre hormone comme l’insuline, produite par le pancréas, a aussi la capacité à entrer dans le cerveau et à agir comme facteur diminuant l’appétit. Il en va de même de plusieurs autres facteurs circulants dont la découverte fait l’objet de recherche active dans le domaine. Parmi eux, la ghréline offre une image « en miroir » de la leptine, en cela que cette hormone est considérée comme une hormone orexigène (susceptible de stimuler la faim). La ghréline est une hormone peptidique sécrétée principalement par l’estomac endocrine. Les teneurs plasmatiques de ghréline sont à leur maximum avant un repas pour diminuer progressivement après la prise alimentaire. La ghréline agit sur le récepteur à l’hormone de croissance (GHS-R), qui active sa sécrétion. L’injection de ghréline augmente les sécrétions acides et la motilité gastrique, la sensation de faim et la prise alimentaire. La leptine, la ghréline et l’insuline ont de multiples territoires d’action au niveau du cerveau, mais chacune de ces hormones a la capacité de moduler directement les neurones NPY/AgRP et POMC.
Les macronutriments et leurs effets directs sur le contrôle de l’appétit
L’alimentation consiste en trois macronutriments, les lipides, les protéines et les glucides, auxquels des goûts sont associés. Du début à la fin de la digestion, l’organisme est informé des propriétés des macronutriments ingérés.
Dans la sphère oropharyngée, des cellules très spécialisées appelées bourgeons du goût expriment une variété de récepteurs activables par les divers macronutriments. Leur activation est la première phase du goût, donc des perceptions et comportements qui en découlent. L’activation de ces récepteurs spécialisés et la transformation du signal chimique en signal électrique sont initiées par les cellules des bourgeons du goût. Ce dernier signal électrique sera transporté vers le cerveau via les nerfs crâniens VII et IX. Ce signal code notamment les différents goûts – sucré, salé, acide, amer, umami et gras. Le « goût du gras » correspond à une inscription récente dans ce répertoire (2015) ; il est dû à une famille de récepteurs dont chacun dispose d’une affinité particulière pour des lipides dont la nature, diverse, est déterminée par la longueur de leur chaîne carbonée.
En phase digestive, les nutriments glucose, protéines et lipides sont tout d’abord détectés au niveau de récepteurs et cellules spécialisés de l’intestin (cellules entéro-endocrines) qui renseignent le cerveau sur la qualité des nutriments absorbés via notamment les afférences nerveuses reliant l’intestin au cerveau. Ainsi, les protéines partiellement digérées vont produire de petits peptides et des acides aminés dont la signalisation par des récepteurs dédiés va avoir des effets majoritairement satiétogènes, via l’activation de la production d’hormones de type CCK et GLP-1 et par l’activation du nerf vague. Pour le glucose, l’activation des cellules entéro-endocrines est à la fois médiée par le transport et le métabolisme du glucose au niveau intracellulaire, mais aussi par l’activation directe de récepteurs qui répondent au glucose. Les cellules entéro-endocrines sont aussi équipées de récepteurs activés par les acides gras libres (à chaîne courte ou longue) ainsi que les mono-, di- et triglycérides (la forme de stockage des lipides). Là encore, le transport et le métabolisme des lipides ainsi que leur capacité à se lier à des récepteurs sur les cellules entéro-endocrines sont autant de phénomènes qui vont contribuer à relayer au niveau du cerveau la nature et la quantité des lipides présents dans la lumière de l’intestin. La détection de sucres et des lipides au niveau de l’intestin emprunte des voies nerveuses différentes. Les lipides activent le nerf vague tandis que les sucres engagent plutôt les nerfs spinaux (ou rachidiens) et le signal envoyé se traduit par une inhibition rapide des neurones NPY/AgRP de l’hypothalamus avec des conséquences satiétogènes. La détection des lipides dans l’axe intestin-cerveau est aussi capable de modifier l’appétit, mais dans sa composante hédonique en exerçant un contrôle sur la quantité de dopamine dans la sphère dite de la récompense, via le nerf vague.
Dans la phase postabsorptive, lorsque les macronutriments s’accumulent au niveau plasmatique, ils sont aussi capables d’avoir une action directe sur l’activité de populations nerveuses impliquées dans la régulation de l’appétit. Le déficit d’un acide aminé en particulier – comme ceux qui sont dits essentiels car non produits par l’organisme – est identifié par des neurones, notamment du cortex piriforme antérieur, dans le bulbe olfactif, et module en retour la prise alimentaire en fonction des teneurs des repas afin de combler les manques en ces acides aminés. Les sucres (le glucose) sont détectés directement au niveau central par des neurones hypothalamiques (parmi lesquels les neurones à POMC et à NPY/AgRP) qui répondent de manière positive ou négative aux variations de glucose et modulent en retour l’appétit. Les acides gras vont avoir des effets centraux différents selon leur nature – libres ou bien estérifiés sous forme de triglycérides. Les acides gras libres inhibent les neurones à NPY/AgRP et activent les neurones à POMC selon des mécanismes qui, là encore, peuvent engager une signalisation couplée à des récepteurs membranaires, ou bien des signaux issus du métabolisme des lipides au niveau des neurones ou des cellules gliales avoisinantes.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Serge LUQUET : directeur de recherche CNRS, université Paris Cité
Classification
Médias
Voir aussi
- ANOREXIE
- POLYPEPTIDES
- NERF PNEUMOGASTRIQUE ou NERF VAGUE
- INTESTIN
- DOPAMINE
- PROTÉINES ALIMENTAIRES
- GOÛT, physiologie
- PHYSIOLOGIE
- NEUROPEPTIDE Y
- GRAS ACIDES
- NEUROPHYSIOLOGIE
- CHOLÉCYSTOKININE
- APPÉTIT
- RÉGULATION BIOLOGIQUE
- RÉCEPTEUR, physiologie
- PEPTIDE YY
- SATIÉTÉ, physiologie
- NEURONE ou CELLULE NERVEUSE
- GLUCOSE
- INSULINE
- GLUCONÉOGENÈSE ou NÉOGLUCOGENÈSE
- MÉTABOLISME ÉNERGÉTIQUE
- NEUROBIOLOGIE
- NEUROMÉDIATEURS ou NEUROTRANSMETTEURS
- SIGNAL, biologie
- BARRIÈRE HÉMATO-ENCÉPHALIQUE
- ALIMENTS
- ALIMENTAIRE COMPORTEMENT
- NUTRITION HUMAINE
- NEUROPEPTIDES
- STIMULUS, neurosciences
- PRISE ALIMENTAIRE
- GRAISSES