CYCLANES & CYCLÈNES
Préparations et utilisations
Les méthodes de préparation directe des cyclanes, par fermeture d'une chaîne carbonée porteuse de fonctions appropriées, sont peu nombreuses ; la seule importante est l'action de certains métaux, comme le zinc, sur les α,ω-dihaloalcanes :

Mais le rendement en cyclane, donc l'intérêt de la réaction, dépend beaucoup de la taille du cycle cherché : excellent pour le cyclopropane, convenable pour le cyclopentane et le cyclohexane, mais très faible pour le cyclobutane et pour les cyclanes au-dessus du cycloheptane ; il décroît très vite si le ou les atomes de carbone porteurs de l'halogène sont substitués.
Aussi les cyclanes, mis à part les cyclo propanes et les cyclobutanes, sont-ils préparés le plus souvent à partir de composés déjà cycliques et d'accès facile, porteurs de fonctions ou de centres insaturés appropriés. Ainsi, l' hydrogénation catalytique du benzène et du cyclopentadiène conduit respectivement au cyclohexane et au cyclopentane. La réduction du carbonyle des cyclanones en groupement − CH2 − (réaction de Wolff-Kishner) permet de préparer les cyclanes en général.
Quant à la préparation des cyclènes, elle met en jeu le plus souvent une réaction d'élimination telle que la déshydratation des cyclanols, la débromhydratation des bromures de cyclo-alcoyle, etc.
Mention particulière doit être faite des réactions de cyclo-addition, au cours desquelles deux molécules insaturées se combinent pour former un composé cyclique unique. On connaît depuis longtemps la réaction de Diels et Alder qui est une cyclo-addition-1,4, à savoir la formation d'un cycle par soudure de l'un et l'autre des carbones d'une double liaison activée aux deux carbones extrêmes d'un diène conjugué, constituant une excellente méthode de préparation des cyclohexènes. De nombreuses réactions de même type ont été découvertes : cyclo-addition-1,2 dans laquelle les carbones de la double liaison activée se soudent à ceux d'une autre double liaison ; cyclo-addition-1,1 où ces deux carbones se soudent à celui d'un carbène.
On connaît de très nombreuses synthèses de cyclopropanes et de cyclopropènes, de cyclobutanes et de cyclobutènes, mettant en jeu des cyclo-additions-1,2 et -1,1 et utilisant des facteurs tels que le chauffage, l'irradiation ultraviolette, etc.
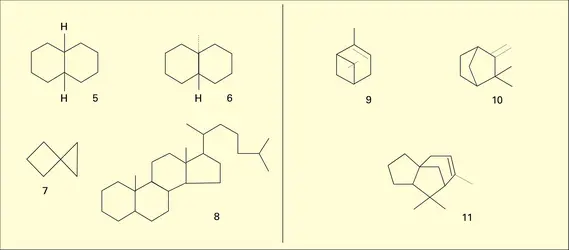
L'intérêt pratique des cyclanes est faible ; le plus souvent, il repose seulement sur leur inertie chimique, et le cyclohexane, par exemple, est utilisé comme solvant ; le cyclopropane est employé comme anesthésique général. Quant aux cyclènes, s'ils interviennent souvent dans la synthèse organique, ils sont assez peu utilisés en tant que tels, sauf certains de ceux qui existent dans les substances naturelles, tel le pinène, principal constituant de l'essence de térébenthine et d'autres terpènes.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean-Marie CONIA : Professeur à la faculté des sciences de Caen
Classification
Médias
Autres références
-
CONFORMATIONS, chimie
- Écrit par Jacques GORÉ
- 3 324 mots
- 5 médias
Du fait de leur plus grand nombre de carbones, ces cyclanes sont plus flexibles que le cyclohexane et, généralement, le nombre de conformations stables est supérieur à deux. Pour le cycloheptane, il existe à côté des formes chaise et bateau, voisines de celles du cyclohexane, une forme croisée... -
CYCLOPENTADIÈNE
- Écrit par Dina SURDIN
- 327 mots
Cyclène de formule :
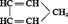
Masse moléculaire : 66,10 g
Masse spécifique : 0,8047 g/cm3
Point de fusion : —85 0C
Point d'ébullition : 42 0C
Liquide incolore.
Insoluble dans l'eau ; soluble dans le sulfure de carbone, l'aniline, l'acide acétique. Miscible à l'éthanol, à l'éther, au benzène et...
-
HYDROCARBURES
- Écrit par Pierre LASZLO
- 4 523 mots
- 4 médias
Les hydrocarbures cycliques, à commencer par les cyclanes ou cycloalcanes, ont des tensions de cycle, dénommées tension de Baeyer, du nom du chimiste allemand Adolf von Baeyer (1835-1917) qui le premier les signala. Le cyclopropane C3H6 en est un exemple (fig. 1). Le cycle y a la forme d'un triangle... -
PÉTROLE - Le pétrole brut
- Écrit par Bernard TISSOT
- 3 439 mots
- 6 médias
Les cyclanes sont en quantité assez variable : parmi eux les molécules tétracycliques et pentacycliques sont responsables de l'activité optique des hydrocarbures saturés (stéranes, triterpanes ; ).