CYCLES BIOGÉOCHIMIQUES
L'azote
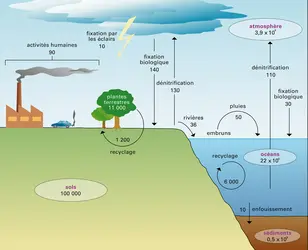
L'azote (N) a un cycle complexe parce qu'il existe sous forme de composés solides, gazeux ou dissous dans des liquides. Dans la matière vivante, il est étroitement couplé aux autres éléments, au point que, dans l'océan, leur rapport est quasi constant. Beaucoup de composés azotés ont un intérêt économique et le cycle naturel de l'azote est lui aussi perturbé par les activités humaines.
Différentes formes chimiques
L'azote, pouvant prendre des degrés d'oxydation variant de + 5 à – 3, apparaît sous des formes très variées :
– L' acide nitrique, HNO3, résulte de l'oxydation naturelle des oxydes d'azote. Il est produit industriellement, car les nitrates servent à fabriquer des engrais et des explosifs.
– Le peroxyde d'azote, NO2, gaz toxique irritant, déchet de l'industrie chimique, est produit dans l'atmosphère par oxydation de NO.
– L'oxyde nitrique, NO, est un sous-produit de toutes les combustions. Il est surtout abondant en zone urbaine, où le mélange NO-NO2 est responsable de brumes photochimiques et de nombreuses réactions avec les composés minoritaires de l'atmosphère (oxyde de carbone, ozone, radicaux divers).
– L'oxyde nitreux, N2O, peu réactif, a une longue durée de vie (120 ans). Il peut être transporté jusque dans la stratosphère, où il intervient dans les réactions contrôlant l'ozone.
– L'azote (N2), gaz incolore, inerte, constitue 78 p. 100 de l'atmosphère.
– L'ammoniac, NH3, est un produit d'excrétion des animaux ; ses sels servent d'engrais.
– Des composés organiques – amines (dérivés organiques de l'ammoniac), amides comme l'urée, ou protéines – constituent une grande partie du matériel cellulaire. Les composés azotés sont donc présents dans les produits d'excrétion ou de décomposition des matières organiques.
Les transformations biologiques
Les réactions biologiques contribuent au transfert d'azote entre les différents réservoirs (atmosphère, eaux continentales et marines, biosphère, lithosphère). Les flux les plus intenses sont associés aux échanges de la biosphère avec les sols et l'eau.
La fixation biologique est la source unique d'azote pour les plantes en l'absence d'engrais. Celle-ci est réalisée par des algues en milieu aquatique et par des bactéries dans les systèmes terrestres (par exemple, celles des racines des légumineuses utilisées dans l'agriculture traditionnelle pour enrichir les sols). Les micro-organismes sont susceptibles de nombreuses réactions permettant de transformer l'azote en composés assimilables par les êtres vivants : fabrication de composés ammoniaqués, nitrification, qui permet de passer de l'ammoniac aux nitrates assimilables par les plantes pour être transformés en matière organique, dénitrification, réduisant les nitrates en azote ou en oxyde nitreux.
Beaucoup d'organismes sont capables d'assimiler directement les produits de décomposition des matières organiques. Cependant, une fraction des composés gazeux produits aux divers stades du cycle biologique de l'azote (NH3, NO, NO2, N2O) est susceptible de passer dans l'atmosphère, où ils subissent de nouvelles réactions chimiques.
Les réactions chimiques abiotiques
Les oxydes d'azote sont très réactifs dans l'air et, bien que peu abondants, jouent un rôle majeur sur la chimie de l'atmosphère et notamment celle de l'ozone.
Les pluies éliminent une grande fraction des composés azotés qui peuvent se dissoudre dans les gouttes d'eau sous forme d'ions ammonium ou de nitrate. L'ammoniac est très rapidement recyclé sous le couvert végétal au voisinage du sol, de sorte que sa concentration diminue rapidement avec l'altitude. Celui qui s'échappe est soumis à l'oxydation photochimique par les radicaux OH, ce[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean-Claude DUPLESSY : directeur de recherche au C.N.R.S., Centre des faibles radioactivités, Gif-sur-Yvette
Classification
Médias
Autres références
-
BACTÉRIES
- Écrit par Jean-Michel ALONSO , Jacques BEJOT et Patrick FORTERRE
- 11 055 mots
- 3 médias
Tous les éléments constitutifs de la matière vivante subissent une transformation cyclique, passant sans cesse de l'état minéral à l'état organique et vice versa. Grâce à l'énergie solaire, les plantes vertes, par assimilation chlorophyllienne, procèdent à « l'organisation » de la matière, autrement... -
BIOSPHÈRE
- Écrit par Paul DUVIGNEAUD , Maxime LAMOTTE et François RAMADE
- 3 432 mots
- 5 médias
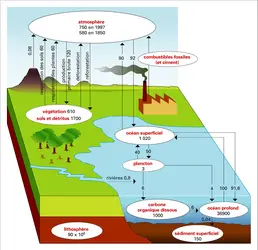
...oxygène, hydrogène – peuvent être suivis et dosés dans le milieu ambiant, en dehors des organismes vivants. Ainsi peuvent être définis ce que l'on appelle des cycles biogéochimiques et par là précisées, à la fois qualitativement et quantitativement, les modalités du fonctionnement de la biosphère comme celles... -
ENVIRONNEMENT - Un enjeu planétaire
- Écrit par Jean-Paul DELÉAGE
- 2 014 mots
- 1 média
...terrestre, désastre que les biologistes désignent comme « la sixième extinction en masse » depuis l'apparition de la vie sur Terre. Elle bouleverse ainsi les cycles biogéochimiques avec l'entrée dans l'ère de l'« Anthropocène ». Paul J. Crutzen et Eugene F. Stoermer ont ainsi désigné (2000) l'époque géologique... -
MILIEU, écologie
- Écrit par Cesare F. SACCHI
- 7 832 mots
- 1 média
...indispensables à la vie des végétaux autotrophes, puis à celle des animaux puisqu'ils sont la source des éléments biogènes fondamentaux, phosphore et azote. Le cycle biogéochimique de l'azote est complexe, entraînant des réactions multiples d'oxydation et de réduction, car il fait partie des protides à l'état... - Afficher les 7 références