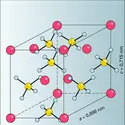
EPSOMITE
Article modifié le
Se présentant généralement en croûtes, en efflorescences ou en groupements de fines aiguilles, ce sulfate de magnésium hydraté cristallise dans le système orthorhombique. Les cristaux peuvent paraître tétragonaux de par la présence d'un angle voisin de 900 entre les faces du prisme. La cassure est conchoïdale. L'epsomite, comme d'autres minéraux solubles avides d'eau, peut être caractérisée par sa saveur : elle présente un goût amer, ce qui lui a valu son appellation de sel amer ou sel anglais, alors qu'elle était utilisée en médecine comme purgatif. Transparente à translucide, avec un éclat vitreux (soyeux pour les variétés en aiguilles), l'epsomite voit sa coloration varier avec les traces qu'elle admet : ainsi, incolore à blanche, elle peut être rosée par le cobalt, ou verdâtre par le nickel. Toutefois sa poussière reste incolore. D'une dureté proche de celle de l'ongle (2 à 2,5), c'est un minéral peu dense (1,68).
La caractérisation par voie humide de l'epsomite, MgSO4, 7 H2O, est aisée puisque sa solubilité et sa saveur lui sont propres. Outre le nickel et le cobalt, le zinc et le manganèse peuvent entrer dans sa composition chimique. De plus, des phénomènes de substitution en toutes proportions entre zinc, nickel et magnésium conduisent à une série de minéraux secondaires, où nous pouvons citer la goslarite, pôle zincifère, et la morénosite, pôle nickélifère.
L'epsomite, minéral de dépôts marins par évaporation, se forme par altération de la kiesérite MgSO4, H2O ou à partir de l'anhydrite. Son habitat le plus courant est celui des gisements de sels potassiques (cas des sels de Sibérie ou de Californie). Ce minéral résulte aussi parfois de l'altération de roches magnésiennes.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Yannick LOZAC'H : étudiant en troisième cycle de géologie
Classification
Autres références
-
SULFATES NATURELS
- Écrit par André JAUZEIN
- 2 023 mots
- 5 médias
Les deux principaux sulfates de magnésium sontl'epsomite MgSO4 . 7 H2O, forme de basse température, de symétrie rhomboédrique (groupe P212121) et la kiésérite MgSO4.H2O, forme de haute température monoclinique (C2/c). Ces deux sulfates sont communs dans les séquences lacustres ou...
Voir aussi