ACÉTYLACÉTIQUE ESTER
Article modifié le
Tautomérie de l'acétylacétate d'éthyle
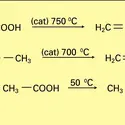
L'ester acétylacétique est un liquide incolore, d'odeur agréable, assez soluble dans l'eau. Il se présente, à l'état pur et dans les conditions normales de température et pression, comme un mélange en équilibre de deux formes tautomères (réaction 4) renfermant 92 p. 100 de forme cétonique (I) et 8 p. 100 de forme énolique chélatée (II). Ce mélange est appelé allélotrope. La vitesse d'équilibration dépend de la température mais surtout de la présence de catalyseurs. Une trace d'acide ou de base accélère la transformation réversible des deux formes (réactions 5).
En présence d'une trace d'acide, le catalyseur est l'acide conjugué (III) de la forme cétonique (réaction 5a) ; en présence d'une base, c'est l'anion énolate (IV) formé par arrachement du proton méthylénique acide (réaction 5b). En l'absence rigoureuse de catalyseur, la vitesse d'équilibration est relativement lente et l'on peut, par refroidissement brutal à − 78 0C d'une solution dans l'éther, obtenir la forme cétonique (I) cristallisée. La forme énolique peut être obtenue soit par distillation, sous pression très réduite dans une verrerie en silice (absence de l'alcalinité du verre), car elle est la plus volatile (chélation), soit par addition d'acide chlorhydrique gazeux et sec à une suspension, dans l'éther méthylique, du sel de sodium de l'ester : l'énolate (IV), anion ambident, se protone (acide dur) préférentiellement sur l'oxygène (base dure) plutôt que sur le carbone (base molle). Les solvants protiques favorisent la forme cétonique (99,5 p. 100 dans l'eau, 90 p. 100 dans l'éthanol) solvatable spécifiquement au niveau des fonctions carbonylées, tandis que, dans les solvants aprotiques, la forme énolique (interaction spécifique intramoléculaire) est un peu plus abondante (32 p. 100 dans le disulfure de carbone, 48 p. 100 dans l'hexane).
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Médias
Autres références
-
ACÉTIQUE ACIDE
- Écrit par Jacques METZGER
- 2 113 mots
- 3 médias
Ce dernier est un composé dicarbonylé très utile pour certaines synthèses organiques en raison de la facilité avec laquelle, comme les composés organomagnésiens, il fournit des carbanions sur lesquels peuvent se fixer des réactifs électrophiles.
Voir aussi