FER L'élément métallique
Composés minéraux
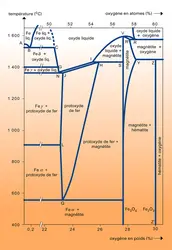
Le diagramme de la figure situe le domaine d'existence des différents oxydes : FeO, protoxyde de fer ; Fe3O4, magnétite Fe2O3, sesquioxyde.
Le protoxyde FeO est métastable à la température ordinaire. Il se forme au cours des traitements du minerai de fer et du travail à chaud du métal. Sa composition peut s'écarter notablement de la composition stœchiométrique, ce qui le rapproche d'un oxyde semi-métallique.
Le sesquioxyde existe sous deux formes allotropiques : la forme α rhomboédrique est la forme naturelle ; la forme quadratique préparée par oxydation de la magnétite a une structure ordonnée dérivant du spinelle. La magnétite est un oxyde mixte de type spinelle répondant à la formule [Fe23+ Fe2+]O42—. Elle est ferromagnétique et c'est un semi-conducteur dont la résistivité varie fortement avec la température. Ces ions Fe3+ et Fe2+ peuvent être remplacés par des ions M3+ et M2+, d'où une multiplicité de solutions solides.
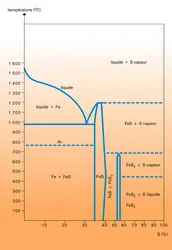
Le diagramme de la figure 9 indique les domaines d'existence des deux seuls composés fer-soufre. Le sulfure ferreux FeS tolère de larges écarts à la composition stœchiométrique, tant par excès de fer que par excès de soufre vis-à-vis du rapport 1/1. Des solutions solides dans lesquelles le fer ou le soufre sont remplacés par des équivalents (Mn, Ni... ; Sc, As...) sont très nombreuses. Le bisulfure FeS2 se présente sous deux formes cristallines : l'une instable, la marcassite, l'autre stable, la pyrite.
L' azote peut former des solutions solides d'insertion dans le fer α (nitroferrite, nitromartensite), dans le fer γ (nitro-austénite), dans le fer δ et 3 composés semi-métalliques : les nitrures Fe4N (γ′), Fe3N (ε′), Fe2N (ζ).
Le phosphore peut former des solutions solides avec le fer α et le fer γ et 4 composés définis : Fe3P, Fe2P, FeP, FeP2.
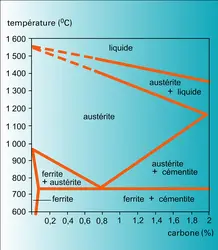
Le diagramme fer-carbone (fig. 10) est à la base de la connaissance des aciers et des fontes [cf. acier (technologie)]. Le carbone peut former : des solutions solides d'insertion dans le fer α (ferrite, martensite), dans le fer γ (austénite), dans le fer δ, et 4 composés semi-métalliques : Fe3C, la cémentite ; Fe5C2 ; le carbure de Hägg Fe7C3 ; et le carbure hexagonal non stœchiométrique voisin de Fe2C.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Simone TALBOT-BESNARD : maître de recherche au C.N.R.S.
Classification
Médias
Autres références
-
APPARITION DE L'INDUSTRIE DU FER
- Écrit par Nicole CHÉZEAU
- 183 mots
Les premières traces de l'industrie du fer sont attestées vers 1700 à 1500 avant J.-C. dans le sud du Caucase. À cette époque, les forgerons chalybes faisaient chauffer un mélange de minerai de fer et de charbon de bois dans un simple trou. Chez les Hittites, ce procédé primitif évolue vers le...
-
FER, FONTE ET ACIER - (repères chronologiques)
- Écrit par Olivier LAVOISY
- 585 mots
— 1700-— 1500 Début de l'industrie du fer avec les premières traces, au Sud du Caucase, de foyers permettant la réduction (élimination d'oxygène) de minerais de fer au charbon de bois.
Vers — 1250 Une lettre du roi hittite Hattusil III mentionne une épée en fer.
— 1100-— 800...
-
ACIER - Technologie
- Écrit par Louis COLOMBIER , Gérard FESSIER , Guy HENRY et Joëlle PONTET
- 14 178 mots
- 10 médias
Rappelons que le fer existe sous deux variétés allotropiques différentes, c'est-à-dire avec deux formes cristallines. -
AIMANTS
- Écrit par Roger FONTAINE
- 6 274 mots
- 13 médias
-
ALLIAGES
- Écrit par Jean-Claude GACHON
- 7 363 mots
- 5 médias
...mis en œuvre pour des usages tels que les pièces soumises aux plus gros efforts dans les trains d'atterrissage des avions (cf. acier – Technologie). L'acier le plus simple est un alliage de fer et de carbone, renfermant moins de 2 p. 100 en poids de carbone (9 atomes pour 100). Il faut rappeler que... -
APPARITION DES HAUTS-FOURNEAUX
- Écrit par Olivier LAVOISY
- 222 mots
En Occident, les premiers hauts-fourneaux apparaissent vraisemblablement dans la région de Liège durant la seconde moitié du xive siècle. Le principe est d'augmenter la taille des foyers pour accroître la production de fer. Cependant la réduction (élimination de l'oxygène) de minerais de fer...
- Afficher les 55 références