GELS
Le gel est formé de deux milieux dispersés l'un dans l'autre :
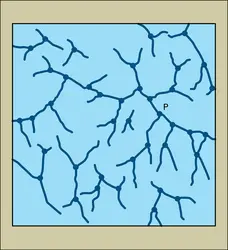
– le milieu dit « solide » est constitué de longues molécules connectées entre elles par des points de réticulation pour former un réseau tridimensionnel ;
– le milieu liquide (solvant) est constitué de molécules indépendantes.
Le gel se distingue d'une solution colloïdale où le milieu « solide » n'est pas connecté. Il est nécessaire de remarquer que la dénomination gel est parfois délicate à attribuer à certains corps, car la limite gel-solution colloïdale n'est pas franche.
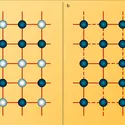
On distingue deux grandes familles de gels : les gels chimiques et les gels réversibles. Pour les gels chimiques, les points de réticulation sont formés par réaction chimique pour constituer le milieu « solide ». Celui-ci ne peut être dissous que par dégradation. Tandis que, pour les gels réversibles, les longues molécules sont reliées entre elles en certains points par des liaisons faibles. Ces liaisons peuvent être des microcristaux (chlorure de polyvinyle), des hélices (gélatine), des liaisons hydrogènes (alcool de polyvinyle). Pour liquéfier les gels réversibles, il suffit de modifier les conditions physiques (par exemple la température, le pH) ou de les soumettre à une agitation mécanique (thixotropie). Le gel se reforme lorsqu'on le replace dans les conditions physiques initiales.
Dans le cas des gels chimiques, la concentration de solvant peut varier (par simple évaporation), depuis la concentration d'équilibre jusqu'à la concentration nulle. On a alors un gel sec (le caoutchouc notamment).
Exemples de gels en biochimie, en agroalimentaire et en chimie
Le gel est un corps très particulier qui peut avoir un rôle de filtre, en laissant migrer sélectivement des éléments en fonction de leur dimension, ou un rôle de piège, en fixant des éléments. C'est aussi un corps très particulier grâce aux propriétés élastiques de la composante « solide ». Ces propriétés peuvent être modifiées en changeant la concentration en solvant, la taille ou la conformation des molécules entre points de réticulation. Ces propriétés justifient le rôle important du gel aussi bien dans la nature que dans les applications en chimie, en agroalimentaire et en biochimie.
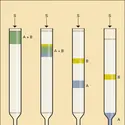
La peau, constituée de molécules de collagène, permet la libre diffusion des éléments – eau, oxygène, sels minéraux. Les gels employés en chromatographie (gel de silice, par exemple) ou en électrophorèse (polyacrylamide) permettent, en fonction du temps de transit à travers le gel, de séparer des particules de dimensions différentes. Les gels sont utilisés dans la fabrication de cristaux de corps peu solubles ; on fait réagir, par diffusion à travers un gel, deux composés solubles dont le mélange direct aurait donné une poudre. Par exemple, on obtient un cristal de calcite à partir du chlorure de calcium et du carbonate de sodium séparés par un gel de silice. En photographie, le chlorure d'argent est fixé par la gélatine qui, appliquée en couche mince sur un support, constitue les films. Dans les cas de l'agroalimentaire, les gels utilisés sont soit d'origines végétales, comme les algues (alginates, carraghenanes), les graines de céréales (amidon de maïs) ou les fruits (pectines), soit d'origines animales, comme la gélatine (collagène). L'emploi de ces gels permet une tenue supposée agréable des aliments, ainsi que l'immobilisation d'éléments nutritifs dans le réseau (par exemple, les crèmes desserts).
Dans le cas des cosmétiques comme dans celui des peintures, le rôle de fixateur d'un gel thixotrope est utilisé. Dans ces cas, les produits actifs sont dispersés dans des gels qui, sous agitation, deviennent des liquides visqueux facilement applicables en couche mince. Après application, le liquide peut retrouver sa structure de gel, et donc avoir[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Mireille ADAM : ingénieur au Commissariat à l'énergie atomique, Gif-sur-Yvette
- Michel DELSANTI : ingénieur au Commissariat à l'énergie atomique, Gif-sur-Yvette
Classification
Médias
Autres références
-
CHROMATOGRAPHIE
- Écrit par Robert ROSSET , Louis SAVIDAN et Alain TCHAPLA
- 17 046 mots
- 8 médias
La colonne est remplie d'un gel microporeux minéral ou organique : silice, polystyrène réticulé, dextrane réticulé. Quand un soluté en solution est en présence d'un milieu poreux non adsorbant, ses molécules diffusent dans ce milieu, établissant un équilibre de sa concentration en solution dans les... -
ÉLECTROPHORÈSE
- Écrit par Jean GUASTALLA , Jean MORETTI et Jean SALVINIEN
- 4 742 mots
- 10 médias
Le support est constitué à l'aide d'une solution de gélose (agar-agar) à 1 p. 100 dans le tampon choisi. On la coule à chaud sur une lame de verre où elle se solidifie par refroidissement. Le pouvoir de résolution est identique à celui du papier. Mais le gel d'agarose purifiée présente l'avantage de... -
ÉLECTROPHORÈSE EN CHAMP PULSÉ
- Écrit par Jean-Luc GUESDON
- 263 mots
La technique d'électrophorèse classique en gel d'agarose ou de polyacrylamide permet de séparer des fragments d'ADN suivant leur taille. Sur ces gels constitués d'un réseau désorganisé de longues fibres, on dépose l'ADN dont les molécules sont chargées négativement. Soumises à...
-
PERCOLATION
- Écrit par Jean ROUSSENQ
- 1 953 mots
- 3 médias
– Dans la transition de gélification (la prise d'une gélatine par exemple), des éléments polymériques s'associent pour former un réseau tridimensionnel. Au seuil de gélification (correspondant au seuil de percolation) apparaît un amas infini (le gel). On associe à la masse du gel la notion de paramètre...