HÉPATITE C
Article modifié le
Le virus de l'hépatite C
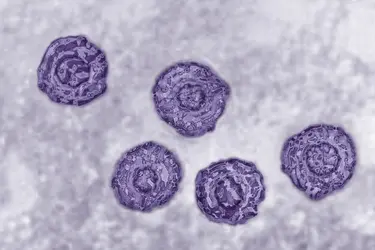
Les particules virales C sont de petites sphères de 60 nanomètres de diamètre, constituées de trois structures : de l’extérieur vers l’intérieur, une enveloppe protéo-lipidique, une capside protéique et le génome viral. Longtemps évanescent, le virus n’a été vu pour la première fois au microscope électronique qu’en 2016.
Le génome viral
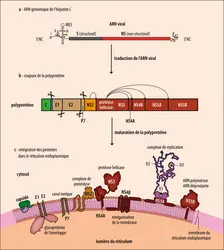
Le génome viral est un ARN simple brin linéaire long de 9,6 kilobases, de polarité positive, qui se lit donc (se décode en protéines) directement comme un ARN messager. Il comprend, de 5’ en 3’ : une région 5’ non codante, un cadre de lecture ouvert (partie de l’ARN codante pour des protéines) et une région 3’ non codante. La région dite « 5' non codante » –, très conservée parmi les différents isolats – exercerait une fonction régulatrice dans la traduction du génome viral dans les cellules infectées. Le cadre de lecture qui suit comprend deux régions :
– une région dite structurale qui code pour les protéines de capside et d'enveloppe. Les séquences codant pour ces dernières sont beaucoup moins conservées et des régions hypervariables y ont été identifiées ;
– puis une région dite non structurale qui code des protéines impliquées dans la réplication virale. Enfin, la région 3’ non codante comporte une région variable d’une souche virale à l’autre, une région poly-U/C et une région en 3’ très conservée.
Le taux de mutation des séquences nucléotidiques est d'environ 1,2·10–5/nucléotide/an. Cette variabilité génomique a permis de distinguer différents génotypes, sous-types et isolats du VHC. Les génotypes sont définis comme des groupes de virus présentant des divergences de 20 à 30 % des séquences nucléotidiques des protéines d’enveloppe entre groupes. La divergence entre isolats d'un même génotype est inférieure à 10 %. In fine, il existe au moins sept génotypes principaux (numérotés de 1 à 7), distribués en sous-types auxquels sont attribuées des lettres (par exemple 1a, 1b, 2a, 2b, 2c, 3a ...). La distribution des différents génotypes varie selon les zones géographiques et selon les facteurs de risque de contamination. La variabilité génomique était clairement associée à la qualité de la réponse thérapeutique avant l’avènement des antiviraux directs (AVD) oraux.
La traduction du cadre de lecture produit une protéine précurseur longue d'environ 3 000 aminoacides, secondairement clivée par une protéase virale en protéines structurales et non structurales. Il y a trois protéines structurales (une protéine de capside C et deux protéines d’enveloppe, E1 et E2). Il existe six protéines non structurales : P7 (dont le rôle est inconnu), NS2 (protéase), NS3 (activités protéase et NTPase/hélicase), NS4A (cofacteur de la protéase NS3), NSA4B (associée au complexe de réplication), NS5A (multifactorielle, associée au complexe de réplication) et NS5B (ARN-polymérase dépendante de l’ARN). Cette dernière enzyme, associée aux autres protéines virales non structurales et à des protéines de l’hôte, forme le complexe de réplication. Ce dernier permet, à partir de l’ARN viral infectant, la synthèse d’un brin d’ARN négatif, servant de matrice pour la synthèse de brins d’ARN positifs qui seront ensuite : soit protégés par la protéine de capside (encapsidés) et enveloppés par des fragments de membrane puis relargués sous forme de nouvelles particules virales ; soit utiles aux nouveaux messagers pour la synthèse des protéines virales. L’ensemble de ce processus est exclusivement intracellulaire, ce qui facilite l’adressage des drogues antivirales.
Physiopathogénie de l'infection virale C
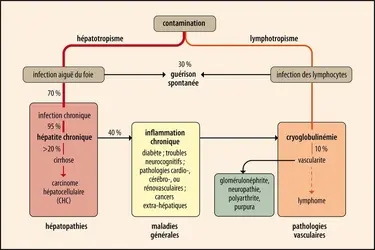
Le tropisme dominant du VHC pour les hépatocytes est lié à la présence d'un récepteur de la membrane cellulaire appelé CD81, et connu pour son rôle dans le métabolisme du cholestérol. Ce récepteur permet l’internalisation du virus, qui peut alors commencer le processus de multiplication. Il est présent sur les cellules sensibles, hépatocytes et aussi lymphocytes, bien que plus faiblement. C'est pourquoi ces derniers peuvent constituer un réservoir viral à l’origine de récidives infectieuses après transplantation hépatique. Cela explique également les deux versants, hépatique et extra-hépatique, de l'infection virale C.
Un effet toxique direct du virus sur les cellules n’est observé que dans les situations d'immunosuppression. En fait, l'impact de la réponse immunitaire de l’hôte contre le VHC est majeur dans les mécanismes de persistance du virus, de chronicisation et dans la genèse des lésions hépatiques. L'infection chronique se développe, en effet, malgré une forte réponse immune polyclonale humorale (anticorps) et cellulaire (surtout des lymphocytes T), contrairement à ce qui a lieu dans l'infection virale B. Cette réponse polyclonale est aussi principalement responsable de l'atteinte hépatique. En même temps, la réponse immunitaire (et le traitement) est également majeure dans l’élimination du virus. La réplication du VHC ne passe pas par un stade ADN proviral ou d’intégration génomique, au contraire du VIH et du VHB. Cela explique qu’il puisse y avoir guérison virologique, définie par un ARN du VHC indétectable douze semaines après guérison spontanée d’une infection aiguë ou lors d’une réponse virologique prolongée (RVP). On ne retrouve, dans ce cas, d’ARN viral ni dans les cellules mononuclées du sang ni dans les hépatocytes : il s’agit bien d’une véritable guérison virologique complète et durable. Celle-ci est confirmée par la transplantation d’organe de sujets infectés ayant bénéficié d’un traitement efficace. Contrairement au VHB, par exemple, la transplantation, malgré une immunosuppression profonde, ne conduit pas à une infection de l’organe transplanté.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Stanislas POL : professeur des Universités, praticien hospitalier, département d'hépatologie et d'addictologie, hôpital Cochin, Paris
- Anaïs VALLET-PICHARD : médecin, praticienne hospitalière, service d'hépatologie, hôpital Cochin, Paris
Classification
Médias
Autres références
-
CANCER - Cancers et virus
- Écrit par Sophie ALAIN , François DENIS et Sylvie ROGEZ
- 5 660 mots
- 6 médias
Deux virus sont susceptibles de provoquer des cancers du foie. Ils n'ont aucune parenté entre eux : le virus de l'hépatite B (HBV) est un virus à ADN et le virus de l'hépatite C (HCV), un virus à ARN. -
FOIE
- Écrit par Jacques CAROLI , Encyclopædia Universalis et Yves HECHT
- 9 975 mots
- 6 médias
Les virus à transmission « non naturelle », par lésion de la peau ou des muqueuses (parentérale) concernent les virus B, D, C. On les a découverts d'abord dans les hépatites qui ont suivi des transfusions du sang et de ses diverses fractions thérapeutiques (fractions antihémophiliques, plasma,... -
PRIX LASKER 2016
- Écrit par Gabriel GACHELIN
- 1 231 mots
- 1 média
...Ce prix revient à Ralf F. W. Bartenschlager, Charles M. Rice et Michael J. Sofia, « pour le développement d’un système d’étude de la réplication du virus de l’hépatite C et pour son utilisation pour révolutionner le traitement de cette maladie chronique, souvent mortelle ». Le petit virus à ... -
PRIX NOBEL DE PHYSIOLOGIE OU MÉDECINE 2020
- Écrit par Gabriel GACHELIN
- 1 165 mots
- 1 média
Le 5 octobre 2020, l’assemblée Nobel de l’Institut Karolinska a attribué conjointement le prix Nobel de physiologie ou médecine aux Américains Harvey J. Alter et Charles M. Rice ainsi qu’au Britannique Michael Houghton « pour la découverte du virus de l’hépatite C ». Après avoir honoré,...
Voir aussi
- INTERFÉRON
- CONTAMINATION
- HÉPATOCARCINOME
- ANTIVIRAUX
- VACCINS & SÉRUMS
- HÉPATOCYTE
- SÉROLOGIE
- GÉNOTYPE
- CHARGE VIRALE
- INFECTION
- TRANSAMINASE
- VIROLOGIE MÉDICALE
- RIBAVIRINE
- GÉNOME
- HÉPATITES
- CIRRHOSE
- SANTÉ DANS LE MONDE
- ANTICORPS
- FACTEUR DE RISQUE, épidémiologie
- LYMPHOCYTES
- HÉPATITE VIRALE
- PROTÉINES
- DÉPISTAGE, médecine
- EFFETS SECONDAIRES, pharmacologie
- RICE CHARLES M. (1952- )
- ALTER HARVEY J. (1935- )
- HOUGHTON MICHAEL (1949- )