HÉPATITE C
Article modifié le
Le traitement du virus de l’hépatite C
Traitement avant les antiviraux oraux à action directe
Une particularité de l’infection virale C est qu’elle est la seule infection virale chronique dont il soit possible de guérir : il n’y a en effet pas de réservoir viral et la réponse virologique prolongée (RVP), comme on l’a vu plus haut, constitue une véritable guérison virologique. Le point remarquable est que le traitement du VHC a évolué avec un taux de RVP qui a été multiplié par dix depuis 2000.
Avant l’identification du virus, les traitements standards par interféron (une famille de molécules de l’immunité innée antivirale) des hépatites « non A non B » avaient commencé au cours des années 1980. Un traitement de six mois par l’interféron alpha permettait la guérison d’environ 7 % des patients traités infectés par un génotype 1, le plus fréquent en Europe. Au début des années 1990, la ribavirine – une molécule de synthèse à large spectre d’activité antivirale – associée à l’interféron permettait de doubler le taux de guérison virologique. La stabilisation de la molécule d’interféron, a conduit à une plus grande efficacité antivirale : une seule injection sous-cutanée hebdomadaire associée à la prise de ribavirine selon des posologies adaptées au génotype viral, augmentait l’efficacité thérapeutique. Ainsi, en 1995, la guérison virologique était obtenue chez 45 % des sujets infectés par un génotype 1, et de 65 à 85 % pour les autres génotypes. Mais les effets secondaires liés à l’interféron ou à la ribavirine étaient fréquents, d’autant que le traitement était long (24 semaines pour les génotypes 2 et 3 ; 48 à 72 semaines pour les génotypes 1, 4, 5). En outre, un grand nombre de facteurs biologiques limitaient l’efficacité thérapeutique de la combinaison chez certains sujets.
Une révolution thérapeutique
Au milieu des années 2000, la meilleure caractérisation des protéines du VHC impliquées dans la réplication virale a défini des cibles nouvelles et le développement d’antiviraux spécifiques du virus de l’hépatite C.
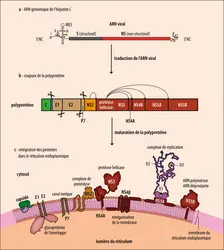
Les inhibiteurs spécifiques des protéases virales ont constitué une première vraie rupture dans le paysage thérapeutique. Ces molécules bloquent le clivage de la polyprotéine et ainsi la réplication du virus. Les premiers inhibiteurs de protéase ayant eu une autorisation de mise sur le marché entre 2011 et 2014 – télaprévir et bocéprévir – étaient combinés au traitement standard antérieur et permettaient une réduction de moitié de la durée du traitement chez 50 % des patients et de guérir environ les trois quarts des patients infectés par un génotype 1, au prix cependant d’effets secondaires qui s’ajoutaient à ceux liés au traitement classique. Une des limites du traitement était aussi son coût (aux alentours de 35 000 € pour les coûts directs) et son protocole, un grand nombre de gélules à absorber toutes les huit heures au moment d’un repas graisseux, se rajoutant aux quatre à six gélules de ribavirine.
En dépit de ces inconvénients, ces antiprotéases ont constitué la première étape de la révolution thérapeutique pour les infections liées au génotype 1, notamment chez les patients ayant une cirrhose ou une fibrose extensive de progression rapide. Le taux de guérison était alors de 75 % chez les sujets naïfs de traitement antérieur, et de 85 % chez les patients « rechuteurs », mais nettement plus faibles pour les autres.
Ces molécules de première génération ont été rapidement dépassées par des inhibiteurs spécifiques du complexe de réplication virale. Le développement du premier inhibiteur de la polymérase – le sofosbuvir – et du premier inhibiteur de la NS5A – le daclatasvir –, a transformé le pronostic et la tolérance des traitements, car environ 95 % des patients les recevant, d’abord associés au traitement standard, étaient guéris. La vraie révolution a suivi de près : la combinaison de deux ou trois AVD oraux combinant des inhibiteurs de protéase, des anti-NS5A et des antipolymérase NS5B, et l’abandon du traitement standard. Ces combinaisons permettent de guérir entre 95 et 98 % des patients traités, avec des résultats comparables quelle que soit la combinaison, et une très bonne tolérance.
Trois combinaisons orales ayant une activité pangénotypique sont ainsi disponibles depuis avril 2017 et permettent la guérison virologique de presque tous les patients dépistés. Le traitement dure de huit à douze semaines, est simplifié avec la prise de seulement une à trois gélules par jour, selon la combinaison, avec une tolérance satisfaisante.
En 2020, la puissance antivirale de ces traitements pangénotypiques a totalement annulé les facteurs de mauvaise réponse à un traitement, lequel peut être donné dans pratiquement toutes les situations cliniques. Enfin, les effets secondaires associés à ces traitements sont rares (céphalées, asthénie, troubles digestifs chez environ 15 % des patients).
De ce fait, les recommandations thérapeutiques sont désormais de traiter tous les patients infectés par le VHC en priorisant ceux ayant des maladies hépatiques (fibrose), ou extra-hépatiques (vascularite) avancées, ou ayant des risques de progression rapide de la fibrose. Depuis janvier 2017, en France, le coût du traitement est intégralement pris en charge pour tous les patients infectés par le VHC, après une politique de priorisation de l’accès au traitement selon la sévérité des atteintes entre 2014 et 2017 : les traitements antiviraux oraux ont été autorisés à partir de décembre 2013 chez les patients les plus graves sur le plan hépatique, puis chez ceux ayant des fibroses significatives ou des manifestations extra-hépatiques entre 2014 et 2015, avant l’ouverture de la prescription pour tous les patients en janvier 2017 et à tous les médecins depuis mai 2019.
Le bénéfice de ces traitements est non seulement individuel mais aussi collectif en diminuant les risques d’infection et de réinfection dans les communautés à risque. Les seules limites aux traitements restent liées à leur coût (environ 18 500 € la guérison en 2021, des génériques étant disponibles dans les pays du Sud), les interactions médicamenteuses parfaitement contournables, et l’observance thérapeutique par le patient, qui justifie pour les populations difficiles une éducation thérapeutique. Ainsi, l’histoire thérapeutique du VHC se termine sur une grande efficacité de médicaments pangénotypique, faciles d’usage et bien tolérés.
La guérison virologique s’accompagne habituellement d’une amélioration voire d’une guérison clinique des manifestations hépatiques et extra-hépatiques. Elle permet la réduction attendue de la mortalité liée aux impacts de l’infection chronique. Dans de larges cohortes de sujets infectés par le VHC et guéris, il existe, parallèlement à la réduction de la mortalité globale et de la mortalité hépatique, une réduction de la mortalité extra-hépatique. À titre d’exemple, dans la cohorte prospective CIRVIR de cirrhotiques compensés suivie par l’ANRS-INSERM, on observe une réduction des risques de survenue du carcinome hépatocellulaire chez les patients guéris (13,6 versus 1,9 % à trois ans et 21,8 versus 3,3 % à cinq ans). Encore cette évolution ne s’observe qu’en cas de comorbidité hépatique. La guérison virologique permet, en plus d’une réduction du cancer chez les patients cirrhotiques et non cirrhotiques, une amélioration de l’espérance de vie. La réduction de la mortalité hépatique est en rapport avec la capacité de remodelage de la fibrose à tous les stades de l’atteinte hépatique avec des possibilités de réversibilité de la cirrhose réduisant le risque de mortalité. Une réduction significative des risques de décompensation cirrhotique est accompagnée d’une réduction de même amplitude des risques d’infections bactériennes et, de façon plus démonstrative, une réduction des risques vasculaires (infarctus, AVC ou artériopathie oblitérante des membres inférieurs) avec une réduction de 9,1 à 2,3 % à trois ans et 12,3 versus 3,5 % à cinq ans chez les patients cirrhotiques guéris, par rapport aux patients non guéris. Si la fibrose extensive ou la cirrhose ont été associées à une augmentation du risque d’artériosclérose carotidienne, il est fascinant de noter que l’épaisseur de l’intima des carotides (leur paroi interne) diminue avec les traitements antiviraux oraux.
En cas de guérison virologique, les anomalies biologiques, morphologiques et les manifestations extra-hépatiques de vascularite disparaissent de façon majoritaire. Sur le plan hépatique et en l’absence de comorbidité hépatique, la fibrose va se remodeler et on assiste à une réparation progressive du foie ; la meilleure illustration en est la réduction significative de la mortalité hépatique (complication des cirrhoses y compris le carcinome hépatocellulaire) chez les patients guéris par opposition à ceux qui n’ont pas guéri. Ainsi, la guérison virologique permet de réduire les risques de complications hépatiques et extra-hépatiques, et l’extinction de l’activation inflammatoire associée à l’infection chronique semble réduire les manifestations vasculaires, métaboliques ou carcinomateuses extra-hépatiques.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Stanislas POL : professeur des Universités, praticien hospitalier, département d'hépatologie et d'addictologie, hôpital Cochin, Paris
- Anaïs VALLET-PICHARD : médecin, praticienne hospitalière, service d'hépatologie, hôpital Cochin, Paris
Classification
Médias
Autres références
-
CANCER - Cancers et virus
- Écrit par Sophie ALAIN , François DENIS et Sylvie ROGEZ
- 5 660 mots
- 6 médias
Deux virus sont susceptibles de provoquer des cancers du foie. Ils n'ont aucune parenté entre eux : le virus de l'hépatite B (HBV) est un virus à ADN et le virus de l'hépatite C (HCV), un virus à ARN. -
FOIE
- Écrit par Jacques CAROLI , Encyclopædia Universalis et Yves HECHT
- 9 975 mots
- 6 médias
Les virus à transmission « non naturelle », par lésion de la peau ou des muqueuses (parentérale) concernent les virus B, D, C. On les a découverts d'abord dans les hépatites qui ont suivi des transfusions du sang et de ses diverses fractions thérapeutiques (fractions antihémophiliques, plasma,... -
PRIX LASKER 2016
- Écrit par Gabriel GACHELIN
- 1 231 mots
- 1 média
...Ce prix revient à Ralf F. W. Bartenschlager, Charles M. Rice et Michael J. Sofia, « pour le développement d’un système d’étude de la réplication du virus de l’hépatite C et pour son utilisation pour révolutionner le traitement de cette maladie chronique, souvent mortelle ». Le petit virus à ... -
PRIX NOBEL DE PHYSIOLOGIE OU MÉDECINE 2020
- Écrit par Gabriel GACHELIN
- 1 165 mots
- 1 média
Le 5 octobre 2020, l’assemblée Nobel de l’Institut Karolinska a attribué conjointement le prix Nobel de physiologie ou médecine aux Américains Harvey J. Alter et Charles M. Rice ainsi qu’au Britannique Michael Houghton « pour la découverte du virus de l’hépatite C ». Après avoir honoré,...
Voir aussi
- INTERFÉRON
- CONTAMINATION
- HÉPATOCARCINOME
- ANTIVIRAUX
- VACCINS & SÉRUMS
- HÉPATOCYTE
- SÉROLOGIE
- GÉNOTYPE
- CHARGE VIRALE
- INFECTION
- TRANSAMINASE
- VIROLOGIE MÉDICALE
- RIBAVIRINE
- GÉNOME
- HÉPATITES
- CIRRHOSE
- SANTÉ DANS LE MONDE
- ANTICORPS
- FACTEUR DE RISQUE, épidémiologie
- LYMPHOCYTES
- HÉPATITE VIRALE
- PROTÉINES
- DÉPISTAGE, médecine
- EFFETS SECONDAIRES, pharmacologie
- RICE CHARLES M. (1952- )
- ALTER HARVEY J. (1935- )
- HOUGHTON MICHAEL (1949- )