- 1. Les isotopes naturels et artificiels de l’hydrogène
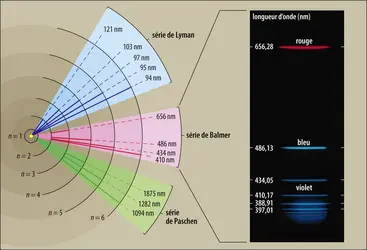
- 2. Le spectre de l’atome d’hydrogène et l’avènement de la mécanique quantique
- 3. Hydrogène et naissance de l’électrodynamique quantique
- 4. Structure du noyau de l’atome d’hydrogène et chromodynamique quantique
- 5. L’antihydrogène
- 6. Les phases de l’hydrogène
- 7. Hydrogène et astrophysique
- 8. Hydrogène et énergie
HYDROGÈNE (physique)
Hydrogène et naissance de l’électrodynamique quantique
En 1947, Willis Lamb (1913-2008) réussit à mesurer très précisément une minuscule différence d'énergie entre deux états excités de l’atome d’hydrogène qui ne devait pas exister selon les théories existantes. Ce « décalage de Lamb » – comme on l'appelle depuis lors – montre des insuffisances dans la théorie quantique existante, malgré les progrès introduits en 1928 par Paul Dirac (1902-1984) pour décrire correctement l'électron en tenant compte de son spin. Pour expliquer ce décalage des niveaux d’énergie de l’hydrogène, il apparaît qu’en gardant le formalisme introduit par Dirac pour l’électron, il faut aussi « quantifier » le champ électromagnétique et considérer en même temps l’énergie de l’électron sur son orbite et l’état du champ magnétique présent autour du noyau. En d’autres termes, il faut incorporer l’électromagnétisme dans la mécanique quantique. Il faut en particulier prendre en compte le fait que l'électron est entouré de paires virtuelles évanescentes formées d’un électron (e–) et d’un positron (e+), phénomène qu'on désigne comme la « structure complexe du vide quantique ». Cela signifie qu’on doit soigneusement distinguer le « néant » du « vide physique quantique », ce dernier étant défini comme l’état d’énergie minimale d’un système physique, par exemple l’entourage d’un électron. Les travaux théoriques, initiés par un premier calcul de Hans Bethe (1906-2005) en 1947 et parachevés quelques années plus tard par Richard Feynman (1918-1988), Julian Schwinger (1918-1994) et Sin-Itiro Tomonaga (1906-1979), et beaucoup d’autres théoriciens, ont permis la construction de ce que beaucoup considèrent comme un des plus grands succès de la physique moderne : l’électrodynamique quantique. Toutes les lois de l’électromagnétisme classique dérivent de l’électrodynamique quantique, ce qui permet de plus de comprendre des phénomènes optiques ou magnétiques nouveaux, des lasers aux semi-conducteurs.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Bernard PIRE : directeur de recherche émérite au CNRS, centre de physique théorique de l'École polytechnique, Palaiseau
Classification
Médias
Autres références
-
DÉCOUVERTE DE L'HYDROGÈNE PAR CAVENDISH
- Écrit par Bernard PIRE
- 728 mots
L’article envoyé en mai 1766 par l’honorable Henry Cavendish (1731-1810) à la Royal Society, dont il est membre, décrit de façon magistrale la découverte d’un gaz léger s’échappant de certaines réactions chimiques : l’hydrogène. Ces travaux, publiés dans la livraison datée du 1...
-
ACIDO-BASIQUE ÉQUILIBRE
- Écrit par Pierre KAMOUN
- 2 958 mots
- 1 média
L'apport alimentaire en ions hydrogène H+ est essentiellement représenté par les amino-acides introduits par les protéines (10 g de protéines libèrent 6 à 7 milliéquivalents d'ions H+). -
AMMONIAC
- Écrit par Henri GUÉRIN
- 5 035 mots
- 5 médias
L'action des sels d'ammonium sur les métaux dans l'ammoniac liquide est semblable à celle des acides en phase aqueuse : on obtient un sel du métal attaqué et un dégagement d' hydrogène :
-
ARCHÉES ASGARD
- Écrit par Patrick FORTERRE
- 3 786 mots
- 3 médias
...avec une bactérie sulfato-réductrice du genre Desulfovibrio et une archée productrice du méthane du genre Methanogenium. L’archée Loki produit de l’hydrogène qui est utilisé par la bactérie pour produire du sulfure d’hydrogène et par Methanogenium pour produire du méthane. Hiroyuki Imachi... -
ASTROCHIMIE
- Écrit par David FOSSÉ et Maryvonne GERIN
- 4 390 mots
- 3 médias
- Afficher les 59 références