- 1. La découverte des terres rares
- 2. État naturel
- 3. Séparation et purification
- 4. Propriétés Physiques
- 5. Propriétés chimiques
- 6. Toxicité des terres rares
- 7. Applications liées aux propriétés chimiques
- 8. Applications liées aux propriétés optiques
- 9. Applications liées aux propriétés magnétiques
- 10. Économie des lanthanides
- 11. Bibliographie
LANTHANE ET LANTHANIDES
Propriétés Physiques
Rayons ioniques et électronégativité
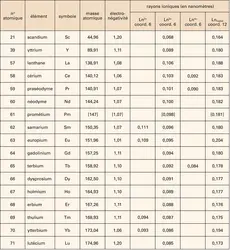
Le volume occupé par un ion dans un cristal dépend de sa charge électrique, du nombre et du type de ligandes (coordination) et du caractère ionique de la liaison (covalence). Les terres rares présentent le paradoxe d'avoir des rayons ioniques décroissants lorsque le numéro atomique augmente. C'est la contraction lanthanidique qui atteint 20 p. 100 de la distance maximale à la fin de la série. Elle s'explique par une attraction plus forte du noyau lorsque le nombre atomique augmente, alors que l'électron gagné va se loger dans la couche 4f, bien protégée au cœur du cortège électronique et sans créer d'espace supplémentaire. Au contraire, l'électronégativité, caractérisant l'affinité d'un élément pour un gain d'électrons, est moyenne et ne varie que relativement peu avec l'ion (tabl. 1). Toutefois, le lanthane, le gadolinium et le lutécium constituent une rupture dans l'évolution de l'électronégativité, en raison de leurs caractères à couche électronique f respectivement vide, demi-pleine et pleine.
Configurations électroniques
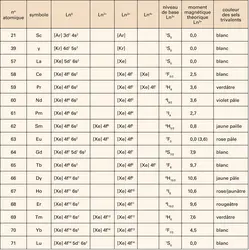
Les propriétés des terres rares sont intimement liées à leurs configurations électroniques (tabl. 6). Celles des atomes neutres sont [Xe]6s24fN+1, [Xe] représentant la configuration électronique à couches complètes du xénon. N, le nombre d'électrons 4f, varie de 0 à 14 avec le numéro atomique croissant de l'élément. Toutefois, les configurations de La, Gd et Lu, sont différentes : [Xe]6s25d14fN (N = 0, 7 et 14) correspondant à des couches électroniques 4f respectivement vides, à demi-pleine et pleine. L'état d'oxydation le plus stable étant trivalent, les configurations correspondantes sont [Xe]4fN. Cela implique que les propriétés physiques de ces éléments dépendent en grande partie des caractéristiques de la partie radiale de la fonction d'onde associée aux orbitales atomiques f.
Parmi tous les éléments connus de la classification périodique, seuls les lanthanides et les actinides possèdent de telles orbitales. La caractéristique principale de l'orbitale 4f est d'être interne dans les couches électroniques successives, en raison d'une distance moyenne au noyau plus faible, protégée par des orbitales externes de type 5s et 6p. Il en résulte que la liaison chimique modifiera peu l'orbitale atomique et que le champ électrique (champ cristallin) créé par l'environnement des atomes voisins sera faible, ce qui explique une grande partie des propriétés optiques et magnétiques.
Les configurations électroniques des terres rares sont parfaitement analysées par la théorie des spectres atomiques développée au milieu du xxe siècle. L'application des méthodes de la théorie des groupes finis et infinis ouvre une voie royale pour leur compréhension formelle. Ce n'est que depuis le début des années 1970 que leur simulation se fait aisément ; il suffit de nos jours d'un simple ordinateur de bureau. On considère que les électrons des couches incomplètes sont soumis à des interactions perturbatrices à l'action d'un champ central, représentant l'attrait des électrons par le noyau. On les exprime selon la méthode quantique des perturbations de Dirac. Si l'on considère au départ une situation sans perturbation, la configuration électronique 4fN se définira par sa dégénérescence, c'est-à-dire le nombre de déterminants de Slater qu'il est possible de construire sur la base des différentes valeurs prises par les nombres quantiques principaux (n), orbitaux (l) et de spin (s) des électrons 4f. Cette situation serait associée à une seule valeur énergétique. L'ion libre, supposé un moment isolé de tout environnement chimique, tel qu'on le rencontre dans un plasma, aura cette dégénérescence partiellement levée sous l'effet[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Concepcion CASCALES
:
cientifico titular - Patrick MAESTRO : auteur
- Pierre-Charles PORCHER : directeur de recherche au C.N.R.S.
- Regino SAEZ PUCHE : professeur de chimie inorganique
Classification
Médias
Autres références
-
COMPLEXES, chimie
- Écrit par René-Antoine PARIS et Jean-Pierre SCHARFF
- 4 306 mots
- 5 médias
...éliminer les cations métalliques des eaux résiduaires par coagulation-floculation. En outre, les séparations très délicates des éléments du groupe des lanthanides et du groupe des actinides n'ont pu être réalisées commodément que selon deux techniques utilisées soit séparément, soit conjointement :... -
IONS ÉCHANGEURS D'
- Écrit par Robert ROSSET
- 6 110 mots
- 13 médias
La séparation deslanthanides : elle est effectuée sur un échangeur de cations en superposant à la réaction d'échange simple, pour laquelle les différences d'affinité sont quasi nulles, une réaction de formation de complexes, en solution, avec l'acide α-hydroxyisobutyrique (CH... -
MAGNÉSIUM
- Écrit par Maurice HARDOUIN et Michel SCHEIDECKER
- 4 275 mots
- 8 médias
L'addition de thorium (radioactif), delanthanides ou d'argent permet de maintenir les propriétés mécaniques mesurées à chaud. Ces éléments sont compatibles avec le zirconium, et les propriétés spécifiques des deux types d'addition sont cumulatives. Ces alliages sont susceptibles de durcissement... -
MAGNÉTISME
- Écrit par Damien GIGNOUX , Étienne de LACHEISSERIE et Louis NÉEL
- 15 620 mots
- 14 médias
Le magnétisme le plus marqué et le mieux compris est celui des terres rares, oulanthanides, dont les électrons « magnétiques » sont ceux de la couche profonde 4f, écrantée par d'autres couches complètes extérieures, 5s et 5p. Les effets de l'environnement, sans bouleverser totalement... - Afficher les 7 références