LIAISONS CHIMIQUES Liaison hydrogène
Article modifié le
Importance des liaisons hydrogène
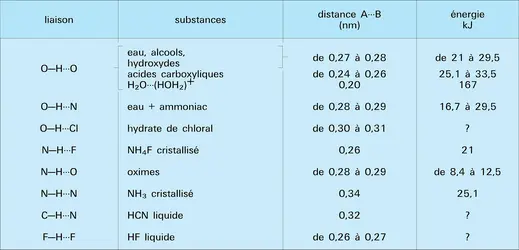
Malgré les faibles énergies mises généralement en jeu dans les liaisons hydrogène, le rôle qu'elles jouent du point de vue structural est très important. En effet, ce sont elles qui assurent la cohésion de nombreux cristaux de type moléculaire (glace, alcools, phénols, oxacides, hydroxydes, sels hydratés, etc.) et qui, pour une part importante, sont responsables des associations entre les diverses bases fondamentales entrant dans l'édification des acides nucléiques ainsi qu'entre les protéines pour constituer les tissus vivants (cf. biologie-La biologie moléculaire, protéines).
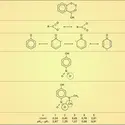
Du point de vue chimique, l'établissement de liaisons hydrogène peut altérer assez profondément le comportement des molécules. Par exemple, dans la série des phénols substitués :
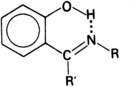
la liaison intramoléculaire O–H...N réduit la réactivité du groupement C=N jusqu'à le rendre inerte vis-à-vis de certains réactifs caractéristiques de celui-ci.
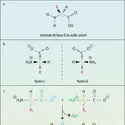
La présence d'une liaison intramoléculaire dans un acide carboxylique, mettant en jeu le groupement C=O, exalte en général l'acidité de la molécule. En effet, l'énergie de liaison dans l'ion est supérieure à celle de la liaison dans la molécule, à cause de la charge nette négative apparue sur l'oxygène. Par exemple, l'acide salicylique a une constante d'acidité égale à seize fois celle de l'acide benzoïque. Si, au contraire, c'est le groupement OH de l'acide qui est impliqué dans une liaison intramoléculaire, par suite de la présence en position convenable d'un atome électronégatif pouvant jouer le rôle de B, le départ du proton sera plus difficile et, de ce fait, l'acidité sera diminuée. C'est le cas des acides benzoïques orthohalogénés dont l'acidité augmente au fur et à mesure que l'électronégativité de l'halogène diminue, c'est-à-dire que la liaison est moins solide.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- André JULG : professeur émérite à l'université de Provence
Classification
Médias
Autres références
-
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 367 mots
- 7 médias
Le caractère acide d'une molécule HA repose principalement sur la nature de la liaison chimique entre H et le reste A de la molécule. -
ADSORPTION
- Écrit par Xavier DUVAL
- 4 819 mots
- 2 médias
En chimisorption, les liaisons dans les molécules sont profondément modifiées par suite de la formation de liaisons chimiques avec l'adsorbant. L'objectif des recherches concerne principalement la description des espèces adsorbées et l'étude de leur stabilité, en relation avec leur rôle essentiel d'intermédiaires... -
AMINOACIDES ou ACIDES AMINÉS
- Écrit par Encyclopædia Universalis et Pierre KAMOUN
- 3 487 mots
- 6 médias
...nettement les acides aminés les uns des autres en leur conférant des propriétés physico-chimiques particulières. Du fait de ces interactions, des groupes R, éloignés les uns des autres dans la chaîne ou les chaînes, peuvent être rapprochés dans la structure spatiale et constituer, par exemple, le centre réactif... -
ANTIMOINE
- Écrit par Encyclopædia Universalis et Jean PERROTEY
- 3 876 mots
- 3 médias
...3- n'ont pu être caractérisés. L'ion Sb5+ n'existe pas, mais Sb3+ est connu, ce qui n'est pas le cas de son homologue arsénié. Comme dans le cas de l'arsenic, deux principaux modes de liaison sont possibles pour les composés trivalents, avec comme conséquence des propriétés structurales... - Afficher les 38 références
Voir aussi
- HYDROGÈNE LIAISON
- INTERACTIONS MOLÉCULAIRES
- EAU, physico-chimie
- TEMPÉRATURE DE FUSION
- RMN (résonance magnétique nucléaire), physico-chimie
- DIFFRACTION PAR LES CRISTAUX
- HYDROXYLE ou OXHYDRYLE
- INTRAMOLÉCULAIRES FORCES
- THERMODYNAMIQUE CHIMIQUE
- POLARISATION, chimie
- ASSOCIATION MOLÉCULAIRE
- CRISTAL MOLÉCULAIRE
- MISCIBILITÉ
- ÉNERGIE DE LIAISON
- STABILITÉ, chimie
- TEMPÉRATURE D'ÉBULLITION