LIAISONS CHIMIQUES Liaisons biochimiques faibles
Morphogenèse des macromolécules et de leurs associations
Les macromolécules biologiques sont des polymères à la structure originale. Deux classes particulièrement importantes sont les acides nucléiques, dont la structure est associée à leur rôle de matrice du patrimoine héréditaire, et les protéines, qui sont les objets de l'expression de ce patrimoine et les effecteurs de la vie cellulaire.
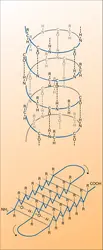
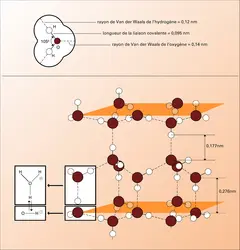
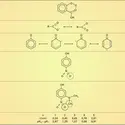
Les protéines sont constituées par un enchaînement linéaire d' acides aminés unis par une liaison covalente, la liaison amide, appelée dans ce cas liaison peptidique. Ce sont donc des polypeptides. Il existe vingt acides aminés naturels, et la structure primaire d'une protéine est réalisée par la disposition séquentielle des différents acides aminés. En conséquence de cette organisation séquentielle, la forme géométrique de la protéine varie. Il existe pourtant certaines caractéristiques qu'on retrouve dans un grand nombre de protéines et qu'on regroupe sous le nom générique de structure secondaire. Il s'agit de structures hélicoïdales (hélice α), stabilisées grâce à la contribution de liaisons hydrogène régulièrement réparties entre atomes d'oxygène et d'azote de deux liaisons peptidiques, de structures presque planes (feuillets β), résultant elles aussi d'un arrangement stabilisé par des liaisons hydrogène particulières, mais aussi des liaisons de Van der Waals entre les résidus variables des acides aminés, et enfin de tournants β qui utilisent une géométrie particulière de certains acides aminés leur permettant un arrangement régulier grâce à la contribution de diverses liaisons faibles. La forme finale de la protéine, que l'on associe généralement à sa fonction dans la vie cellulaire, est sa structure tertiaire. Elle résulte de la combinaison de sections organisées suivant les divers types de structure secondaire (dont la contribution varie le plus souvent entre 10 et 90 p. 100 du total des acides aminés) et d'acides aminés arrangés dans l'espace de manière à constituer un maximum d'interactions faibles, le plus souvent en exposant à la surface de la protéine des acides aminés permettant de nombreuses liaisons avec l'eau, et, au contraire, formant un grand nombre de liaisons de Van der Waals vers l'intérieur.
On distingue de même pour les acides nucléiques une structure primaire (enchaînement avec répétition de quatre nucléotides) et une structure secondaire dont le type le plus connu est la fameuse hélice d'ADN dont le modèle a été proposé en 1953 pour expliquer le mécanisme de la reproduction du patrimoine héréditaire.
L'un des problèmes majeurs de la biologie moléculaire est de proposer des mécanismes permettant de rendre compte de la morphogenèse des macromolécules. Deux hypothèses, qui ne sont pas exclusives, peuvent être avancées. Ou bien c'est au cours de la biosynthèse de ces molécules qu'elles prennent leur forme définitive, ou bien, par la seule présence des interactions entre la molécule et le solvant, la macromolécule s'organise dans l'espace. Bien qu'on sache aujourd'hui que la première hypothèse est plus proche de ce qui se passe in vivo, de nombreuses expériences faites sur des molécules purifiées et isolées ont montré que la machinerie biosynthétique n'est pas nécessaire à la genèse de la forme finale, dans la plupart des cas. Il est possible, en effet, de « dénaturer », en les transformant en une « pelote statistique », les protéines ou les acides nucléiques (en changeant de solvant ou en élevant la température) et d'étudier, à partir de cette forme plus ou moins aléatoire, les conditions du retour à la forme primitive.
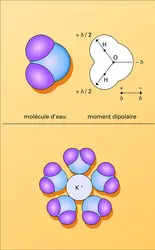
Ainsi, plonger la double hélice d'ADN dans la formamide, au lieu de l'eau contenant des ions appropriés, conduit à la disparition de sa forme géométrique.[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Antoine DANCHIN : directeur de recherche au CNRS, professeur à l'Institut Pasteur
Classification
Médias
Autres références
-
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 364 mots
- 7 médias
Le caractère acide d'une molécule HA repose principalement sur la nature de la liaison chimique entre H et le reste A de la molécule. -
ADSORPTION
- Écrit par Xavier DUVAL
- 4 819 mots
- 2 médias
En chimisorption, les liaisons dans les molécules sont profondément modifiées par suite de la formation de liaisons chimiques avec l'adsorbant. L'objectif des recherches concerne principalement la description des espèces adsorbées et l'étude de leur stabilité, en relation avec leur rôle essentiel d'intermédiaires... -
AMINOACIDES ou ACIDES AMINÉS
- Écrit par Encyclopædia Universalis et Pierre KAMOUN
- 3 486 mots
- 6 médias
...nettement les acides aminés les uns des autres en leur conférant des propriétés physico-chimiques particulières. Du fait de ces interactions, des groupes R, éloignés les uns des autres dans la chaîne ou les chaînes, peuvent être rapprochés dans la structure spatiale et constituer, par exemple, le centre réactif... -
ANTIMOINE
- Écrit par Encyclopædia Universalis et Jean PERROTEY
- 3 875 mots
- 3 médias
...3- n'ont pu être caractérisés. L'ion Sb5+ n'existe pas, mais Sb3+ est connu, ce qui n'est pas le cas de son homologue arsénié. Comme dans le cas de l'arsenic, deux principaux modes de liaison sont possibles pour les composés trivalents, avec comme conséquence des propriétés structurales... - Afficher les 38 références