MATIÈRE (physique) État gazeux
Article modifié le
Absorption d'un milieu gazeux
Dans le cas d'un gaz sous faible pression, les interactions entre molécules sont faibles et on peut relier les propriétés d'absorption ou d'émission du gaz à celles de la molécule isolée.
Du fait du principe de la conservation de l'énergie, l'énergie perdue (absorption) ou gagnée (émission) par le rayonnement se retrouve sous la forme d'énergie gagnée ou perdue par les molécules. Cet effet se traduit essentiellement par l'échange d'un photon d'énergie hν entre la molécule et le rayonnement :

Les niveaux d'énergie peuvent être discrets ou appartenir au continuum. Dans le premier cas, on observe l'existence de raies spectrales de fréquences ou de nombres d'onde bien déterminés alors que, dans le second cas, on a une absorption continue.
Les transitions entre niveaux d'énergie sont le plus souvent des transitions dipolaires électriques qui résultent de l'interaction du moment dipolaire électrique de la molécule avec le rayonnement électromagnétique. Elles ne sont pas toutes permises et obéissent à ce qu'il est convenu d'appeler des règles de sélection.
L'intensité lumineuse I(v̄) transmise par une couche homogène de gaz absorbant d'épaisseur l éclairée par un rayonnement incident d'intensité I0(v̄) est donnée par la loi de Beer-Lambert :
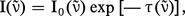
L'épaisseur optique s'exprime en fonction du coefficient d'absorption α (v̄) :
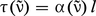
A (v̄) et la transmission T (v̄) par :
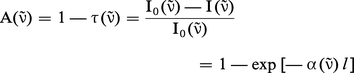
Spectres de raies
Lorsque l'absorption du rayonnement lumineux correspond à des transitions entre niveaux discrets, on observe ce qu'il est convenu d'appeler un spectre de raies, et pour chaque raie de nombre d'onde v̄0 on a :


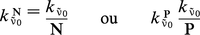
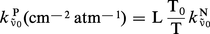
En définitive, le coefficient d'absorption s'écrit :
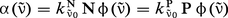
Le profil de Gauss (ou profil gaussien) est le profil d'une raie dont l'élargissement est dû uniquement à l'effet Doppler. En effet, compte tenu de l'agitation thermique, toutes les molécules n'absorbent pas le rayonnement exactement à la fréquence v̄0, et il en résulte un profil qui s'écrit :
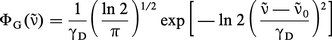
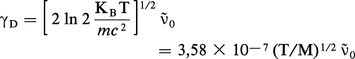
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Henri DUBOST : docteur ès sciences, directeur de recherche au C.N.R.S.
- Jean-Marie FLAUD : docteur ès sciences, directeur de recherche au C.N.R.S.
Classification
Médias
Autres références
-
ÉTAT DE LA MATIÈRE, notion d'
- Écrit par Bernard PIRE
- 1 521 mots
L'expérience quotidienne permet à chacun d'appréhender la notion d'état de la matière (parfois appelé phase) et celle de transition de phase qui lui est étroitement liée. L'exemple typique est celui des trois états si différents que prend l'eau lorsque sa température varie : à partir de 0 ...
-
MATIÈRE, notion de
- Écrit par Jean-Marc LÉVY-LEBLOND
- 2 022 mots
Le mot « matière » cache sous sa généralité abstraite une origine concrète fort éclairante. En latin archaïque, materia appartient à la langue rustique et désigne la substance dont est fait le tronc de l'arbre, en tant qu'elle est productrice (de branches, de feuilles). L'élargissement successif...
-
ANTIMATIÈRE
- Écrit par Bernard PIRE et Jean-Marc RICHARD
- 6 934 mots
- 4 médias
...associé est bâti avec les antiquarks correspondants. Les mésons résultent de la liaison d'un quark et d'un antiquark. Dans cette description moderne, la matière est constituée par trois « générations » de quarks et de leptons, le nombre trois a été établi par les expériences du C.E.R.N. (laboratoire européen... -
ATOME
- Écrit par José LEITE LOPES
- 9 146 mots
- 13 médias
L'atome est le terme ultime de la division de la matière dans lequel les éléments chimiques conservent leur individualité. C'est la plus petite particule d'un élément qui existe à l'état libre ou combiné. On connaît 90 éléments naturels auxquels s'ajoutent le ...
-
BOHR ATOME DE
- Écrit par Bernard PIRE
- 369 mots
- 1 média
Deux ans après avoir soutenu sa thèse sur la théorie électronique des métaux, le physicien danois Niels Bohr (1885-1962) écrit en 1913 trois articles fondamentaux qui révolutionnent la compréhension de la structure de la matière. Le premier, paru le 5 avril dans le Philosophical Magazine...
-
ATOME, notion d'
- Écrit par Bernard PIRE
- 1 499 mots
« Brique insécable » de la matière selon son étymologie, l'atome est le terme ultime de la division de la matière dans lequel les éléments chimiques conservent leur individualité. C'est la plus petite particule d'un élément qui existe à l'état libre ou combiné, les corps simples étant...
- Afficher les 40 références
Voir aussi
- ONDE ou RAYONNEMENT ÉLECTROMAGNÉTIQUE
- GAZ DIATOMIQUES
- GAZ POLYATOMIQUES
- ABSORPTION, physique
- PRESSION, physique
- POLARISABILITÉ MOLÉCULAIRE
- UNITÉS SYSTÈMES D'
- ÉTATS DE LA MATIÈRE
- LIBRE PARCOURS MOYEN
- POTENTIEL INTERMOLÉCULAIRE
- INTERACTIONS MOLÉCULAIRES
- ISOBARE
- PHASE TRANSITIONS DE
- VITESSE
- ÉTAT CHANGEMENT D'
- COLLISION, physique
- COLLISIONS ÉLASTIQUES
- ÉQUILIBRE THERMODYNAMIQUE
- MOLÉCULES DIATOMIQUES
- DIFFUSION
- ÉTAT ÉQUATION D'
- ÉNERGIE INTERNE
- DIAGRAMME, thermodynamique
- POINT CRITIQUE
- EXCITATION ÉLECTRONIQUE ÉNERGIE D'
- CHARLES LOI DE
- COMPRESSIBILITÉ ISOTHERME COEFFICIENT DE
- CLAPEYRON DIAGRAMME DE
- FUSION
- MAXWELL-BOLTZMANN DISTRIBUTION DE
- GAZ MONOATOMIQUES
- GAZ RÉELS
- GAZ PARFAITS LOI DES
- LOSCHMIDT NOMBRE DE
- GAY-LUSSAC LOI DE
- ISOTHERME
- VAN DER WAALS ÉQUATION DE
- POLAIRES MOLÉCULES
- TRANSMISSION, optique
- VAPORISATION
- SUBLIMATION, thermodynamique
- POINT TRIPLE, thermodynamique
- MOLÉCULES POLYATOMIQUES
- THERMIQUE AGITATION
- ROTATION MOLÉCULAIRE ÉNERGIE DE
- VIBRATION MOLÉCULAIRE ÉNERGIE DE
- VARIABLES D'ÉTAT
- BEER-LAMBERT LOI DE
- TRANSITION, physique
- ÉNERGIE POTENTIELLE
- PASCAL, unité
- ÉPAISSEUR OPTIQUE
- ENTHALPIE
- GAZEUX ÉTAT
- FONCTION D'ÉTAT, thermodynamique
- TRAVAIL, physique
- TEMPÉRATURE
- BOLTZMANN CONSTANTE DE
- PARTITION FONCTION DE
- ÉNERGIE LIBRE DE HELMHOLTZ
- NIVEAU, physique atomique
- ISOCHORE
- JOULE LOIS DE, thermodynamique
- BOYLE-MARIOTTE LOI DE
- ADIABATIQUE TRANSFORMATION
- CAPACITÉ CALORIFIQUE
- AMAGAT DIAGRAMME D'
- LONDON FORCES DE
- VIRIEL ÉQUATION DU
- ÉNERGIE CINÉTIQUE
- DISTRIBUTION DE CHARGE
- PHASES, physico-chimie
- TEMPÉRATURE CRITIQUE
- TRANSPORT ÉQUATION DE
- TRANSFORMATIONS THERMODYNAMIQUES
- AVOGADRO NOMBRE D'
- RAIE SPECTRALE
- SPECTRE D'ABSORPTION
- MOMENT ÉLECTRIQUE
- COEFFICIENT DE DIFFUSION
- CONDUCTION THERMIQUE
- TORR ou MILLIMÈTRE DE MERCURE, unité