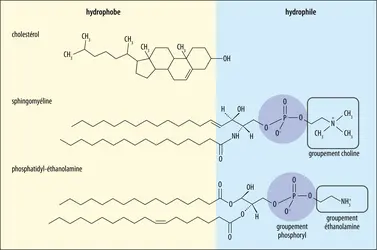
- 1. La double couche de lipides, une structure commune à toutes les membranes biologiques
- 2. Le modèle de la membrane mosaïque fluide
- 3. Mouvements affectant la membrane cellulaire
- 4. Mouvements de particules et macromolécules
- 5. Quid de la perméabilité sélective ?
- 6. La membrane comme interface dynamique
- 7. Bibliographie
MEMBRANES CELLULAIRES
Article modifié le
Mouvements de particules et macromolécules
Les amibes lancent des pseudopodes et englobent une microgoutte du milieu extracellulaire qui contient des bactéries et fragments divers, leur nourriture : on parle de pinocytose, phénomène non spécifique. En 1886, lors de son séjour au laboratoire de biologie marine de Messine, Elie Metchnikoff observe que des cellules de l'intestin d'une étoile de mer sont capables de fixer des particules, puis de les internaliser : on parle de phagocytose, un phénomène plus précis que le précédent, mais peu spécifique lui aussi. Lorsque, deux ans plus tard, il étend ses observations à l'absorption de bactéries par des cellules immunitaires de vertébrés vaccinés contre une bactérie, Metchnikoff décrit une phagocytose spécifique – elle n’existe que faiblement chez les animaux non vaccinés – d'une bactérie, dont on a montré ensuite qu’elle était due aux anticorps antibactéries qui établissent un pont entre la cellule et la bactérie : ce phénomène constitue l’endocytose spécifique.
Endocytose spécifique
L’endocytose par récepteur spécifique est une situation dans laquelle les mouvements de la membrane cellulaire permettent de faire pénétrer dans la cellule certaines substances du milieu extracellulaire, à la suite de leur interaction avec une protéine réceptrice membranaire. L’endocytose implique en outre la coordination des mouvements de la membrane avec ceux du cytosquelette. À l’inverse, l’exocytose est le phénomène qui permet la sécrétion de molécules ou de particules virales ; elle mobilise également les membranes intracellulaires et plasmatique et le cytosquelette.
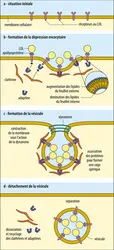
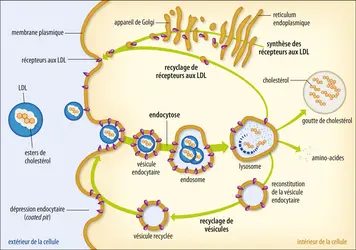
Les mécanismes de l'endocytose par récepteur spécifique sont presque les mêmes pour l’entrée dans la cellule d’un virus comme le SARS-Cov-2 que pour la pénétration du cholestérol à partir du sang. On partira de ce dernier exemple car la complexité des phénomènes sous-jacents a été démêlée d'abord par l'étude des différentes formes de l'hypercholestérolémie essentielle d'origine génétique chez l'homme – ce travail valut leur prix Nobel aux Américains M. S. Brown et J. L. Goldstein en 1985. Les particules appelées LDL (pour low density lipoproteins) sont des édifices plurimoléculaires qui assurent le transport du cholestérol dans le sang. Un de leurs composants protéiques, l’apolipoprotéine B, se lie à son récepteur spécifique situé sur la face externe de la cellule. Ce récepteur est une protéine transmembranaire qui s’associe à une protéine de la famille des adaptines sur la face interne de la membrane. Une adaptine fixe elle-même une molécule rigide du cytosquelette, une des clathrines, elles-mêmes édifices de trois protéines. Le complexe ainsi formé (apolipoprotéine-récepteur-adaptine-clathrine ou LDL) diffuse dans le plan de la membrane et se rassemble, révélant des structures spécialisées dans l'endocytose, longtemps énigmatiques à la seule observation en microscopie électronique : les puits recouverts (coated pits). Ces zones apparaissent spontanément plusieurs milliers de fois par minute dans une cellule mobile. La membrane y est déformée localement ; son feuillet interne s’appauvrit en lipides, au contraire du feuillet externe. Des mécanismes flip-flop président à ces modifications. Le bourgeon se referme sur lui-même et est « ligaturé » par une protéine également issue du cytosquelette, la dynamine. L’ensemble constitue alors une structure en forme de cage à maille hexagonale constituée en particulier de clathrine enfermant les LDL, et qui est désormais internalisée sous forme de vésicule d'endocytose qui migre dans le cytoplasme. L’ensemble de ce processus exige une dépense d’énergie, en particulier la consommation de guanosine triphosphate (GTP) et non d’adénosine triphosphate (ATP). Dans les endosomes, la clathrine est détachée de la vésicule par un mécanisme qui exige également de l'énergie, puis recyclée. Le contenu de la vésicule s’acidifie alors sous l'effet d'une pompe à protons membranaire, ce qui amène à la dissociation du complexe récepteur-ligand. Les récepteurs se concentrent dans une sorte de bourgeon de la vésicule qui va se détacher et retourner à la membrane plasmique : la plus grande partie de ces récepteurs est ainsi recyclée. Les types de clathrine et d’adaptine déterminent la destination de la vésicule dans la cellule. Le ligand va de ce fait subir un destin variable. La vésicule d'endocytose qui les contient fusionne avec d'autres vésicules spécialisées qui ont bourgeonné à partir du trans-Golgi, les endosomes. La dégradation des ligands s’opère dans la vésicule résultante, appelée lysosome. Le cholestérol, par exemple, libéré de son transporteur, sera utilisé pour la production des membranes. Dans un autre exemple, le fer lié à la transferrine sera libéré par dégradation de la protéine porteuse. Les bactéries et de nombreuses protéines étrangères captées par des anticorps seront dégradées par des jeux d'enzymes. L’ADN ou l’ARN d’un virus est libéré, etc.
Il existe d’autres types d’endocytose sans interaction spécifique ligand-récepteur préalable, comme les invaginations membranaires appelées cavéoles, mues par la polymérisation d’une protéine membranaire cytoplasmique, la cavéoline. Les vésicules ainsi formées rejoignent la voie endocytaire. Les cavéoles jouent des rôles importants dans la physiologie des muscles.
Exocytose
L’exocytose correspond au mouvement inverse, la manière dont une macromolécule synthétisée dans la cellule est sécrétée, ou intégrée dans la membrane cellulaire.
La synthèse des protéines membranaires et des protéines sécrétées est ici l’exemple de la complexité des mouvements membranaires dans l’exocytose. La présence de la séquence hydrophobe qui permet l’insertion de protéines dans la membrane interdit leur synthèse directe dans le cytoplasme : elles y seraient insolubles, mal formées et dégradées. Elles sont produites au contact d’une membrane intracellulaire, le réticulum endoplasmique. La machinerie habituelle de synthèse des protéines est accolée au réticulum endoplasmique. Les « grains de Palade », observés par ce célèbre microscopiste des années 1950, sont des ribosomes qui assurent la synthèse des protéines. Lorsque la traduction de l’ARN messager fait apparaître, au début du processus, une séquence d'acides aminés hydrophobes, celle-ci est bloquée par un adaptateur de la membrane réticulaire, et le complexe est ensuite reconnu par une structure protéique formant un pore qui traverse cette membrane. La synthèse se poursuit, la protéine naissante est injectée dans la lumière du réticulum endoplasmique. La courte séquence initiale d’adressage, appelée séquence signal, est clivée au niveau du premier acide aminé hydrophile. La synthèse se poursuit avec l’édification de ce qui sera la partie extracellulaire de la protéine membranaire. La future séquence transmembranaire reste bloquée dans la membrane du réticulum au moment de sa synthèse, cette dernière se terminant sur la face cytoplasmique : la future protéine membranaire est ainsi dans sa bonne position, insérée dans la membrane. Si la protéine est destinée à être sécrétée, elle s’accumule dans la lumière du réticulum. Lorsque la synthèse est terminée, le réticulum relargue des vésicules membranaires qui fusionnent avec une proche structure membranaire en forme de sacs plats empilés, l'appareil de Golgi. Ce dernier fonctionne comme une véritable plate-forme de tri, d’adressage vers la destination finale de la protéine. Il est également d’une certaine manière organisateur du cytosquelette. Au cours de son transfert de sac en sac vers le plus éloigné, appelé trans-Golgi, la protéine est modifiée, en particulier par addition de sucres complexes au niveau de séquences d'acides aminés acceptrices. Dans le trans-Golgi, qui fonctionne comme une véritable gare de triage, les vésicules contenant le matériel néosynthétisé reçoivent leur billet pour trois destinations principales : certaines deviendront des vésicules sécrétoires, qui fusionneront avec la membrane et libéreront leur matériel à l'extérieur. D'autres fusionneront avec la membrane qui intégrera alors ces nouvelles protéines membranaires. D'autres enfin migreront vers les lysosomes. Des systèmes différents, mais également fondés sur l'hydrophobicité d’une partie de la protéine, permettent l'adressage spécifique des protéines vers d’autres membranes, en particulier celles des organites (mitochondries, chloroplastes des cellules végétales, noyau), leur destination finale. La substance sécrétée est relâchée dans le milieu extérieur, les protéines membranaires resteront insérées dans les produits de fusion.
Les mécanismes de fusion entre vésicules ne sont pas laissés au hasard de la rencontre entre deux phases lipidiques : les fusions sont spécifiques et sont assurées par l’interaction entre protéines de la membrane des vésicules, les v-SNARE (vesicular-soluble N-ethylmaleimide-sensitive-factor attachment protein receptor, et les protéines t-SNARE (t pour target), caractéristiques des types de membranes avec lesquelles elles vont fusionner. Les protéines SNARE, sont au nombre d'une quarantaine, chacune assurant un type de fusion donné. Lorsqu’une v-SNARE reconnaît son récepteur t-SNARE, les deux protéines s’associent fortement et la fusion des membranes s’opère au prix d’un remaniement important des lipides des deux types de membranes, dans lesquels les mécanismes flip-flop et scramblase opèrent.
D’autres processus d'endocytose et d'exocytose existent, mais conservent les mêmes principes d’interaction entre membranes. La migration des protéines membranaires, sécrétées ou « endocytées », est donc une affaire de successions d'adressages, les adresses étant lues par des « lecteurs biologiques ». La migration correcte des vésicules membranaires sur le chemin de leur destination finale n'est donc pas laissée au hasard. Le cytosquelette – fibres d'actine, microfilaments, microtubules et filaments intermédiaires –, en association avec de véritables moteurs moléculaires, détermine le mouvement des vésicules vers l’étape suivante. Enfin, un ensemble d’au moins 70 protéines GTPases, membranaires, les protéines RAB, semblables mais différentes dans leur fonction d’adressage des éléments des diverses membranes, coordonnent finement ce processus de mouvements vers une localisation précise dans la cellule. RAB7, par exemple, identifie les lysosomes, ce qui permet leur reconnaissance par les endosomes tardifs, issus de l’endocytose. Ainsi, la migration des vésicules n'est ni libre ni aléatoire ; elle est contrainte par leur association avec le cytosquelette, véritable réseau de communication du trafic cellulaire.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Gabriel GACHELIN : chercheur en histoire des sciences, université Paris VII-Denis-Diderot, ancien chef de service à l'Institut Pasteur
Classification
Médias
Autres références
-
MITOSE
- Écrit par Nina FAVARD
- 6 522 mots
- 5 médias
...Chez les cellules animales, la cytodiérèse se fait par étranglement du cytoplasme de la cellule mère (fig. 7). Au milieu ou à la fin de l'anaphase, la membrane plasmique s'invagine tout autour de la cellule selon un plan correspondant à la région équatoriale du fuseau. Le sillon circulaire ainsi formé... -
ABSORPTION VÉGÉTALE
- Écrit par René HELLER et Jean-Pierre RONA
- 4 441 mots
- 6 médias
Labicouche phospholipidique des membranes des cellules végétales (plasmalemme et tonoplaste) est peu perméable à l'eau et à la plupart des ions minéraux, mais leur vitesse de diffusion et la sélectivité vis-à-vis des ions peuvent être augmentées par la présence de canaux (ions, eau) et de transporteurs... -
AQUAPORINES
- Écrit par Pierre LASZLO
- 2 344 mots
Lescellules sont encloses dans une membrane, faite d'une bicouche lipidique, qui enferme le cytoplasme, avec ses organelles et inclusions. Sur la face externe de la membrane, se trouve une autre solution aqueuse, contenant, de même d'ailleurs que le cytoplasme, des ions tels que sodium, potassium, ammonium,... -
ARCHÉOBACTÉRIES ou ARCHÉES
- Écrit par Patrick FORTERRE
- 2 138 mots
...les séquences des ARNr 16S d'archées étaient pratiquement aussi éloignées des séquences des ARNr 16S bactériens que de celles des ARNr 18S eucaryotes. L'originalité des archées a été rapidement confirmée par l'analyse de leurs glycérolipides membranaires. Alors que les glycérolipides des bactéries et... - Afficher les 49 références
Voir aussi
- INTESTIN
- RÉTICULUM ENDOPLASMIQUE
- GOLGI APPAREIL DE
- MEMBRANE PLASMIQUE ou PLASMALEMME
- PINOCYTOSE
- TRAFIC INTRACELLULAIRE
- PEPTIDE SIGNAL, cytologie
- IMMUNITAIRE SYSTÈME
- AMPHIPHILE MOLÉCULE
- PROTÉINES MEMBRANAIRES
- LIPIDES MEMBRANAIRES
- INTERNALISATION, biologie
- SODIUM, biologie
- POTASSIUM, biologie
- RÉGULATION BIOLOGIQUE
- GLYCOSPHINGOLIPIDES
- MEMBRANES BIOLOGIQUES
- PHOSPHOLIPIDES
- ORGANITES CELLULAIRES
- ANTICORPS
- MODÈLE, biologie
- PROTÉINES BIOSYNTHÈSE DES
- SPHINGOLIPIDES
- PERMÉABILITÉ, physiologie cellulaire
- CYTOLOGIE ou BIOLOGIE CELLULAIRE
- MOSAÏQUE FLUIDE MODÈLE EN
- MESSAGER, biochimie
- GLYCOLIPIDES
- GLYCOPROTÉINES
- RECONNAISSANCE, biologie
- EXOCYTOSE
- RECONNAISSANCE, immunologie
- SINGER SEYMOUR JONATHAN (1924- )
- HYDROPHOBICITÉ, chimie
- ENDOSOME
- RÉCEPTEURS MEMBRANAIRES
- LDL (low density lipoproteins)
- CYTOSQUELETTE
- CLATHRINE
- RÉCEPTEUR, biochimie
- TRANSDUCTION MEMBRANAIRE
- LIPID RAFT ou RADEAU LIPIDIQUE
- ENDOCYTOSE À RÉCEPTEURS
- ADRESSAGE DES PROTÉINES