MICROBIOLOGIE
Article modifié le
La microbiologie environnementale
Micro-organismes des milieux naturels
Les micro-organismes occupent sur notre planète l'ensemble d'une sphère irrégulière qui comprend une fraction de la croûte terrestre, la totalité de la masse aqueuse et l'atmosphère. Cette colonisation de tous les sites de la biosphère, sans exception, est due à une extraordinaire adaptabilité à la fois génotypique et phénotypique des micro-organismes aux stress physico-chimiques. Ainsi, des milieux aux conditions extrêmes sont occupés tels que les glaciers, les fontaines hydrothermales, les milieux maritimes, y compris les abysses ou les marais salants. Les milieux naturels ont fourni de nombreuses souches microbiennes productrices d’antibiotiques.
Par ailleurs, la maîtrise de la qualité de l'environnement peut être améliorée en utilisant certains micro-organismes pour biodégrader des produits toxiques issus de l'activité humaine tels que le toluène (par exemple, Pseudomonas putida).
Ils sont, plus généralement, très utiles dans les opérations de décontamination. Leur rôle dans le traitement des effluents ménagers est mis à profit dans l'assainissement des eaux usées (cf. eau - Approvisionnement et traitement). En revanche, ils peuvent participer à des phénomènes de détérioration (« maladie » des pierres) des monuments ou constituer des enduits nocifs, appelés biofilms, à la surface des installations urbaines ou industrielles.
Biofilms
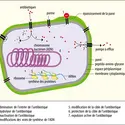
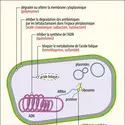
Dans la nature, les biofilms sont des populations de micro-organismes intimement associées à des surfaces vivantes ou minérales par l'intermédiaire d'une substance muqueuse composée d'eau et de polymères biologiques (sucres, protéines, ADN, acides humiques). Ils sont présents partout : sur le tronc des arbres ou les galets du fond d'une rivière, mais aussi sur la coque des bateaux, à l'intérieur des tuyauteries de distribution d'eau ou des radiateurs de chauffage central, et même dans notre bouche et sur nos gencives, où ils forment la plaque dentaire.
Depuis les années 1990, les microbiologistes ont pris conscience que la réalisation du biofilm constitue en fait le mode de vie de l'immense majorité des organismes unicellulaires et que cela oblige à reconsidérer leur physiologie, jusque-là principalement étudiée en cultures pures dans des récipients de laboratoire. Il est ainsi apparu que, lorsque des microbes vivent groupés dans des communautés comme les biofilms, bon nombre de leurs propriétés diffèrent radicalement de celles des mêmes cellules nageant ou flottant individuellement au sein d'une phase liquide. Et l'une des caractéristiques les plus inquiétantes que ces organismes acquièrent en biofilm est une nette augmentation des résistances aux agents antimicrobiens, aux détergents et aux défenses immunitaires. C'est la cause de plus de la moitié des infections nosocomiales, ces maladies contractées en milieu hospitalier et qui tuent plus de dix mille patients chaque année en France. La contamination des produits à partir d'installations colonisées par des germes pathogènes est également une hantise quotidienne dans de nombreux secteurs industriels, comme l'agro-alimentaire, la pharmacie, les cosmétiques et la papeterie.
Les biofilms sont chaque année dans le monde la cause du décès de dizaines de milliers de personnes, à la suite d'infections contractées lors d'interventions chirurgicales, d'hospitalisations ou de traitements médicaux. Dans l'immense majorité des cas, ces infections sont le résultat de la colonisation de cathéters intravasculaires ou de sondes urinaires qui restent au contact de la peau du malade et du milieu extérieur. Des biomatériaux posés à demeure, comme les prothèses de hanche, les cristallins artificiels ou les stimulateurs cardiaques, peuvent également être contaminés lors de leur mise en place. De nombreux exemples de septicémies dues au développement du staphylocoque doré à la surface d'implants ont été rapportés. Dans le biofilm, les bactéries sont à l'abri des antibiotiques et des défenses immunitaires. Des traitements parfois très lourds par des antibiotiques à staphylocoques ne sont actifs que sur les bactéries qui se détachent et parviennent dans le flot sanguin. Dès que le traitement cesse, la septicémie reprend, car le biofilm sert de réservoir. Le retrait de l'implant est généralement la seule solution efficace.
Toutes les surfaces des couloirs des hôpitaux et des chambres des malades peuvent être colonisées par des germes pathogènes. C'est également le cas des systèmes d'aération et de distribution d'eau ainsi que des installations de climatisation (où les légionelles trouvent un terrain favorable). La vie en biofilms confère à ces organismes un haut niveau de résistance aux procédures de désinfection, ce qui expose la population affaiblie que constituent les malades hospitalisés à un risque élevé d'infections. Rien qu'aux États-Unis, le surcoût médical des maladies dont les biofilms sont la source est estimé à plus de 1 milliard de dollars par an et il demande pratiquement de repenser toute l'hygiène des établissements de soin.
Comme il n'existe aucun moyen d'empêcher l'adhérence des bactéries aux surfaces, la contamination microbienne des biomatériaux en contact avec le sang est actuellement le frein technologique majeur au développement et à la généralisation de bon nombre de dispositifs médicaux, comme les cœurs et les reins artificiels.
En dehors du domaine médical, le coût des biofilms est aussi très lourd. Sur toute surface industrielle de production ou de conditionnement en contact avec de l'eau (ou de l'air humide) et un minimum de matières organiques se développe un biofilm très difficile à éradiquer par des méthodes de nettoyage conventionnelles. Il en va de même des tuyauteries, où la matrice qui englobe les cellules peut se charger de sels minéraux et conduire à un entartrage capable d'obstruer complètement les conduits. Ces proliférations de micro-organismes non seulement peuvent endommager gravement les installations industrielles – on parle alors de « biodétérioration » – mais sont évidemment aussi très préjudiciables pour la qualité des produits et des effluents : les contaminations des aliments par des salmonelles et des Listeria et celles des tours de refroidissement par les légionelles ont presque toujours un biofilm pour origine. Au niveau planétaire, le coût annuel des biodétériorations industrielles, des pertes de production et des procédures particulières de décontamination est estimé à plusieurs milliards d'euros.
Des sommes équivalentes sont dépensées dans le domaine maritime, où les biofilms microbiens qui se développent en quelques jours sur tout matériau immergé permettent l'ancrage de nombreux organismes macroscopiques tels que moules, algues et coquillages. Un film de quelques dizaines de micromètres d'épaisseur suffit à perturber les propriétés hydrodynamiques d'un navire au point d'augmenter significativement la facture énergétique nécessaire à sa propulsion. Lorsque le biofilm gagne en épaisseur et donne lieu à la fixation d'êtres pluricellulaires, les processus de corrosion et les pertes d'énergie rendent l'immobilisation du bateau et le nettoyage de sa coque obligatoires.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Corinne DOREL : maître de conférences à l'Institut national des sciences appliquées de Lyon
- Philippe LEJEUNE : professeur à l'Institut national des sciences appliquées de Lyon
- Jean-Michel PANOFF : biologiste, professeur à l'université de Caen Basse-Normandie
Classification
Médias
Autres références
-
ALIMENTATION (Aliments) - Risques alimentaires
- Écrit par Jean-Pierre RUASSE
- 4 759 mots
- 1 média
...cas de germes parasitaires : ascaris, ténias, douves, trichines dont la présence dans certains aliments nécessite un dépistage préventif systématique. Quant aux éléments microbiens et viraux, ils peuvent rendre l'aliment dangereux par trois mécanismes essentiels : la prolifération, la toxinogenèse et... -
AMMONIFICATION ou AMMONISATION
- Écrit par Didier LAVERGNE
- 1 920 mots
- 1 média
...fait est démontré par la sensibilité du phénomène vis-à-vis des facteurs qui limitent la vie (ex. température, aération, humidité) et par l'isolement des germes responsables. La propriété de détacher la fonction amine des aminoacides, issus de l'hydrolyse des protéines, est d'ailleurs une faculté métabolique... -
ANTIBIORÉSISTANCE
- Écrit par Aurélie CHABAUD , Sylvain MEYER et Marie-Cécile PLOY
- 5 907 mots
- 4 médias
Les antibiotiques sont des molécules naturellement produites par des bactéries ou des champignons, et qui contribuent à l’équilibre entre populations de micro-organismes au sein d’une niche écologique. L’utilisation d’antibiotiques pour prévenir ou traiter une infection, pour accélérer la croissance...
-
ANTIBIOTIQUES
- Écrit par Aurélie CHABAUD , Sylvain MEYER et Marie-Cécile PLOY
- 6 760 mots
- 6 médias
Au début des années 1940, le microbiologiste américain Selman A. Waksman, découvreur de nombreux antibiotiques dont la streptomycine – ce qui lui valut le prix Nobel de médecine en 1952 –, définit un antibiotique comme une substance chimique, produite par un micro-organisme, qui inhibe la croissance...
- Afficher les 73 références
Voir aussi
- CONTAMINATION
- MICRO-ORGANISME
- DEUTÉROMYCÈTES
- HYPHES
- EUCARYOTES
- MOISISSURES
- INFECTION
- RÉSISTANCE, biologie
- HÔPITAL
- BIOFILMS
- PROTOZOAIRES
- PROCARYOTES ou PROTOCARYOTES
- AGROALIMENTAIRE TECHNOLOGIE
- UNICELLULAIRES
- ALIMENTS
- GERMES, biologie
- BIOMATÉRIAUX
- PAROI CELLULAIRE
- IMPLANT, médecine
- EUBACTÉRIES
- BIOLOGIE HISTOIRE DE LA
- AGENTS PROBIOTIQUES