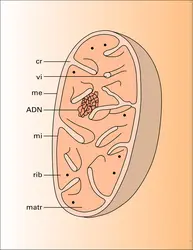
MITOCHONDRIES
Fonctions mitochondriales
Les oxydoréductions biologiques
Les différentes formes de l'énergie libre dans une cellule
L' énergie libre (ou enthalpie libre) est, par définition, l'énergie que l'on peut récupérer sous forme de travail. Elle est donnée par l'équation générale du second principe de la thermodynamique :

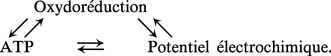
L'énergie d'oxydoréduction
La plupart des réactions chimiques rencontrées dans les cellules sont des réactions d'oxydoréduction. Par définition, une réaction d'oxydoréduction est constituée de deux couples oxydoréducteurs pouvant exister dans leur forme réduite et leur forme oxydée :

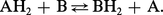
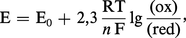
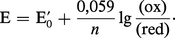
C'est une convention, en biologie, de donner une valeur négative aux couples plus réducteurs que le couple H2/2H+ à pH = 0, et une valeur positive aux couples qui le sont moins. Le tableau 2 donne les valeurs de E′0 de quelques-uns des couples les plus importants rencontrés dans les cellules. Les couples les plus réducteurs sont des couples comme celui du glycérate, impliqué dans la glycolyse cytoplasmique, ou celui de la ferrédoxine, un des transporteurs d'électrons les plus importants de la photosynthèse dans les chloroplastes des cellules végétales. Le couple le plus oxydant est celui de O2/H2O. À partir des valeurs de E′0, on peut calculer la variation d'énergie libre standard ΔG′0 résultant d'une réaction d'oxydoréduction en appliquant la relation :

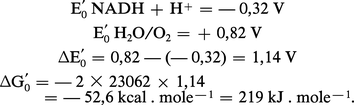
Mitochondrie et chloroplaste dans le cycle énergétique
Respiration et photosynthèse sont des phénomènes biologiques caractéristiques de la nutrition cellulaire mais thermodynamiquement tout à fait opposés.
Dans la mitochondrie, le transit des H+ et des électrons se fait, normalement, des couples les plus réducteurs vers le couple le plus oxydant, celui de l'oxygène.[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Roger DURAND : professeur de biochimie à l'université Blaise-Pascal, Clermont-Ferrand
Classification
Médias
Autres références
-
AÉROBIOSE & ANAÉROBIOSE
- Écrit par Claude LIORET
- 2 736 mots
- 1 média
...moins que les levures situées en surface (levures hautes), donc au contact de l'oxygène. On a montré que, cultivées en anaérobiose, elles possédaient des mitochondries extrêmement peu développées et que les activités de leurs enzymes d'oxydo-réduction respiratoire, en particulier de la cytochrome-oxydase,... -
BIOSYNTHÈSE DE L'ATP
- Écrit par Paul MAZLIAK
- 240 mots
La théorie émise par Peter Mitchell (1920-1992), qu'il baptisa théorie chimiosmotique, bouleversa la bioénergétique. Jusqu'alors, on considérait que l'oxydation des substrats respiratoires dans les mitochondries était couplée avec la synthèse endergonique (consommatrice...
-
CELLULE - L'organisation
- Écrit par Pierre FAVARD
- 11 031 mots
- 15 médias
Lesmitochondries représentent un dernier type d'organite cytoplasmique à structure membranaire. Au nombre d'une centaine dispersées dans le cytosol, les mitochondries du fibroblaste ont la forme de bâtonnets cylindriques aux extrémités arrondies dont le diamètre est de 0,5 μm et la longueur... -
CELLULE - La division
- Écrit par Marguerite PICARD
- 4 983 mots
- 3 médias
En ce qui concerne les organites cellulaires porteurs d' information génétique (mitochondries de toutes les cellules, plastes des cellules végétales), la réplication de leur ADN n'est pas synchrone avec celle de l'ADN nucléaire. Elle peut être continue pendant tout le cycle cellulaire (c'est le... - Afficher les 28 références