MITOCHONDRIES
Article modifié le
La continuité mitochondriale
Les mitochondries se reproduisent-elles par croissance et division ou bien par synthèse de novo ? On sait maintenant qu'elles se reproduisent par croissance de cet organite par suite de la synthèse coordonnée de ses constituants moléculaires. À partir d'un certain volume mitochondrial, il y a coupure de la membrane interne, formation de deux vésicules matricielles et segmentation de la membrane externe qui clôt et sépare les deux vésicules précédemment formées. La masse mitochondriale double à chaque mitose.
Cette continuité physique des mitochondries a été tout d'abord démontrée avec les phospholipides des membranes. Des mutants de Neurospora crassa, auxotrophes pour la choline indispensable à la synthèse de phosphatidylcholine, ont des mitochondries plus denses quand les cellules sont cultivées en absence de choline. L'addition de choline ne s'accompagne pas de la synthèse d'une nouvelle population de mitochondries moins dense, mais de la diminution progressive de densité de la population initiale des organelles. La continuité de la biogenèse des protéines se manifeste aussi par la transformation des promitochondries des levures cultivées en anaérobiose en mitochondries effectives, à la suite de l'addition d'oxygène dans le système de culture des levures.
La biogenèse des mitochondries est un phénomène complexe mettant en jeu le génome nucléaire et le génome propre à la mitochondrie. La coordination de leur activité ne met pas en cause cependant l'autonomie fonctionnelle de ce dernier, comme le prouvent les observations qui précèdent. C'est pourquoi il est possible de postuler l'existence d'une continuité génétique mitochondriale propre à chaque espèce. Les différences génomiques mitochondriales pourraient alors servir à analyser les relations évolutives entre espèces voisines pour reconstituer leur hypothétique phylogenèse (comme on s'est efforcé de le faire en paléoanthropologie avec la théorie de l'« Ève africaine »).
Le génome mitochondrial : structure et fonction
Toutes les mitochondries ont leur propre génome : il ne comporte – comme celui des Procaryotes, auxquels les mitochondries sont peut-être apparentées (selon la théorie dite symbiotique de l'origine des cellules encaryotes) – que de l'ADN bicaténaire, circulaire, sauf exception où il est linéaire. Toutes les séquences sont identiques pour un même organisme.
Structure
La taille de ces molécules d'ADN est relativement uniforme dans le règne animal et est caractéristique de l'espèce : 16 569 paires de bases pour l'ADN mitochondrial humain, 17 400 pour Xenopus laevis, de 15 700 à 19 500 pour la Drosophile. L'ADN mitochondrial de levures a environ 75 000 paires de bases. Le génome mitochondrial des plantes peut être de 20 à 30 fois plus grand que le génome de levure. Il comporte, comme celui des levures, des gènes dispersés dans des zones non codantes riches en adénine et thymine ou guanine et cytosine.
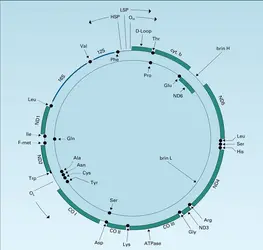
La séquence complète du génome mitochondrial humain a été publiée (Nature, avr. 1981). L'organisation de ce génome est tout à fait remarquable (fig. 13). Les gènes codant pour les 2 ARN ribosomaux, 22 ARN de transfert et 13 protéines sont tellement serrés qu'il n'y a pratiquement pas de bases non codantes entre eux. Quelques codons ne sont pas conformes au code génétique universel : UGA, qui est un codon d'arrêt dans la synthèse qui s'accomplit dans les ribosomes cytoplasmiques, code pour le tryptophane dans les mitochondries ; AGA et AGG, qui codent habituellement pour l'arginine, sont des codons d'arrêt dans les mitochondries.
Les mutants mitochondriaux de levures
Vers les années 1946-1948, Boris Ephrussi observait qu'une culture de levure diploïde ou haploïde donne après repiquage, dans les quelques jours qui suivent, une colonie identique aux cellules mères sauf, dans quelques cas, 1 à 2 p. 100 de cellules plus petites. Les mutants « petite colonie » ne donnent que des petites colonies. La mutation est irréversible. Le traitement des cellules de la souche sauvage par l'acriflavine fait passer le taux de mutation de 1-2 p. 100 à 100 p. 100. Ces mutants poussent lentement car ils ne peuvent respirer, leur métabolisme est uniquement fermentaire, ils ont perdu la capacité de synthétiser un certain nombre d'enzymes respiratoires, dont la cytochrome oxydase. Le croisement de la souche sauvage avec les mutants « petites colonies » montre une ségrégation non mendélienne de la mutation. Après toutes ces observations, Ephrussi devait arriver à la conclusion que la souche sauvage et les mutants « petites colonies » diffèrent par l'absence, dans le dernier cas, d'unités cytoplasmiques requises génétiquement pour la synthèse de certains enzymes respiratoires. À une époque où les mitochondries venaient à peine d'être reconnues, en tant qu'organites, par la microscopie électronique et par la cytophysiologie, c'était l'acte de naissance de la génétique mitochondriale. En 1968, on devait démontrer que la mutation « petite colonie » est due à une altération importante de l'ADN mitochondrial.
Les mutants « petites colonies » constituent les souches ρ—. Leur quantité d'ADN mitochondrial est identique à celle des souches sauvages désignées par ρ+ (des mutants ρ0 existent, ils ont perdu totalement leur ADN mitochondrial).
Les mutants ρ— ne sont pas les seuls mutants mitochondriaux. De nombreuses mutations avec résistance aux antibiotiques ont été identifiées, elles affectent des sites d'inhibition très divers : les ribosomes (mutants résistant au chloramphénicol par exemple), l'ATP synthétase (mutants résistant à l'oligomycine), le complexe III de la chaîne respiratoire (mutants résistant à l'antimycine). Des mutations peuvent enfin intervenir dans les gènes qui codent pour les composants indispensables à la synthèse protéique mitochondriale ( ARN ribosomaux et de transfert) : ce sont les mutants syn—. Dans le cas où ce sont les gènes codant pour les protéines synthétisées dans les mitochondries qui sont affectés, ce sont les mutants mit—.
Ces mutants ont été très précieux. En combinant techniques génétiques d'établissement des cartes génomiques et analyse séquentielle des fragments de restriction de l'ADN mitochondrial des mutants, ils ont permis de localiser les gènes.
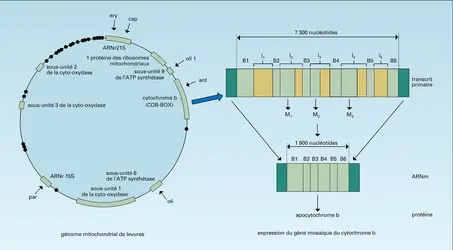
Le génome mitochondrial de levure se caractérise non seulement par une dispersion des gènes connus dans de vastes zones non codantes mais aussi par une structure en mosaïque avec exons et introns dans certains gènes (ceux de l'ARNr 21 S, de la sous-unité 1 de la cytochrome oxydase, de l'apocytochrome b). Les exons codent pour des parties de la protéine et vont s'associer pour constituer l' ARNm qui sera traduit dans le cytoplasme ; les introns sont constitués de séquences codantes et/ou de séquences non codantes : les séquences codantes des introns contrôlent la synthèse d'enzymes, les maturases, qui interviennent dans l'excision et l' épissage des exons à partir du transcrit primaire. Ce résultat remarquable a été obtenu dans le laboratoire de Piotr Slonimski à Gif-sur-Yvette.
Les interrelations entre génome nucléaire et génome mitochondrial
Des systèmes multienzymatiques comme la cytochrome oxydase, l'ATP synthétase ont des sous-unités protéiques codées par le génome nucléaire et d'autres par le génome mitochondrial. Comment sont coordonnées les synthèses entre les deux génomes ? Comment se fait l'assemblage dans la membrane entre les deux types de sous-unités ?
Là encore, les études faites avec les levures ont permis d'apporter des éléments de réponse. Outre les mutants mitochondriaux obtenus avec ces organismes, on peut trouver des mutants nucléaires chez lesquels sont affectés des gènes codant pour les protéines mitochondriales. Des mutants nucléaires ont été obtenus par exemple pour des protéines de la chaîne respiratoire, de l'ATP synthétase, des enzymes catalysant la synthèse du noyau hémique des cytochromes. Le très grand nombre de mutants isolés a permis d'estimer à au moins 1 000 le nombre de gènes nucléaires impliqués dans la biogenèse des mitochondries. On connaît par exemple des mutants nucléaires de levure qui n'ont pas de sous-unité 2 ou de sous-unité 3 de la cytochrome oxydase que code pourtant le génome mitochondrial : des protéines synthétisées dans le cytoplasme moduleraient par conséquent l' expression du génome mitochondrial.
Le contrôle étroit du génome nucléaire sur l'expression du génome mitochondrial ne fait aucun doute. Une autre question peut cependant se poser : l'expression du génome mitochondrial module-t-elle l'activité des gènes nucléaires codant pour des protéines mitochondriales ? Pour vérifier cette hypothèse on peut par exemple inhiber la synthèse mitochondriale par le chloramphénicol dans des cellules de levures et voir ce qui se passe quant à la biogenèse des protéines mitochondriales codées par le génome nucléaire (sous-unités 4, 5, 6 et 7 de la cytochrome oxydase). Une situation analogue est celle des mutants « petites colonies » ρ—. On constate que, dans les deux cas, des protéines mitochondriales s'accumulent soit dans le cytoplasme soit sur la membrane de l'organite, mais sans que ces protéines s'intègrent à celle-ci. La synthèse mitochondriale serait donc essentielle pour l'insertion des protéines dans la membrane.
Génome mitochondrial humain
Organisation
Le génome mitochondrial humain est très semblable à celui des mammifères supérieurs (souris, bœuf). C'est une molécule d'ADN double brin de 16 569 paires de base. Il se caractérise par une extrême compacité : tout l'ADN est codant à l'exception de la zone contenant les origines de transcription, l'origine de réplication de l'un des brins et la boucle de déplacement (D loop). Il n'y a pas de zones non codantes entre les gènes, pas d'introns à l'intérieur des gènes et certains gènes se chevauchent (gènes ATPase 8 et ATPase 6, gènes ND4 et ND4L). Certains gènes n'ont même pas de codon d'arrêt complet. Tous les gènes sont identifiés : 2 ARNr, 22 ARNt et 13 gènes codants pour des protéines appartenant aux complexes I, III et IV de la chaîne respiratoire et à l'ATP synthétase (tabl. 5). Le code génétique présente quelques exceptions dans les mitochondries, et ces exceptions diffèrent d'un type de mitochondrie à l'autre (tabl. 6). Cela a probablement constitué un avantage sélectif qui a permis aux mitochondries de maintenir leur autonomie génétique au sein de la cellule.
Expression
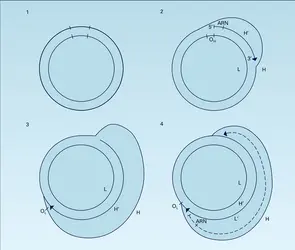
La réplication de l'ADNmt se fait en continu tout au long du cycle cellulaire. Elle est catalysée par l'ADN polymérase γ, qui est une protéine d'origine nucléaire et qui intervient spécifiquement dans les mitochondries. La synthèse d'un nouveau brin H se fait en utilisant le brin L comme matrice. Son origine de réplication se trouve dans la zone de la boucle de déplacement. Cette synthèse s'effectue de façon unidirectionnelle, dans le sens des aiguilles d'une montre. Elle s'arrête lorsque la zone de l'origine de réplication du brin L est atteinte, et commence alors la synthèse du nouveau brin L pendant que se termine celle du nouveau brin H.
La transcription est catalysée par une ARN polymérase spécifique des mitochondries et d'origine nucléaire sur le plan génétique. Il y a synthèse de trois transcrits primaires : le transcrit de la totalité du brin L, qui sera ensuite clivé en ARNt et ARNm de ND6, un transcrit du brin H couvrant les ARNr et les ARNt phe ala et val, un transcrit du brin H couvrant l'ensemble des gènes de ce brin. Il y a une inégalité transcriptionnelle pour le brin H : la transcription des gènes ribosomaux est environ de quinze à soixante fois plus importante que celle des autres gènes. Les ARNm résultant du clivage des transcrits primaires ont des durées de vie variables : la demi-vie de l'ARNm du gène ND6 est de 7 minutes alors que les ARNm du brin H ont des demi-vies allant de 25 à 90 minutes.
La traduction des ARNm mitochondriaux en protéines se fait dans la matrice. Les 22 ARNt sont suffisants pour cette traduction. Les acides aminés et toutes les protéines indispensables à la traduction viennent du cytoplasme.
Les mutations et leurs conséquences pathologiques
L'ADNmt est particulièrement sensible aux agents mutagènes (de dix à vingt fois plus que l'ADN nucléaire). Il est peu protégé par des protéines et la matrice mitochondriale accumule facilement les cations ou anions mutagènes en raison de la présence du gradient de potentiel électrochimique de part et d'autre de la membrane interne. Par ailleurs, les accidents survenant au moment de la réplication peuvent difficilement être réparés, aucun système de réparation n'ayant été mis en évidence.
Les myopathies ou cytopathies mitochondriales résultant des mutations sont à hérédité maternelle, puisque seule la mère (en principe) transmet à sa descendance son stock mitochondrial présent dans l'ovocyte. On constate généralement dans la descendance un phénomène d'hétéroplasmie se traduisant dans les cellules par un certain pourcentage d'ADNmt muté coexistant avec de l'ADNmt normal. La pathologie est généralement d'autant plus marquée que cette proportion est élevée.
Les mutations ponctuelles affectent un seul nucléotide. Cela peut être le cas d'un gène d'une protéine impliquée dans les phosphorylations oxydatives. Dans la maladie de Leber (neuropathie optique héréditaire), caractérisée par la perte rapide bilatérale de la vision centrale après la puberté, il a pu être découvert, au moins dans deux tiers des cas, une mutation ponctuelle entraînant le remplacement d'une arginine par une histidine dans la protéine ND4 du complexe I.
Dans le cas de l'épilepsie myoclonique avec fibres rouges en lambeaux (MERRF), se traduisant par des anomalies dans les réponses visuelles et à l'électroencéphalogramme dans les cas les plus légers, on a pu détecter une mutation ponctuelle dans le gène codant pour l'ARNt lysine. La synthèse des protéines est ainsi affectée, surtout celle des protéines comme ND1, ND2, ND5, riches en lysine.
Le syndrome de Kearns-Sayre est caractérisé par une ophtalmoplégie externe progressive, une rétinite pigmentaire et des troubles de la conduction cardiaque. Il y a des fibres rouges en lambeaux dans le tissu musculaire. Ce syndrome est le plus souvent corrélé avec des délétions de l'ADNmt allant de 1,3 à 8,8 kb, soit, dans ce dernier cas, la moitié du génome mitochondrial. Les délétions sont souvent rencontrées entre les deux origines de réplication, là ou s'effectue la synthèse du nouveau brin H. Ces délétions vont ainsi affecter les gènes des complexes I, III ou IV, les gènes ATPase 6 et 8 selon la longueur de la délétion.
Protéogenèse
Les protéines cytoribosomales indispensables à la synthèse protéique mitochondriale
Tous les ARN messagers traduits dans la matrice mitochondriale sont codés par l'ADN mitochondrial. Il n'y a pas de transit d'ARN messagers nucléaires dans la matrice aux fins de traduction sur les ribosomes mitochondriaux.
Certaines protéines mitochondriales sont codées par l'ADN du noyau cellulaire, lequel s'exprime par des ARN messagers qui se lient aux ribosomes du cytoplasmes. Les protéines produites sont dites cytoribosomales. D'autres protéines mitochondriales sont formées à partir de l'information génétique fournie par l'ADN mitochondrial : elles sont dites mitoribosomales.
Or, la machinerie de la synthèse protéique mitochondriale exige un ensemble de protéines cytoribosomales. Les plus connues, à l'heure actuelle, sont celles entrant dans la structure des ribosomes, celles impliquées dans la réplication de l'ADN mitochondrial (ADN polymérase), la transcription (ARN polymérase), la traduction des ARNm (aminoacyl ARNt synthétases, facteurs d'initiation, facteur d'élongation, etc.).
L'origine traductionnelle des sous-unités protéiques
Certains complexes protéiques ont une dualité d'origine : tel est le cas de la cytochrome oxydase dans la levure (complexe IV de la chaîne respiratoire). Les sous-unités 1, 2 et 3, qui catalysent la réduction de l'oxygène et l'éjection de protons, sont mitoribosomales. Les sous-unités 4, 5, 6 et 7, qui jouent un rôle régulateur, sont cytoribosomales.
L'origine traductionnelle de chaque groupe de sous-unités a été facilitée par l'utilisation d'antibiotiques inhibiteurs spécifiques de la biosynthèse des protéines dans le cytoplasme et dans les mitochondries. La traduction cytoribosomale peut être inhibée par la cycloheximide qui bloque l'initiation et l'élongation des chaînes polypeptidiques. La traduction mitoribosomale peut être inhibée par le chloramphénicol qui agit en se fixant sur les ribosomes mitochondriaux.
La méthodologie suivie est simple. Des cellules de levure sont cultivées en présence de cycloheximide et d'un acide aminé radioactif, la méthionine-35S. Aucune incorporation de l'acide aminé ne sera décelée dans les protéines d'origine cytoribosomale, qu'elles soient cytoplasmiques ou mitochondriales. En revanche, si l'on isole les mitochondries et que l'on purifie les sous-unités 1, 2 et 3 par immunopurification, on constate qu'elles sont radioactives. Ce résultat montre qu'elles sont synthétisées dans les mitochondries. Une expérience semblable effectuée avec du chloramphénicol permet de démontrer que les sous-unités 4 à 7 sont cytoribosomales.
L'incorporation de méthionine-35S dans des mitochondries isolées confirme les résultats précédents. Dans ces conditions, seules les protéines mitoribosomales incorporent la méthionine-35S. Et cette incorporation est inhibée par le chloramphénicol.
La régulation de la synthèse mitoribosomale et cytoribosomale
La concentration de la cytochrome oxydase de levure est un phénomène très bien régulé. La croissance anaérobie, la répression catabolique par le glucose entraînent une perte de mitochondries pleinement différenciées et une perte d'activité cytochrome oxydase. Le phénomène est parfaitement réversible. A priori, deux types de régulation peuvent être envisagés : un effet des produits de la traduction mitochondriale sur la synthèse cytoplasmique des protéines mitochondriales et un effet des produits cytoribosomaux sur la synthèse mitoribosomale.
Il semble, à première vue, que la synthèse mitoribosomale ait peu d'effet sur la synthèse cytoribosomale des protéines mitochondriales. En absence de synthèse mitoribosomale, les protéines synthétisées dans le cytoplasme ne peuvent s'intégrer dans la membrane interne. La synthèse mitoribosomale serait donc seulement essentielle pour l'intégration des polypeptides dans la membrane.
En revanche, des produits cytoribosomaux peuvent exercer un effet sur la synthèse mitoribosomale. Le cytoplasme des cellules contient des éléments qui stimulent la synthèse mitoribosomale. De plus, on a pu montrer que des mutants nucléaires « petites » n'avaient pas de sous-unité 2 ou de sous-unité 3 de la cytochrome oxydase. Des mutations dans le génome nucléaire peuvent donc affecter la synthèse de polypeptides codés par l'ADN mitochondrial.
La synthèse des protéines mitochondriales cytoribosomales et leur transfert dans les mitochondries
La synthèse des polypeptides mitoribosomaux se fait probablement au voisinage de la face matricielle de la membrane interne des mitochondries. Les étapes de cette synthèse sont encore mal connues.
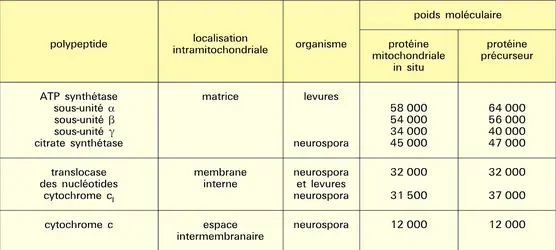
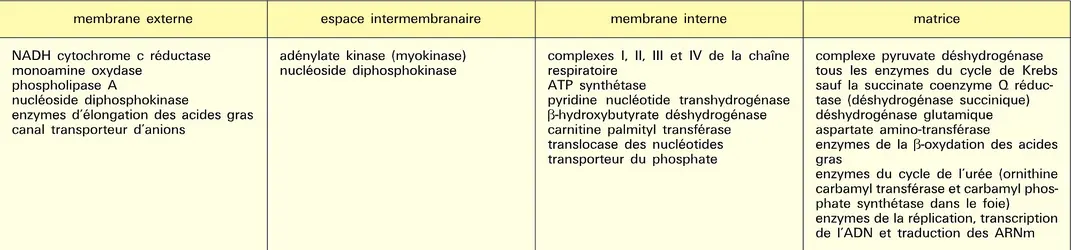
Les étapes de la synthèse des protéines mitochondriales cytoribosomales sont mieux élucidées. On a cru tout d'abord que l'intégration dans les membranes mitochondriales, voire la diffusion des protéines cytoribosomales dans la matrice, étaient un phénomène de type cotraductionnel comme celui démontré pour les membranes du réticulum endoplasmique. En fait, on sait maintenant que la plupart des protéines mitochondriales cytoribosomales (tabl. 4) sont synthétisées sous forme de protéine précurseur dont le poids moléculaire est plus élevé que celui des protéines matures. La protéine précurseur se fixe sur la membrane externe, probablement par l'intermédiaire de récepteur spécifique, puis diffuse dans la membrane interne selon un processus contrôlé par le potentiel électrochimique membranaire. Des enzymes protéolytiques présentes dans la matrice interviennent enfin pour couper une partie de l'extrémité N-terminale de la protéine. Il en résulte un changement de conformation qui facilite la mise en place de la protéine dans son environnement hydrophobe.
Ce processus a été bien étudié dans les mitochondries de levure pour les sous-unités α, β et γ de la composante F1 de l'ATP synthétase, de même que pour les sous-unités 4 à 7 de la cytochrome oxydase. Les protéines de la matrice, comme la carbamyl phosphate synthétase, sont synthétisées et transportées selon un processus identique. Dans certains cas, comme le cytochrome c1, la maturation se fait en deux étapes. La protéine précurseur (poids moléculaire 37 000) est tout d'abord transformée en protéine intermédiaire (poids moléculaire 35 000) sous l'action d'une protéase matricielle. Puis, une seconde coupure intervient du côté de la face matricielle pour transformer la protéine intermédiaire en cytochrome c1 (poids moléculaire 31 500). Cette seconde étape est catalysée par une autre protéase et exige que le noyau hémique soit fixé covalemment sur la protéine intermédiaire.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Roger DURAND : professeur de biochimie à l'université Blaise-Pascal, Clermont-Ferrand
Classification
Médias
Autres références
-
AÉROBIOSE & ANAÉROBIOSE
- Écrit par Claude LIORET
- 2 736 mots
- 1 média
...moins que les levures situées en surface (levures hautes), donc au contact de l'oxygène. On a montré que, cultivées en anaérobiose, elles possédaient des mitochondries extrêmement peu développées et que les activités de leurs enzymes d'oxydo-réduction respiratoire, en particulier de la cytochrome-oxydase,... -
BIOSYNTHÈSE DE L'ATP
- Écrit par Paul MAZLIAK
- 240 mots
La théorie émise par Peter Mitchell (1920-1992), qu'il baptisa théorie chimiosmotique, bouleversa la bioénergétique. Jusqu'alors, on considérait que l'oxydation des substrats respiratoires dans les mitochondries était couplée avec la synthèse endergonique (consommatrice...
-
CELLULE - L'organisation
- Écrit par Pierre FAVARD
- 11 031 mots
- 15 médias
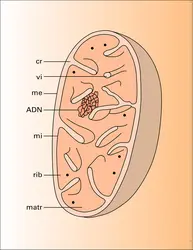
Lesmitochondries représentent un dernier type d'organite cytoplasmique à structure membranaire. Au nombre d'une centaine dispersées dans le cytosol, les mitochondries du fibroblaste ont la forme de bâtonnets cylindriques aux extrémités arrondies dont le diamètre est de 0,5 μm et la longueur... -
CELLULE - La division
- Écrit par Marguerite PICARD
- 4 983 mots
- 3 médias
En ce qui concerne les organites cellulaires porteurs d' information génétique (mitochondries de toutes les cellules, plastes des cellules végétales), la réplication de leur ADN n'est pas synchrone avec celle de l'ADN nucléaire. Elle peut être continue pendant tout le cycle cellulaire (c'est le... - Afficher les 28 références
Voir aussi
- ENZYMES
- MATURATION DE L'ARN
- GÈNES EN MOSAÏQUE
- TRANSPORTS MEMBRANAIRES
- CATALYSE ENZYMATIQUE
- POTENTIEL ÉLECTRIQUE
- HÉRÉDITAIRES MALADIES ou MALADIES GÉNÉTIQUES
- ATP SYNTHÉTASE
- PROTÉINES FER-SOUFRE
- CYTOPLASME
- ADN POLYMÉRASE
- CODON, biologie moléculaire
- ARN DE TRANSFERT ou ARNt
- ARN MESSAGER ou ARNm
- ARN POLYMÉRASE
- RÉPLICATION, biologie moléculaire
- TRANSCRIPTION, biologie moléculaire
- TRADUCTION, biologie moléculaire
- THERMOGENÈSE
- CYTOCHROMES
- POTENTIEL D'OXYDORÉDUCTION
- NERNST ÉQUATION DE
- MALADIES MITOCHONDRIALES
- OXYDATION
- URÉE
- MÉTABOLISME CELLULAIRE
- INHIBITEURS, biochimie
- COENZYMES ou COFACTEURS ENZYMATIQUES
- CHIMIOSMOTIQUE THÉORIE
- GRAS ACIDES
- NIGERICINE
- PHOSPHORYLATION
- DÉCARBOXYLATION
- FLAVINE ADÉNINE DINUCLÉOTIDE (FAD)
- FLAVOPROTÉINES
- UBIQUINONES ou COENZYMES Q
- NICOTINAMIDE ADÉNINE DINUCLÉOTIDE PHOSPHATE (NADP)
- PYRUVATE
- TRANSAMINASE
- PHOSPHATES
- PHOSPHORYLATION OXYDATIVE
- PROTÉINES MEMBRANAIRES
- HÉRÉDITÉ FAMILIALE
- CITRATE
- CYTOCHROME OXYDASE
- AMMONIAC, biochimie
- GÉNOME
- URÉOGENÈSE
- PHOSPHOLIPIDES
- NICOTINAMIDE ADÉNINE DINUCLÉOTIDE (NAD)
- ORGANITES CELLULAIRES
- COLORATION, cytologie
- GUANOSINE TRIPHOSPHATE (GTP)
- CHLORAMPHÉNICOL
- ENTHALPIE LIBRE ou ÉNERGIE LIBRE DE GIBBS
- RÉDUCTION, chimie
- GRAS MÉTABOLISME DES ACIDES
- BÊTA-OXYDATION
- BIOSYNTHÈSES
- ACÉTYL-COENZYME A ou ACÉTYL-CoA
- GLUCONÉOGENÈSE ou NÉOGLUCOGENÈSE
- PROTÉINES BIOSYNTHÈSE DES
- OXYDORÉDUCTIONS, biologie
- BIOÉNERGÉTIQUE
- CHAÎNE RESPIRATOIRE
- CITRATE SYNTHÉTASE
- OXALOACÉTATE
- SUCCINATE
- MALATE
- CYTOPLASMIQUE HÉRÉDITÉ
- CONTRACTION MUSCULAIRE
- GLYCOLYSE
- DIFFUSION TRANSMEMBRANAIRE, biologie
- CYTOLOGIE ou BIOLOGIE CELLULAIRE
- RÉGULATION GÉNÉTIQUE
- TRANSPORT D'ÉLECTRONS, bioénergétique
- FORCE PROTOMOTRICE
- COUPLAGE, biochimie
- EXPRESSION GÉNÉTIQUE
- EXON
- INTRON
- PASTEUR EFFET
- DÉCOUPLAGE, biochimie
- VALINOMYCINE
- ADÉNOSINE DIPHOSPHATE (ADP)
- PROTONS GRADIENT DE
- CALCIUM & MÉTABOLISME CELLULAIRE
- PHOSPHOÉNOLPYRUVATE (PEP)
- CHOLINE & PHOSPHODÉRIVÉS CHOLINIQUES
- GÉNÉTIQUE MOLÉCULAIRE
- RÉGULATIONS BIOCHIMIQUES
- FERRÉDOXINE
- LIPOSOMES
- PHOSPHOFRUCTOKINASE
- ARN RIBOSOMIQUE ou ARNr
- DÉSHYDROGÉNASES
- ÉPISSAGE, génétique moléculaire
- REDOX COUPLE
- CARBONIQUE GAZ ou DIOXYDE DE CARBONE