DIPOLAIRES MOMENTS
Bibliographie
C. J. F. Böttcher & P. Bordewijk, « Dielectrics in time dependent fields », in C. J. F. Böttcher & P. Bordewijk dir., Theory of Electric Polarization, vol. II, Elsevier, Amsterdam, 1978
C. J. F. Böttcher, O. C. Van Belle, P. Bordewijk & A. Rip, « Dielectrics in static fields », ibid., vol. I, 1973
A. D. Buckingham, « Intermolecular interactions from diatomics to biopolymers », in B. Pullman dir., Quantum Mechanics of Molecular Conformation, pp. 1-67, Wiley, New York, 1978
G. Stell, G. N. Patey & J. S. H
oye, « Dielectric constant of fluid models », in I. Prigogine & S. A. Rice dir., Statisticalmechanicaltheory and its quantitative implementation, t. XLVIII, p. 183, Wiley, 1981
H. V. Temperley & D. H. Trevena, Les Liquides et leurs propriétés : traité moléculaire et macroscopique avec applications, Technique et Documentation, Paris, 1980
M. R. Wright, The Nature of Electrolyte Solutions, Macmillan Education, Londres, 1988.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean BARRIOL : Correspondant de l'Institut. Professeur émérite à l'Université Nancy
Classification
Médias
Autres références
-
DEBYE PETER JOSEPH WILLEM (1884-1966)
- Écrit par P. M. HEIMANN
- 1 237 mots
...sont inégalement distribués parmi les atomes dans les molécules, de sorte que celles-ci peuvent être considérées comme des dipôles électriques permanents. Debye put expliciter la liaison entre structure moléculaire et moment dipolaire (produit de la charge par la distance constante entre les pôles). -
FERRO-ÉLECTRICITÉ
- Écrit par Lucien GODEFROY
- 2 836 mots
- 3 médias
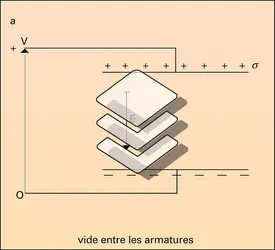
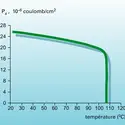
Les corps ferro-électriques sont une classe de diélectriques solides, dont l'étude s'est développée depuis 1945. L'intérêt de ces matériaux n'est pas seulement théorique ; leur très grande constante diélectrique, leurs propriétés non linéaires, tant électriques qu'optiques, sont exploitées dans de...
-
INTERACTIONS (physique) - Électromagnétisme
- Écrit par Bernard DIU
- 4 448 mots
- 6 médias
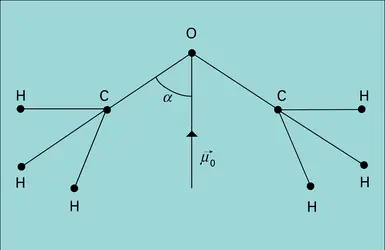
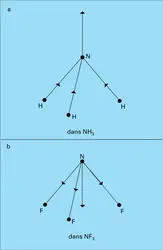
Deux charges opposées localisées en des points distincts constituent un dipôle électrique.Les molécules d'eau H2O et d'ammoniac NH3 sont ainsi dipolaires : les électrons qui assurent dans ces molécules les liaisons covalentes sont (partiellement) repoussés par les H, « électropositifs... -
LIAISONS CHIMIQUES - Liaison et classification
- Écrit par André JULG
- 8 250 mots
- 7 médias
Le centre de gravité des électrons ne coïncidant alors plus avec celui des noyaux positifs, la liaison possède un moment dipolaire. Les moments des diverses liaisons se composent géométriquement pour donner le moment dipolaire total de la molécule. - Afficher les 9 références