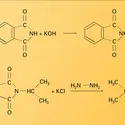
NITRILES
Bibliographie
N. L. Allinger et al., Organic Chemistry, Worth, New York, 2e éd. 1976
H. Beyer & W. Walter, Lehrbuch der Organischen Chemie, Hirzel, Stuttgart, 22e éd. 1991
F. A. Carey, Advanced Organic Chemistry, Plenum, New York, 3e éd. 1990
A. Chauvel, G. Lefebvre & L. Castex, Procédés de pétrochimie, Technip, Paris, 2e éd. 1985
J. March, Advanced Organic Chemistry, J. Wiley & Sons, New York, 4e éd. 1992
J. McMurry, Organic Chemistry, Brooks-Cole Publishing Company, Pacific Grove California, 3e éd. 1992
T. W. G. Solomons, Organic Chemistry, J. Wiley & Sons, 5e éd. 1991
A. Streitwieser Jr. & C. H. Heathcock, Introduction à la chimie organique, Ellipses, Paris, 1986
K. Weissermel & H. J. Arpe, Chimie organique industrielle, Masson, Paris, 1981.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques METZGER : professeur de chimie organique à la faculté des sciences de Marseille
Classification
Média
Autres références
-
AMIDES
- Écrit par Jacques METZGER
- 1 922 mots
- 3 médias
L' hydratation des nitriles, en catalyse acide ou basique, conduit aux amides primaires, mais la réaction est difficile à contrôler car ces derniers, dans ces conditions, s'hydrolysent en sel d'ammonium de l'acide. On peut toutefois contrôler cette hydratation en employant l'eau oxygénée qui forme un... -
AMINES
- Écrit par Jacques METZGER
- 3 235 mots
- 4 médias
Ces dernières sont également obtenues par l'hydrogénation catalytique desnitriles sur catalyseur de nickel à 100 0C. On les prépare enfin par réduction des imines : ces dernières résultant de l'action de l'ammoniac sur un dérivé carbonylé, ces deux composés sont soumis à l'hydrogénation :... -
CASSINI-HUYGENS (MISSION)
- Écrit par Athéna COUSTENIS
- 4 465 mots
- 9 médias
...atmosphère et produisent des composés organiques complexes (essentiellement des hydrocarbures comme l’éthane, l’acétylène et le propane, ou des nitriles comme l’acide cyanhydrique) qui se diffusent à travers l’atmosphère, se condensent et viennent se déposer à la surface de ce satellite. Les mesures... -
CYANURE D'HYDROGÈNE
- Écrit par Encyclopædia Universalis
- 331 mots
Également appelé formonitrile, le cyanure d'hydrogène H—C≡N est un liquide incolore, très mobile, de forte odeur d'amandes amères, fortement toxique et miscible à l'eau en toutes proportions : ses solutions sont connues sous le nom d'acide cyanhydrique ou acide prussique (nom provenant...
- Afficher les 8 références