PLASMIDES
Article modifié le
Plasmides R : plasmides de résistance aux antibiotiques
Historique
C'est vers la fin des années 1950 que deux microbiologistes japonais, Ochiai et Akiba, observèrent au cours d'une épidémie de dysenterie bacillaire l'apparition de bactéries résistantes à trois antibiotiques à la fois, rendant les malades atteints insensibles au traitement par des antibiotiques habituellement efficaces. Un mécanisme de mutation chromosomique-sélection, auparavant décrit par Ledeberg et qui permettait d'expliquer les résistances bactériennes observées jusque-là, ne permettait pas d'expliquer cette triple résistance simultanée à trois familles d'antibiotiques différentes. Les auteurs japonais montrèrent alors que cette résistance multiple se transférait entre bactéries intestinales dans le tube digestif des malades, puis ils reproduisirent ce transfert in vitro entre colibacilles et shigelles et démontrèrent que ces bactéries résistantes possèdent en plus de leur chromosome d'autres structures composées d'ADN portant les gènes responsables de cette résistance multiple transférable : ce sont les plasmides de résistance aux antibiotiques ou plasmides R. La découverte de ces éléments génétiques extrachromosomiques mobiles apparut d'emblée d'une importance considérable en clinique par leur incidence sur l'arsenal thérapeutique antibiotique. Les plasmides R permettent aux bactéries d'acquérir la résistance à un ou plusieurs antibiotiques d'emblée ; cette résistance est transférable de bactérie à bactérie de la même espèce mais aussi d'espèces voire de genres différents ; la résistance peut apparaître ainsi dans une espèce bactérienne jusque-là sensible, la sélection par un antibiotique peut être responsable de la sélection de la résistance à plusieurs antibiotiques non employés, enfin la coexistence possible de plusieurs plasmides R dans une seule cellule bactérienne permet d'expliquer l'émergence dans les milieux à forte pression de sélection antibiotique comme le milieu hospitalier de bactéries multirésistantes responsables d'échec thérapeutique. Depuis leur découverte chez les entérobactéries, des plasmides R ont pu être mis en évidence chez la plupart des bactéries d'intérêt médical, vétérinaire ou industriel.
Espèces bactériennes hébergeant des plasmides
Depuis leur découverte chez Shigella dysenteriae, des plasmides de résistance ont été isolés dans la plupart des bactéries pathogènes. Des plasmides ont été mis en évidence chez les bacilles à Gram négatif (entérobactéries diverses, Yersinia, Pseudomonas, Acinetobacter, Aeromonas, Vibrio, Haemophilus, Pasteurella, Bordetella, Campylobacter, Bacteroides fragilis), les bacilles à Gram positif (Actinomyces, Bacillus, Clostridium perfringens), les cocci à Gram positif (staphylocoques, streptocoques) et les cocci à Gram négatif (gonocoques). Le pneumocoque et le méningocoque restent les deux seules bactéries de grande importance en pathologie infectieuse dépourvues pour l'instant de plasmides. Des plasmides de résistance peuvent être isolés de nombreuses bactéries de l'environnement, en particulier chez les Streptomyces, bactéries productrices d'antibiotiques. Ces bactéries possèdent les gènes de résistance qui les protègent de l'action de l'antibiotique qu'elles produisent. Ces bactéries productrices d'antibiotiques seraient le réservoir et l'origine de la dissémination des gènes de résistance chez les bactéries pathogènes.
Diversification
Deux mécanismes, la mutation et la transposition, permettent la diversification du matériel plasmidique.
Mutation
Des mutations spontanées ou provoquées par des agents mutagènes permettent d'isoler à partir du plasmide originel des variants ou délétants qui sont très utiles pour étudier les propriétés des plasmides : étude de la réplication à l'aide de mutants thermosensibles, étude du transfert avec des mutants déréprimés pour le transfert ou au contraire mutants ayant perdu la transférabilité. Ces mutants ont peu d'incidence sur le phénomène de résistance des antibiotiques.
Transposition
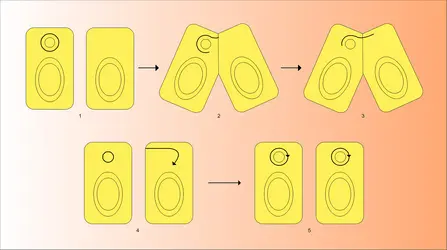
Les plasmides peuvent acquérir de nouveaux gènes, en particulier des gènes de résistance aux antibiotiques par le mécanisme de transposition. Certains gènes responsables de la résistance aux antibiotiques sont inclus dans un petit fragment d'ADN qui a la propriété de se détacher ou de « s'exciser » de la molécule d'ADN qui le contient et de s'insérer sur une autre molécule d'ADN. Ces morceaux d'ADN sauteurs ont été appelés « transposons ». Certains gènes de résistance sont donc capables par ce mécanisme de sauter d'un plasmide à un autre, d'un plasmide sur un chromosome ou d'un chromosome sur un plasmide. Le phénomène de transposition est un mécanisme qui assure une dissémination très efficace des gènes de résistance. La transposition est un phénomène différent de la recombinaison classique. Elle ne nécessite pas l'enzyme recombinase, elle ne nécessite pas d'homologie entre les ADN donneurs et receveurs du transposon. C'est ainsi que des plasmides appartenant à des groupes d'incompatibilité différents et sans homologie ADN-ADN peuvent porter des gènes de résistance identiques. Les transposons connus mesurent de 2,5 à 20 kilobases, et portent en plus des gènes responsables de la résistance aux antibiotiques, des gènes codant pour des enzymes responsables du mécanisme de transposition et de sa régulation. De nombreux transposons codant pour la résistance à différents antibiotiques ont été caractérisés : β-lactamines, streptomycine, kanamycine, gentamicine, tétracycline, érythromycine, chloramphénicol, triméthoprime, sulfamides, phosphomycine. La transposition permet d'expliquer d'une part comment des plasmides R sont capables au cours de leur évolution d'acquérir de nouveaux gènes de résistance ; d'autre part elle explique comment des plasmides sans fonction connue et que l'on appelle « cryptiques » peuvent acquérir des gènes de résistance par le mécanisme de transposition et devenir ainsi des plasmides de résistance. La résistance envers un antibiotique peut apparaître ainsi dans des espèces bactériennes jusque-là sensibles. Ce phénomène a permis d'expliquer l'apparition de souches résistant à la pénicilline chez les Haemophilus et les gonocoques, espèces jusque-là sensibles à cet antibiotique, par la transposition sur des plasmides cryptiques, connus dans ces espèces, de gènes de résistance provenant d'Escherichia coli.
Importance pratique
Les mécanismes de résistance codés par les plasmides
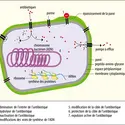
Les plasmides sont capables de rendre les bactéries résistantes par différents mécanismes qui impliquent généralement la synthèse de protéines codées par des gènes plasmidiques : production d'enzymes inactivant l'antibiotique en modifiant sa molécule, modification de la cible de l'antibiotique par une enzyme, diminution de la quantité d'antibiotique transportée à l'intérieur de la bactérie, substitution d'une molécule nouvelle à la place de la cible de l'antibiotique. La majorité des antibiotiques est inactivée par l'un ou l'autre de ces mécanismes, et rares sont les antibiotiques pour lesquels aucune résistance plasmidique n'a été décelée.
Outils pour génie génétique
L'existence de plasmides de résistance n'a pas que des aspects néfastes en amputant l'arsenal thérapeutique. Ce sont des outils particulièrement efficaces dans les expériences de génie génétique. Un des champs d'application privilégiés du génie génétique est l'introduction de gènes codant pour des protéines animales ou humaines dans Escherichia coli pour transformer cette bactérie en usine à fabriquer des protéines d'intérêt thérapeutique ou industriel : hormones, insuline, interféron, etc. Il n'est pas possible actuellement d'introduire directement un fragment d'ADN venant d'organismes supérieurs dans une bactérie et de le fixer sur le chromosome bactérien pour que cette information soit répliquée et transmise à la descendance de la bactérie ; un intermédiaire que l'on appelle « vecteur » est indispensable à cette opération. Les plasmides de résistance sont avec les phages les vecteurs essentiellement utilisés. Le plasmide choisi est isolé de la bactérie résistante, purifié, et coupé par une endonucléase de restriction. Le fragment d'ADN étranger peut alors être inséré dans le plasmide ouvert, la molécule hybride recircularisée (fragment d'ADN + plasmide) est introduite chez Escherichia coli. Les bactéries ayant reçu la molécule hybride sont aisément sélectionnées par leur résistance à un antibiotique, codée par le plasmide. Introduire un gène étranger par cet artifice chez Escherichia coli est une opération simple aujourd'hui. Cependant, l'expression de ce gène « importé » dans un environnement qui lui est totalement étranger reste largement imprévisible. Ce phénomène est à l'origine des échecs relativement nombreux rencontrés par les précurseurs dans ce domaine, difficultés qui sont actuellement partiellement résolues.
Problèmes épidémiologiques
Actuellement, la résistance d'origine plasmidique rend compte de plus de 80 p. 100 de la résistance bactérienne aux antibiotiques. Dans la nature, chez l'homme sain ou malade, et chez les animaux, les bactéries porteuses de plasmides de résistance sont de plus en plus nombreuses. Les quantités considérables d'antibiotiques déversées dans l'environnement à des fins thérapeutiques ou autres depuis les années 1940 sont vraisemblablement à l'origine de la sélection de bactéries résistantes. L'antibiosupplémentation de l'alimentation du bétail, en particulier, a été mise en cause dans l'augmentation de fréquence des bactéries multirésistantes. Ainsi, on a pu montré que 100 p. 100 des porcs et des veaux recevant des antibiotiques hébergeaient dans leur tube digestif des entérobactéries porteuses de plasmides de résistance transférables. Chez les éleveurs ne recevant pas d'antibiotiques, mais en contact avec les animaux, le portage digestif d'entérobactéries résistantes est de 50 p. 100 ou plus ; en revanche, l'étude d'une population isolée de Bornéo sans contact avec les antibiotiques a montré que moins de 1 p. 100 des bactéries des selles pouvaient transférer leur résistance. Dans l'environnement, on peut isoler des bactéries multirésistantes dans les égouts, sur les plages par exemple. On peut donc supposer que c'est l'utilisation massive des antibiotiques qui est responsable d'un si brutal changement écologique. La dissémination de la résistance s'effectue par plusieurs mécanismes parfois étroitement intriqués. Une souche d'une bactérie pathogène peut acquérir un plasmide de résistance provenant d'une entérobactérie du tube digestif, puis cette souche disséminer dans la population (ou de malade à malade), réalisant de la sorte une épidémie due à une seule et unique souche. Il existe de nombreux exemples de telles épidémies : épidémie de fièvre typhoïde en Amérique latine due à une Salmonella porteuse d'un plasmide de résistance au chloramphénicol et à l'ampicilline, épidémies hospitalières à bactéries multirésistantes responsables d'infections nosocomiales dans un milieu à forte pression de sélection par les antibiotiques. En milieu hospitalier, on peut suivre un autre mode de dissémination de la résistance : des épidémies de plasmides, le même plasmide de résistance se propageant au fil du temps dans plusieurs espèces bactériennes différentes dans le même hôpital. De telles épidémies de plasmides de résistance à la gentamicine et au triméthoprime ont été bien individualisées par la comparaison fine des plasmides isolés des différentes espèces de bactéries résistant aux mêmes antibiotiques. Enfin, plus récemment, on a pu démontrer l'identité des gènes de résistance et isoler des transposons identiques sur différents plasmides hébergés par des espèces ou des genres bactériens très divers. Il s'agit alors d'épidémies de transposons. Une appréciation correcte du danger de la résistance plasmidique repose sur l'épidémiologie des plasmides et des gènes de résistance permettant de connaître, de suivre, éventuellement de prévoir et d'empêcher leur dissémination.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Annie BUU HOÏ : docteur en médecine, assistant des hôpitaux, chef de travaux
- Michel GUÉRINEAU : maître de recherche au C.N.R.S.
Classification
Médias
Autres références
-
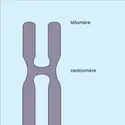
EUCARYOTES (CHROMOSOME DES)
- Écrit par Denise ZICKLER
- 7 724 mots
- 9 médias
...centrale très riche en adénine et thymine (Fitzgerald-Hayes et al., 1982). Ces fragments d'ADN (de 600 à 800 paires de nucléotides) ont été insérés dans des plasmides, molécule d'ADN circulaire, autoréplicable, qui sont eux-mêmes réintroduits dans une cellule de levure. Grâce à un jeu de marqueurs génétiques... -
ANTIBIORÉSISTANCE
- Écrit par Aurélie CHABAUD , Sylvain MEYER et Marie-Cécile PLOY
- 5 907 mots
- 4 médias
Lesplasmides de résistance (en réalité les plasmides porteurs de gènes de résistance) sont les principaux acteurs de la dissémination de ces gènes au sein des populations bactériennes. Les plasmides sont de petites molécules d’ADN circulaire fermées, indépendantes du chromosome bactérien, et capables... -
BACTÉRIES
- Écrit par Jean-Michel ALONSO , Jacques BEJOT et Patrick FORTERRE
- 11 055 mots
- 3 médias
...fonctions non codées par les gènes chromosomiques. Ces ADN extrachromosomiques sont transférables d'une bactérie à l'autre. Il s'agit des plasmides et épisomes. Les plasmides au sens strict sont des ADN extrachromosomiques se répliquant dans le cytoplasme bactérien, indépendamment de la réplication du... -
BACTÉRIOLOGIE
- Écrit par Jean-Michel ALONSO , Jacques BEJOT , Michel DESMAZEAUD , Didier LAVERGNE et Daniel MAZIGH
- 18 335 mots
- 11 médias
...génétique consiste à l'amplification des gènes en amenant les structures qui les portent à être répliquées rapidement. On multiplie ainsi les plasmides, petits morceaux d'ADN circulaires extrachromosomiques au nombre de 2 à 30 par bactérie. Dans certaines espèces, pour amplifier des gènes et... - Afficher les 13 références
Voir aussi
- HYBRIDATION MOLÉCULAIRE
- RÉPLICATION, biologie moléculaire
- SHIGELLA
- EUCARYOTES
- ALIMENTATION ANIMALE, élevage
- AZOTE ATMOSPHÉRIQUE
- BIOLOGIE MOLÉCULAIRE
- RHIZOBIUM
- AZOTE CYCLE DE L'
- CHROMOSOMES
- PROCARYOTES ou PROTOCARYOTES
- RÉSISTANCE BACTÉRIENNE
- STREPTOMYCES
- ÉPISOMES
- ÉPIDÉMIES
- ENZYMES DE RESTRICTION ou ENDONUCLÉASES DE RESTRICTION
- CONJUGAISON BACTÉRIENNE
- GÉNÉTIQUE MOLÉCULAIRE
- TRANSPOSON