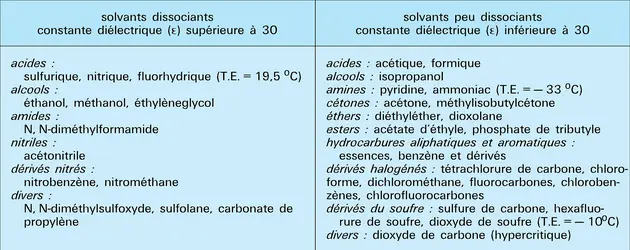
SOLVANTS
La chimie en solution
La mise en contact des réactifs en solution provoque des réactions qui évoluent spontanément jusqu'à un état d'équilibre caractérisé par un ensemble de constantes d'équilibre thermodynamique. Dans ces réactions, le solvant n'est pas inerte et les états d'équilibre sont étroitement dépendants de sa nature. L'acquisition d'un grand nombre de données relatives aux équilibres en solution dans des solvants variés et dans des mélanges de solvants permet d'intervenir de façon rationnelle sur la réactivité des espèces, par modification de l'acidité, ou par le jeu de réactions de formation de complexes, par exemple. Ces effets sont également mis en œuvre dans les techniques de séparation, aussi bien sur le plan analytique en chromatographie en phase liquide que sur le plan préparatif en extraction liquide-liquide. Le solvant agit également sur la vitesse des réactions : cela est important en synthèse organique où un choix judicieux permet d'orienter la réaction à partir de critères cinétiques. Par exemple, la vitesse des réactions de substitution nucléophile est plus importante dans les solvants les plus polaires.
Les propriétés oxydoréductrices de l'eau peuvent, comme les caractéristiques acide-base, en limiter les applications et justifier l'emploi d'un solvant. Le développement des piles et batteries au lithium, par exemple, n'a été possible qu'en faisant appel à des électrolytes à base de solvants non aqueux (carbonate de propylène ou de dioxolane, etc.) ; ces solvants sont peu sensibles au pouvoir réducteur du lithium métallique utilisé comme électrode.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques DEVYNCK : directeur de recherche au C.N.R.S.
Classification
Média
Autres références
-
ACÉTONE
- Écrit par Roger GALLO
- 641 mots
Liquide volatil incolore, d'une odeur piquante, miscible avec l'eau, l'alcool, l'éther, le chloroforme et le benzène, l'acétone, ou diméthylcétone, ou propan-2-one, a pour formule brute C3H6O : un atome de carbone C est lié par des liaisons chimiques simples à deux...
-
ACÉTYLÈNE
- Écrit par Henri GUÉRIN
- 5 094 mots
- 6 médias
...l'extension, lorsque les travaux de Linde et de Claude eurent fourni la possibilité d'extraire facilement l'oxygène de l'air. La préparation de solvants chlorés : trichloréthylène et perchloréthylène, entreprise dès 1910 en Allemagne, ne devait surtout se développer en France et dans les autres... -
ACIDES & BASES
- Écrit par Yves GAUTIER et Pierre SOUCHAY
- 12 367 mots
- 7 médias
Enraison de sa charge élevée par rapport à son volume, H+ n'existe pas comme tel en solution, mais se fixe sur le solvant (dénommé SH) qui se trouve jouer ainsi le rôle de base. Par conséquent, l'ionisation d'un acide dans l' eau ne s'écrira pas :mais : et la constante...
et la constante...
-
ALCOOL ÉTHYLIQUE ou ÉTHANOL
- Écrit par Fernand COUSSEMANT
- 694 mots
Alcool primaire, liquide incolore, d'odeur agréable, miscible à l'eau en toutes proportions, miscible à de nombreux solvants organiques, l'éthanol ou alcool éthylique, CH3—CH2OH, a les caractéristiques suivantes :
Masse moléculaire : 46,07 g
Masse spécifique : 0,789 3...
- Afficher les 45 références