SOUFRE
Article modifié le
Composés organiques
Dérivés du soufre bivalent
Thiols, ou mercaptans
Les thiols, ou mercaptans, ont pour formule générale R—SH ; ce sont les analogues sulfurés des alcools (R : aliphatique) et des phénols (R : aromatique) largement utilisés industriellement en agrochimie et en pharmacochimie.
Les termes les plus légers ont une odeur forte, généralement repoussante, mais, quand le nombre d'atomes de carbone de la molécule dépasse 12, l'odeur s'atténue et même disparaît pour les termes les plus lourds.
Les thiols se rencontrent dans de nombreux milieux organiques. On en trouve notamment dans les essences d'ail (prop-2-ènethiol, ou allyl mercaptan), de pamplemousse (p-menthènethiol) et dans l'arôme de viande grillée (furanethiols). Les produits pétroliers contiennent de nombreux mercaptans.
Les thiols peuvent être obtenus par addition d'hydrogène sulfuré à un alcène, vers 160 0C :



Le groupe —SH, caractéristique des thiols, est parfois associé à d'autres fonctions chimiques et est souvent désigné par le préfixe « mercapto ». Il existe dans des aminoacides importants, constituants de protéines ou d'antibiotiques.
La cystéine, dont la formule est HS— CH2—CH(NH2)—CO2H, et le disulfure correspondant, [HCO2—CH(NH2)—CH2—S]2, sont des constituants des protéines.
Sulfures
Les sulfures R—S—R′ correspondent aux oxydes (éthers-oxydes) R—O—R′, mais le soufre est un meilleur nucléophile que l'oxygène, c'est-à-dire qu'il est plus efficace pour se substituer à des groupes ou des atomes électronégatifs comme le brome et l'iode fixés sur une molécule organique. Il en résulte que les ions sulfonium R3S+ sont d'un accès plus aisé que les ions oxonium R3O+.
Les sulfures se rencontrent dans beaucoup de composés naturels. Le sulfure de méthyle a été détecté dans diverses essences végétales et constitue un sous-produit de la fabrication des pâtes à papier par la « méthode au sulfate » ou le procédé Kraft. De nombreux sulfures se trouvent dans les produits pétroliers distillés mais peuvent souvent, comme dans la préparation de la pâte à papier, provenir des réactions chimiques en cours de traitement et ne pas exister dans la matière première.
Un sulfure cyclique C4H8S (tétrahydrothiophène) est un produit industriel important servant à « odoriser » les combustibles pétroliers gazeux pour permettre une détection rapide des fuites éventuelles.
Les sulfures (RSR′) sont généralement obtenus par alkylation d'un thiolate alcalin, ou du sulfure de sodium pour les composés symétriques (R=R′) :
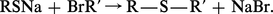

Disulfures et polysulfures
Entre autres propriétés, les thiols se distinguent des alcools par la possibilité de former des disulfures par oxydation douce :
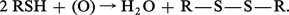
Leurs analogues oxygénés dérivés des alcools, les peroxydes R—O—O—R, sont peu stables et préparés de manière différente.
Des molécules possédant des groupements sulfures et disulfures sont responsables de certains arômes naturels : fruit de la passion, café, cacahuète, asperge, etc. À côté des disulfures, on connaît les polysulfures R— Sn—R (pouvant contenir jusqu'à une dizaine d'atomes de soufre) utilisés comme additifs pour lubrifiants ou pour la sulfuration d'oxydes métalliques, catalyseurs en pétrochimie.
Dérivés sulfurés des aldéhydes et des cétones
En faisant agir des thiols sur les aldéhydes ou sur les cétones, en milieu acide, on obtient aisément des dithioacétals R′CH(SR)2 ou R′R″C(SR)2. Les thioaldéhydes RCH=S et les thiocétones RR′C=S sont plus difficiles d'accès que les composés oxygénés correspondants.
Ces thioaldéhydes et thiocétones sont souvent aisément polymérisables, ce qui rend leur étude délicate. Toutefois, on connaît un bon nombre de thiocétones aromatiques telles que la thiobenzophénone C6H5—CS—C6H5, d'une remarquable couleur bleue.
La réactivité du groupement C=S (thiocarbonyle) est souvent très différente de celle du groupement C=O (carbonyle) de leurs analogues oxygénés. En particulier, l'orientation de l'addition d'un organométallique peut être parfois totalement inversée (addition thiophile) :

Dérivés sulfurés d'acides carboxyliques
Aux acides carboxyliques R—COOH et à leurs esters R—COOR′ correspondent des composés sulfurés dans lesquels un atome d'oxygène a été remplacé par un atome de soufre. Dans le cas des esters, les deux structures possibles R—CS—OR′ et R— CO—SR′ sont facilement accessibles. On connaît aussi des corps où les deux atomes d'oxygène ont été remplacés : les acides et les esters dithiocarboxyliques R—CS—SH et R—CS—SR′. Les xanthates sont des dithiocarbonates formés par action du sulfure de carbone sur des dérivés alcalins d'alcools :

La cellulose est un polyalcool macromoléculaire à partir duquel on peut obtenir des xanthates qui servent à la préparation de fibres (viscose) ou de films (cellophane).
Le sulfure de carbone réagit sur l'ammoniac et sur les amines primaires ou secondaires en donnant des acides dithiocarbamiques :


Dérivés du soufre quadrivalent
Il existe peu de composés de type SX4 où le soufre soit clairement quadrivalent. En chimie organique, la quadrivalence formelle du soufre se manifeste surtout dans des composés tricoordinés, où l'atome de soufre est lié à trois autres atomes, la quatrième valence étant de type électrostatique (charge positive sur le soufre) ou correspondant à une double liaison possible. Il en est ainsi dans les ions sulfonium R3S+, les sulfoxydes R—S(O)—R que l'on peut écrire : R— S(=O)R ou R—S+(O—)—R, et les ylures de sulfonium [R2S=C(R′R″)] ; les sulfoxydes sont généralement obtenus par oxydation ménagée des sulfures correspondants et les ylures par action d'une base sur les sels de sulfonium.
Dans cette classe de composés, on peut aussi citer les acides sulfiniques R—SO—OH que l'on obtient par réduction ménagée de chlorures d'acides sulfoniques :



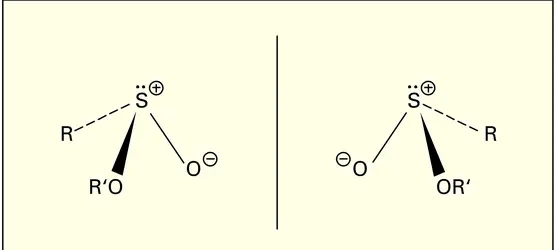
Une propriété physique intéressante des ions sulfonium, des sulfoxydes et des esters sulfiniques est leur stéréo- isomérie optique dès lors que les trois groupes liés au soufre sont différents. Les liaisons du soufre du type sulfonium ne sont pas coplanaires, mais disposées selon les arêtes d'une pyramide à base triangulaire dont l'atome de soufre occupe le sommet (cf. la formule décrivant un ester sulfinique ; cette figure montre que les deux structures symétriques par rapport à un plan ne sont pas superposables).
Cette asymétrie, notamment dans le cas des sulfoxydes, est largement mise à profit en synthèse organique pour induire une asymétrie sur un carbone voisin.
Dérivés du soufre hexavalent
On peut faire sur cette hexavalence du soufre les mêmes réserves que sur sa quadrivalence. Il est peu de composés, comme SF6 et ses dérivés organiques, où le soufre soit à la fois hexacoordiné et hexavalent, et l'on a, le plus souvent, des dérivés du soufre hexavalent où cet élément est quadricoordiné comme dans l'ion sulfate SO2—4.
Acides sulfoniques
La classe la plus importante de composés organiques de ce groupe est constituée sans aucun doute par les acides sulfoniques R—SO3H et leurs dérivés. Comme l'acide sulfurique, ce sont des acides forts, et de nombreux sels d'acides sulfoniques sont solubles dans l'eau. L'introduction de groupes —SO3H dans les molécules organiques est utilisée dans la préparation des détergents et des composés tensioactifs.
En série aliphatique, les acides sulfoniques sont souvent obtenus par sulfochloruration ; celle-ci donne d'abord un chlorure d'acide que l'on hydrolyse ensuite :


Les acides sulfoniques aromatiques sont le plus souvent obtenus par sulfonation des hydrocarbures par l'acide sulfurique concentré, réaction d'ailleurs réversible :
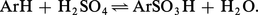
Les acides sulfoniques, traités par le pentachlorure de phosphore, donnent des chlorures d'acides sulfoniques, par une réaction analogue à celle qui fournit les chlorures d'acides carboxyliques :

En présence de chlorure d'aluminium (réaction de Friedel et Crafts), les chlorures d'acides sulfoniques réagissent sur les hydrocarbures aromatiques pour donner des sulfones :

Une réaction importante des chlorures d'acides sulfoniques est la formation d'amides à partir de l'ammoniac ou des amines primaires ou secondaires :
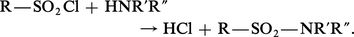
Composés hétérocycliques sulfurés
Les atomes de soufre ou les groupes —SO— ou —SO2— peuvent être inclus dans des cycles saturés, et les composés ainsi obtenus sont en général tout à fait analogues, sauf dans le cas de petits cycles, aux composés non cycliques correspondants : sulfures, sulfoxydes, sulfones.
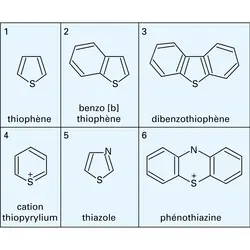
Lorsque le soufre est engagé dans des cycles insaturés à caractère aromatique, ceux-ci présentent une stabilité particulière. Quelques exemples d' hétérocycles sulfurés sont donnés dans le tableau.
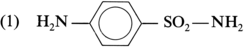
Le thiophène (formule 1) accompagne le benzène dans les goudrons de houille. Ses propriétés physiques sont très proches de celles du benzène, et ses propriétés chimiques présentent aussi des analogies avec celles des hydrocarbures aromatiques.
Des systèmes thiophéniques à cycles condensés (exemple : formule 2) se trouvent dans les fractions lourdes des produits pétroliers, et ces composés, ainsi que des systèmes plus condensés, sont, pour une large part, responsables de la teneur en soufre des fuels lourds.
Ces hétérocycles ont été à l'origine de développements récents dans le domaine des composés organiques conducteurs : les polythiophènes, particulièrement ceux qui sont substitués en position 3 (formule 4), dopés par des donneurs d'électrons (iode, chlorure ferrique, etc.) sont conducteurs de l'électricité (exemple d'application envisagée : accumulateurs), et les dérivés du tétrathiafulvalène (TTF, formule 3) forment des complexes à transfert de charge (exemple : TTF-tétracyanoquinodiméthane) et des sels ions radicaux [exemple : (TTF)+ ( X—]qui présentent des propriétés électriques anisotropes ; à très basse température, certains d'entre eux sont des supraconducteurs organiques.
Le soufre existe aussi dans des composés hétérocycliques sulfurés et azotés. Le noyau du thiazole (formule 5) a une grande importance biologique. On le trouve, sous forme d'ion positif, dans la vitamine B1, ou thiamine. On le rencontre aussi, sous forme hydrogénée, dans les pénicillines.
Enfin, le noyau de la phénothiazine (formule 6) intervient dans la structure de médicaments tranquillisants.
La chimie organique du soufre connaît un développement constant lié à l'utilisation des composés sulfurés comme intermédiaires de synthèse en chimie fine et industrielle (un exemple frappant : l'utilisation des sulfones dans la synthèse industrielle de la vitamine A).
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Fernande CHATAGNER : maître de recherche au C.N.R.S.
- René LECLERCQ : vice-président de l'Institut International du soufre
- Noël LOZAC'H : doyen honoraire de la faculté des sciences de Caen, professeur émérite de l'université de Caen
- Serge MASSON : directeur de recherche au C.N.R.S., Caen
Classification
Médias
Autres références
-
CARBURANTS
- Écrit par Daniel BALLERINI , Jean-Claude GUIBET et Xavier MONTAGNE
- 10 536 mots
- 9 médias
De façon générale, la fabrication du gazole fait intervenir deux grands types de réactions chimiques : la désulfuration et l'hydrogénation. La première permet d'atteindre de très bas niveaux de teneur en soufre maintenant spécifiés par les réglementations antipollution (10 ppm maximum... -
COLORANTS
- Écrit par Daniel FUES
- 6 775 mots
- 4 médias
Les colorants au soufre sont insolubles dans l'eau. Ainsi, leur application en teinture passe par une réduction alcaline pour aboutir à un composé soluble, appelé leucodérivé, qui de surcroît présente de l'affinité pour les fibres. Le colorant est ensuite réoxydé en sa forme insoluble, qui reste emprisonnée... -
CUIR
- Écrit par Laurent VILLA
- 11 145 mots
- 4 médias
Il en est de même des composés soufrés. La peau prétannée ausoufre peut ensuite être tannée aux tanins végétaux. Elle se tanne plus rapidement et, tout en absorbant moins de tanin, fournit un cuir plus souple. Enfin, le cuir prétanné au soufre est susceptible d'absorber des quantités plus importantes... -
CYCLES BIOGÉOCHIMIQUES
- Écrit par Jean-Claude DUPLESSY
- 7 882 mots
- 6 médias
À l'état réduit, lesoufre (S) est un élément indispensable à la vie. À l'état oxydé de sulfate, il constitue le deuxième anion par ordre d'abondance dans les rivières et l'océan (après l'ion chlorure). Son cycle naturel est profondément perturbé, parce que les combustions de charbons et de certains... - Afficher les 24 références
Voir aussi
- VULCANISATION
- SULFURE DE CARBONE
- ANHYDRIDE SULFUREUX ou DIOXYDE DE SOUFRE
- SULFURES
- RÉGULATION MÉTABOLIQUE
- CONDUCTEURS ÉLECTRIQUES
- DISULFURES
- SULFOBACTÉRIES
- CHIMIQUES INDUSTRIES
- FLOTTATION
- CÉTONES
- ALDÉHYDES
- FRIEDEL & CRAFTS RÉACTIONS DE
- OXYDATION
- SULFONIQUES ACIDES
- SULFONATION
- SULFATES
- CYSTÉINE
- PHÉNOTHIAZINES
- MÉTHIONINE
- POLYSULFURES
- DÉSULFURATION
- CYSTATHIONURIE
- THIOFÈNE ou THIOPHÈNE
- MERCAPTANS ou THIOLS
- MÉTABOLIQUES MALADIES
- CYSTATHIONINE
- FRASCH PROCÉDÉ
- SULFOXYDES
- XANTHATES
- ORKLA PROCÉDÉ
- OUTOKUMPU PROCÉDÉ
- SULFONES
- THIAZOLE
- GRILLAGE DES MINERAIS
- HOMOCYSTÉINE
- HOMOCYSTINURIE
- TRANSMÉTHYLATION
- TRANSSULFURATION
- SULFHYDRIQUE ACIDE
- SOUFRE CYCLE DU
- RÉDUCTION, chimie
- ALLOTROPIE
- BIOSYNTHÈSES
- BIOÉNERGÉTIQUE
- ATMOSPHÈRE, chimie
- STÉRÉO-ISOMÉRIE
- CAOUTCHOUC NATUREL
- RÉGULATIONS BIOCHIMIQUES
- SÉRINE
- DÉFICITS ENZYMATIQUE & MÉTABOLIQUE
- ÉNERGIE FOSSILE ou COMBUSTIBLES FOSSILES