SOUFRE
Article modifié le
Métabolisme
Après une rapide étude du cycle biologique du soufre, on examinera successivement les aspects essentiels du métabolisme du soufre, à savoir : l'oxydation des sulfures en sulfates dans la nature, chez certains micro-organismes présentant des caractères particuliers, et, d'une manière plus générale, chez les êtres vivants ; la réduction des sulfates et leur utilisation tout spécialement par certains micro-organismes dotés de propriétés spécifiques ; la biosynthèse des acides aminés soufrés et de leurs dérivés par les micro-organismes et les plantes ; enfin, la dégradation des acides aminés soufrés et de leurs dérivés par les différents organismes vivants.
Le « cycle » du soufre
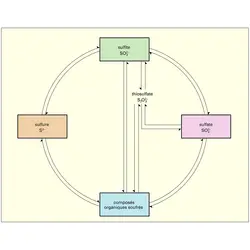
La notion de « cycle » du soufre dans la nature et la matière vivante, dégagée depuis fort longtemps, est justifiée par de multiples observations qu'il est possible de résumer de la façon suivante : les formes minérales réduites du soufre, les sulfures, subissent des oxydations chimiques et enzymatiques qui les transforment en soufre élémentaire et en sulfates ; réciproquement, une réduction des sulfates, faisant intervenir divers intermédiaires, en particulier le sulfite et le thiosulfate, a lieu. De plus, les micro-organismes et les plantes synthétisent, à partir des formes minérales du soufre, un certain nombre de composés organiques nécessaires à leur vie, ou à celle d'autres organismes, principalement les animaux qui doivent obligatoirement trouver dans leur alimentation différents composés organiques soufrés qu'ils utilisent, transforment et dégradent en produits d'élimination.
Certaines étapes indiquées sur la figure sont chimiques ; d'autres sont catalysées par des systèmes enzymatiques.
Oxydation des sulfures en sulfates
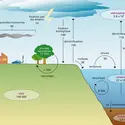
L'oxydation chimique des sulfures soit naturels, soit produits par l'utilisation domestique ou industrielle de divers combustibles (charbon, gaz, dérivés du pétrole) a lieu essentiellement dans l'atmosphère. C'est une transformation lente mais dont l'importance est considérable. Les sulfates ainsi formés sont entraînés par les pluies et répandus sur les sols des continents, dans les fleuves et les océans. W. Kellog et ses collaborateurs (1972) ont décrit le « déséquilibre » des composés soufrés du système atmosphère-océans provoqué par les activités humaines, tout particulièrement les combustions, et souligné l'importance de ces phénomènes en relation avec les problèmes de pollution.
L'oxydation enzymatique des sulfures en sulfates est effectuée par les sulfobactéries autotrophes. Ces phénomènes d'oxydation présentent pour ces organismes une importance particulière, puisqu'ils leur fournissent la majeure partie de l'énergie nécessaire à leur croissance (H. Peck, 1962). Le mécanisme de l'oxydation du sulfite en sulfate a été bien élucidé par H. Peck et ses collaborateurs qui ont montré, en 1965, qu'au cours de cette oxydation il y a formation, à partir de sulfite et d'adénosine 5'-monophosphate (AMP), d'adénosine 5'-phosphosulfate (APS) riche en énergie.
Enfin, chez les plantes, les micro-organismes et les animaux, l'oxydation, en grande partie enzymatique, des sulfures en sulfates constitue un phénomène de détoxication et d'élimination de l'hydrogène sulfuré provenant de la désulfhydration de la cystéine et de l' homocystéine.
Réduction des sulfates et leur utilisation
À l'exception de l'incorporation directe des sulfates dans des molécules organiques pour la formation des esters sulfuriques, l'utilisation des sulfates nécessite leur réduction préalable en sulfites, et leur « activation » par des enzymes qui consomment de l'ATP. Il s'agit alors du métabolisme « assimilatoire » existant en particulier dans la levure.
Chez les animaux supérieurs, la réduction du sulfate n'a pratiquement pas lieu ; en revanche, les plantes supérieures transforment le sulfate en méthionine et cystéine. Enfin, les bactéries sulfatoréductrices réduisent les formes oxydées du soufre minéral en sulfures. Ces phénomènes sont fort importants, puisque les formes oxydées du soufre minéral sont pour ces organismes d'indispensables accepteurs d'électrons.
Biosynthèse des acides aminés soufrés
Les animaux supérieurs sont incapables de synthétiser la méthionine, qui est considérée de ce fait comme un acide aminé indispensable. En effet, elle est nécessaire, d'une part, à la biosynthèse de nombreuses protéines ; d'autre part, elle est la source des groupements méthyle pour les processus de transméthylations. Les animaux doivent donc trouver dans leur alimentation la méthionine elle-même, ou l'un de ses précurseurs.
En revanche, les plantes et les micro-organismes effectuent la biosynthèse de cet acide aminé. Cette biosynthèse a lieu, chez un micro-organisme, Salmonella typhimurium, à partir de méthylmercaptan et d'O-succinylhomosérine (M. Flavin et C. Slaughter, 1967), tandis que, chez les champignons, elle nécessite la présence d'acétylhomosérine (D. Moore et J. Thompson, 1967).
Les bactéries et les tissus animaux synthétisent également la méthionine par transméthylation de l'homocystéine.
L'homocystéine est formée par les plantes et diverses bactéries à partir de dérivés de l'homosérine et de sulfure. Chez Salmonella typhi-murium, ainsi que dans diverses souches de Escherichia coli, elle est également produite par dégradation de la cystathionine, synthétisée elle-même à partir de cystéine et d'O-succinylhomosérine.
Chez les plantes, les micro-organismes et dans les tissus animaux, la cystéine résulte d'une condensation entre l'hydrogène sulfuré et la sérine, ou un de ses dérivés. Cependant, chez les animaux, la majeure partie de la cystéine provient de l'alimentation, ou de la dégradation de la méthionine.
Dégradation des acides soufrés et de leurs dérivés
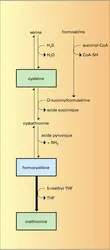
Chez les animaux, la première étape de la dégradation de la méthionine est son activation sous forme de S-adénosylméthionine, qui donne naissance à l'homocystéine. Celle-ci est alors transformée en cystathionine par une réaction de condensation avec la sérine. Cette réaction, catalysée par une enzyme nécessitant le phosphate de pyridoxal comme coenzyme, n'a pas lieu lorsque l'organisme est atteint d'une maladie métabolique, l' homocystinurie, généralement associée à de graves désordres mentaux ; il y a alors accumulation d'homocystéine et d'homocystine dans l'organisme affecté.
La cystathionine est ensuite dégradée en cystéine par une enzyme nécessitant également le phosphate de pyridoxal comme coenzyme. Le défaut de la dégradation de la cystathionine, et donc l'accumulation de cet acide aminé, est observé dans une maladie métabolique, la cystathioninurie, qui est, elle aussi, généralement associée à de profonds troubles mentaux.
La cystéine est soit désulfhydrée, ce qui libère de l'hydrogène sulfuré, soit oxydée en acide cystéine sulfinique, qui subit deux réactions essentielles : une décarboxylation qui conduit à l'hypotaurine, puis à la taurine, l'une des formes d'élimination du soufre, mais aussi substance dont l'importance physiologique semble non négligeable (J. Jacobsen et L. Smith, 1968) ; une désamination entraînant une production de sulfite, qui est ensuite oxydé en sulfate.
Chez les plantes supérieures, les informations sur la dégradation des acides aminés soufrés sont jusqu'ici très fragmentaires. Il faut d'ailleurs signaler que les plantes contiennent un nombre important de composés soufrés qui leur sont spécifiques, mais dont on connaît mal le rôle, et dont on ignore en général les mécanismes de biosynthèse. En revanche, de nombreuses études ont été faites chez les levures, les champignons et les bactéries.
Il n'est pas sans intérêt de remarquer que les phénomènes de transsulfuration – c'est-à-dire le transfert du soufre entre un acide aminé à trois atomes de carbone, la cystéine, et un acide aminé à quatre atomes de carbone, l'homocystéine – sont, en quelque sorte, inverses selon qu'il s'agit des animaux ou des micro-organismes (bactéries, champignons et levures). Dans les deux cas, la cystathionine intervient : chez les animaux, elle est synthétisée à partir d'homocystéine et de sérine, et sa dégradation aboutit à la cystéine ; tandis que, chez les micro-organismes, la cystathionine est synthétisée à partir de la cystéine et d'un dérivé de l'homosérine, et sa dégradation donne naissance à l'homocystéine.
Chez les animaux et chez les micro-organismes, la plupart des enzymes impliquées dans ces phénomènes de biosynthèse et de dégradation ont été bien étudiées, et leurs propriétés sont en grande partie connues. Il s'agit, dans de très nombreux cas, d'enzymes nécessitant le phosphate de pyridoxal comme coenzyme.
La régulation de la biosynthèse et de l'activité de ces enzymes a fait l'objet d'études détaillées (N. Kredich, 1971). Chez les micro-organismes, la méthionine réprime la plupart des enzymes participant à la biosynthèse de cet acide aminé ; chez les animaux, les teneurs en protéines et en pyridoxine des régimes ont une influence sur le taux des enzymes du métabolisme des acides aminés soufrés présents dans divers organes. Enfin, certaines hormones, telles que la thyroxine et l'hydrocortisone, modifient le taux de plusieurs de ces enzymes dans les tissus animaux.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Fernande CHATAGNER : maître de recherche au C.N.R.S.
- René LECLERCQ : vice-président de l'Institut International du soufre
- Noël LOZAC'H : doyen honoraire de la faculté des sciences de Caen, professeur émérite de l'université de Caen
- Serge MASSON : directeur de recherche au C.N.R.S., Caen
Classification
Médias
Autres références
-
CARBURANTS
- Écrit par Daniel BALLERINI , Jean-Claude GUIBET et Xavier MONTAGNE
- 10 536 mots
- 9 médias
De façon générale, la fabrication du gazole fait intervenir deux grands types de réactions chimiques : la désulfuration et l'hydrogénation. La première permet d'atteindre de très bas niveaux de teneur en soufre maintenant spécifiés par les réglementations antipollution (10 ppm maximum... -
COLORANTS
- Écrit par Daniel FUES
- 6 775 mots
- 4 médias
Les colorants au soufre sont insolubles dans l'eau. Ainsi, leur application en teinture passe par une réduction alcaline pour aboutir à un composé soluble, appelé leucodérivé, qui de surcroît présente de l'affinité pour les fibres. Le colorant est ensuite réoxydé en sa forme insoluble, qui reste emprisonnée... -
CUIR
- Écrit par Laurent VILLA
- 11 145 mots
- 4 médias
Il en est de même des composés soufrés. La peau prétannée ausoufre peut ensuite être tannée aux tanins végétaux. Elle se tanne plus rapidement et, tout en absorbant moins de tanin, fournit un cuir plus souple. Enfin, le cuir prétanné au soufre est susceptible d'absorber des quantités plus importantes... -
CYCLES BIOGÉOCHIMIQUES
- Écrit par Jean-Claude DUPLESSY
- 7 882 mots
- 6 médias
À l'état réduit, lesoufre (S) est un élément indispensable à la vie. À l'état oxydé de sulfate, il constitue le deuxième anion par ordre d'abondance dans les rivières et l'océan (après l'ion chlorure). Son cycle naturel est profondément perturbé, parce que les combustions de charbons et de certains... - Afficher les 24 références
Voir aussi
- VULCANISATION
- SULFURE DE CARBONE
- ANHYDRIDE SULFUREUX ou DIOXYDE DE SOUFRE
- SULFURES
- RÉGULATION MÉTABOLIQUE
- CONDUCTEURS ÉLECTRIQUES
- DISULFURES
- SULFOBACTÉRIES
- CHIMIQUES INDUSTRIES
- FLOTTATION
- CÉTONES
- ALDÉHYDES
- FRIEDEL & CRAFTS RÉACTIONS DE
- OXYDATION
- SULFONIQUES ACIDES
- SULFONATION
- SULFATES
- CYSTÉINE
- PHÉNOTHIAZINES
- MÉTHIONINE
- POLYSULFURES
- DÉSULFURATION
- CYSTATHIONURIE
- THIOFÈNE ou THIOPHÈNE
- MERCAPTANS ou THIOLS
- MÉTABOLIQUES MALADIES
- CYSTATHIONINE
- FRASCH PROCÉDÉ
- SULFOXYDES
- XANTHATES
- ORKLA PROCÉDÉ
- OUTOKUMPU PROCÉDÉ
- SULFONES
- THIAZOLE
- GRILLAGE DES MINERAIS
- HOMOCYSTÉINE
- HOMOCYSTINURIE
- TRANSMÉTHYLATION
- TRANSSULFURATION
- SULFHYDRIQUE ACIDE
- SOUFRE CYCLE DU
- RÉDUCTION, chimie
- ALLOTROPIE
- BIOSYNTHÈSES
- BIOÉNERGÉTIQUE
- ATMOSPHÈRE, chimie
- STÉRÉO-ISOMÉRIE
- CAOUTCHOUC NATUREL
- RÉGULATIONS BIOCHIMIQUES
- SÉRINE
- DÉFICITS ENZYMATIQUE & MÉTABOLIQUE
- ÉNERGIE FOSSILE ou COMBUSTIBLES FOSSILES