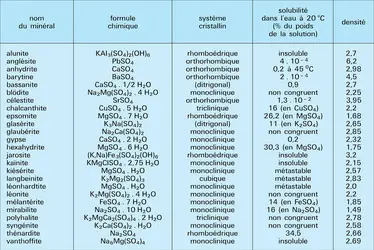
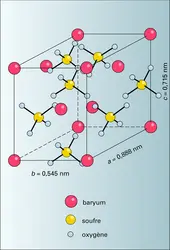
SULFATES NATURELS
Bibliographie
A. Betekhtine, Manuel de minéralogie descriptive, Mir, Moscou, 1968
H. Borchert & R. O. Muir, Salt Deposits, Van Nostrand, Londres, 1964
O. Braitsch, Salt Deposits. Their Origin and Composition (Entstehung und Stoffebestand der Salzlagerstätten, 1971), Springer-Verlag, New York, 1971
W. A. Deer, R. A. Howie & J. Zussman, Rock-Forming Minerals, vol. V, Longman, Londres, 1962
K. Frye, The Encyclopedia of Mineralogy, Hutchinson Ross, Stroudsburg (Penn.), 1981
R. Pierrot, Chemical and Determinative Tables of Mineralogy, Masson, 1979
P. Ramdohr & H. Strunz, Klockmanns Lehrbuch der Mineralogie, F. Enke, Stuttgart, 1978
P. Routhier, Les Gisements métallifères, 2 vol., Masson, Paris, 1963
H. Strunz, Mineralogische Tabellen, Akademische Verlag, Leipzig, 1982.
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- André JAUZEIN : professeur à la faculté des sciences de l'université de Paris-VI-Pierre-et-Marie-Curie, directeur du laboratoire de géologie de l'École normale supérieure de Paris
Classification
Médias
Autres références
-
ANHYDRITE
- Écrit par Yves GAUTIER
- 253 mots
Sulfate anhydre de calcium, l'anhydrite, fréquemment incolore ou blanche à grise, parfois bleutée à rosâtre, se présente généralement en masse finement cristallisée ou granulaire. Les cristaux bien exprimés (prismatiques courts et tabulaires) sont rares. On la reconnaît facilement grâce à ses trois...
-
BARYTINE
- Écrit par Yannick LOZAC'H
- 306 mots
Sulfate de baryum (BaSO4) cristallisé dans le système orthorhombique. Les cristaux s'assemblent fréquemment en masses lamellaires, par suite du développement de la face (001) ; les cristaux prismatiques sont beaucoup plus rares. Le plus souvent, ce sont des amas granulaires, cryptocristallins....
-
BARYUM
- Écrit par Bernard CARTON
- 330 mots
Du grec barus, lourd
Symbole chimique : Ba
Numéro atomique : 56
Masse atomique : 137,34 g
Point de fusion : 725 0C
Point d'ébullition : 1 640 0C
Densité (à 20 0C) : 3,5.
Deuxième membre de la famille des alcalinoterreux (après le calcium), dont C. W. Scheele découvrit la base (baryte)...
-
CALCIUM
- Écrit par Jean PERROTEY
- 2 292 mots
- 2 médias
Le sulfate est lui aussi important, puisque, sous sa forme hydratée, il constitue le plâtre. Le gypse naturel est bihydraté ; chauffé à une température inférieure à 150 0C, il perd 1,5 molécule d'eau et, au-delà, le sulfate anhydre β se forme ; ces phases de la déshydratation étant réversibles,... - Afficher les 16 références