CINÉTIQUE DES FLUIDES THÉORIE
Article modifié le
Grandeurs macroscopiques et fonctions de distribution
Dans les études macroscopiques de fluides (hydrodynamique et physico-chimie), on définit un certain nombre de grandeurs macroscopiques (densité, vitesse de fluide, pression...). Chacune d'entre elles est supposée directement mesurable par une expérience typique ; par exemple, la pression est définie à partir de la force normale agissant sur une paroi. Ces définitions macroscopiques cachent cependant parfois des difficultés et on adoptera ici le point de vue qu'on peut définir les grandeurs macroscopiques à partir des fonctions de distribution ; en cela, on poursuit la méthode régressive qui a permis de passer de D à f1. Bien entendu, ces définitions sont choisies de manière à recouper dans les cas simples celles de l'hydrodynamique élémentaire.
Densité simple et double
La densité simple (nombre de molécules par cm3) est définie par la formule :
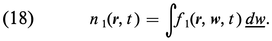
Comme toutes les grandeurs macroscopiques, la densité simple est une fonction de r et de t et non de la vitesse microscopique w, celle-ci s'étant éliminée dans l'intégration (18).
La densité double (dont on se servira pour évaluer l'effet macroscopique des interactions entre molécules) est définie par :
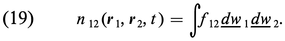
Dans un fluide homogène isotrope, elle ne dépend que de la distance r12 = |r1 − r2|.
Vitesse de fluide
La vitesse de fluide v est la valeur moyenne de w pondérée par la fonction de distribution simple. Soit :
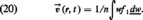
Dans un fluide au repos, →v est nulle ; dans les écoulements lents usuels (subsoniques), la vitesse de fluide est bien plus petite en valeur absolue que les vitesses d'agitation thermique w (→v plus petit que la moyenne de |w|) ; dans de tels écoulements le fluide reste donc presque isotrope.
Flux de molécules dans un gaz isotrope
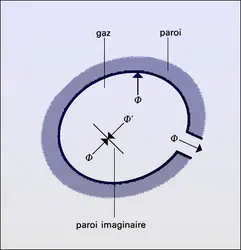
Dans un gaz isotrope, le flux qui traverse un élément de surface placé en un point quelconque du fluide est nul ; mais il est en fait la somme algébrique de deux flux égaux Φ et Φ′ traversant la surface en sens contraire. Le calcul de ces flux à partir de f1 donne la formule générale :

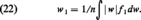
La formule (21) a de nombreuses applications, car on peut l'appliquer non seulement à une paroi imaginaire située dans la masse du gaz, mais aussi à une paroi réelle (étude des phénomènes d'adsorption), ou à un trou dans cette paroi réelle (étude des phénomènes de diffusion thermique dans les corps poreux et dans les canalisations à vide).
Pression
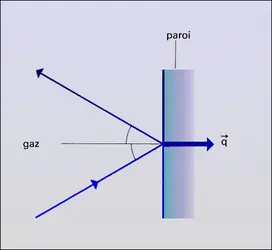
On peut faire un calcul assez simple de la pression dans un gaz en définissant celle-ci comme la force par unité de surface exercée sur une paroi. Du point de vue de la théorie cinétique, cette force est une valeur moyenne due à la succession de petites impulsions élémentaires produites par les collisions des molécules sur les parois. Si l'on suppose que la paroi est parfaitement plane et que les molécules rebondissent élastiquement sur celle-ci, on trouve que la force est normale à la paroi et, dans le cas simple d'un gaz dilué en équilibre thermodynamique à la température T, le calcul conduit, pour la pression p, à la loi des gaz parfaits :

Cependant, de manière générale, un gaz en mouvement est anisotrope et on ne peut pas considérer que la pression en un point soit un scalaire comme on le fait en hydrostatique. D'ailleurs, il est bien connu que la force exercée sur une paroi comporte alors, en plus de la composante normale, une composante tangentielle d'entraînement de la paroi. Mais, chose plus grave, la force exercée sur la paroi dépend a priori non seulement du gaz, mais aussi des propriétés physico-chimiques de la paroi : si l'on adopte le modèle de la figure, on en conclut que la force d'entraînement est nulle. En fait il n'en est rien, ce qui montre clairement qu'un tel modèle est trop simple et que, pour éviter de telles difficultés, la notion de pression doit être définie dans le volume même du gaz, indépendamment de la présence d'une paroi.
L'analyse faite par divers auteurs a démontré que la pression totale est un tenseur du deuxième ordre p. La quantité ∇ . p, divergence de ce tenseur, joue le rôle d'une force par unité de volume appliquée au fluide : p se compose de deux parties de natures différentes : une pression cinétique liée à l'agitation thermique et une pression dite intermoléculaire liée aux interactions entre molécules.
Le tenseur de pression cinétique se calcule à partir de la fonction de distribution f1 par la formule :

Comme le montre cette formule, c'est une mesure de l'agitation thermique, c'est-à-dire des écarts des vitesses w par rapport à la vitesse de fluide v ; la pression cinétique serait nulle dans un faisceau parfaitement ordonné où toutes les molécules auraient la même vitesse w = v. Dans un gaz isotrope, la pression cinétique est un scalaire (plus précisément un tenseur diagonal unitaire), et l'on peut alors poser par définition :

Le tenseur de pression intermoléculaire se calcule à partir de la densité double n12 et de la force d'interaction X12 (force exercée par une molécule placée au point 2 sur une molécule placée au point 1) par la formule générale :

Dans un gaz isotrope, la pression intermoléculaire est un scalaire et peut se déduire du potentiel d'interaction ϕ(r) (r = |r12|) par la formule :

La pression totale p étant la somme Ψ= + π=, il est intéressant de comparer les deux termes de cette somme ; on trouve alors que, dans un gaz dilué, la pression cinétique est dominante, la pression intermoléculaire n'est qu'une faible correction. En d'autres termes, la pression cinétique Ψ= est une généralisation de la loi des gaz parfaits au cas des gaz hors d'équilibre thermodynamique et anisotropes. La pression intermoléculaire est, dans les mêmes conditions, une généralisation des corrections dites de gaz réel ou de Van der Waals (appelées parfois aussi pression interne). Cette correction peut être positive ou négative selon les propriétés des interactions moléculaires. Dans le cas d'un gaz isotrope, la formule (27) montre que π est positif si la loi d'interaction est répulsive à toute distance.
Flux de chaleur
Le tenseur flux de chaleur Q (tenseur du troisième ordre) peut être défini comme le quatrième « moment » de f1 (n, v, Ψ
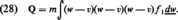
On utilise souvent aussi une quantité un peu plus simple, le vecteur flux de chaleur :

Taux de réaction
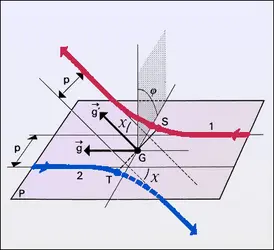
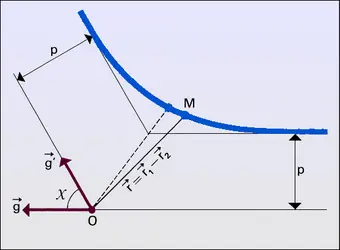
Lorsque les énergies des molécules sont assez élevées, elles peuvent, par des collisions inélastiques, effectuer divers types de réaction. On appelle taux d'une certaine réaction j le nombre de réactions produites par unité de volume et par unité de temps. Ce taux dnj/dt se calcule à partir de la section efficace σj de cette réaction et des fonctions de distribution des particules 1 et 2 qui réagissent. Jusqu'à maintenant n'ont été considérés que des gaz purs constitués d'une seule espèce de molécules ; pour le calcul des taux de réactions, il est nécessaire en général de considérer un mélange gazeux constitué de particules 1 caractérisées par leur fonction de distribution simple f1 et de particules 2 caractérisées par leur fonction de distribution simple f2 (cela n'exclut cependant pas le cas d'un gaz pur où des réactions « symétriques » correspondant à 1 ≡ 2 peuvent se produire). Pour effectuer le calcul, on remarque que les deux distributions f1 et f2 sont équivalentes à un ensemble de faisceaux élémentaires qui se croisent : à chacun de ces couples de faisceaux on peut, en considérant le mouvement relatif, appliquer la relation (10). On obtient ainsi, tout calcul fait pour le taux d'une réaction j, la relation :



Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean-Loup DELCROIX : Professeur à l'Université de Paris-Sud Orsay. Directeur de l'Ecole Supérieure d'Electricité.
Classification
Médias
Autres références
-
AXIOMATIQUE
- Écrit par Georges GLAESER
- 2 037 mots
...surfaces, etc. ; de plus, on décrit les constructions géométriques qui symbolisent, par exemple, les phénomènes de réflexion ou de réfraction. Dans la théorie cinétique des gaz, la théorie mathématique utilisée est relative au comportement statistique d'un grand nombre de « molécules » ; les axiomes... -
CAVITATION
- Écrit par Serge BINDEL
- 842 mots
Ébullition d'un liquide sous vide, donc généralement à température ordinaire ; ce vide peut être produit statiquement (par un émetteur d'ultrasons, par exemple) mais plus fréquemment au sein d'un écoulement, notamment dans les circuits hydrauliques, dans les machines hydrauliques (pompes,...
-
CENTRIFUGATION
- Écrit par Jean LEMERLE
- 1 797 mots
- 3 médias
Lorsque la décantation de particules sous l'effet du champ de pesanteur est inefficace ou trop lente, on a alors recours au procédé de centrifugation. Pour cela, on substitue au champ de pesanteur terrestre un champ de forces centrifuges infiniment plus grand, soit de 500 000 à 1 million de fois l'accélération...
-
CHALEUR
- Écrit par Paul GLANSDORFF
- 985 mots
La première tentative d'interprétation physique assimilait la chaleur à un fluide dit subtil et indestructible dénommé le calorique, répandu partout au sein de la matière. Son passage d'un corps à un autre était notamment responsable du refroidissement du premier et de l'échauffement du second....
- Afficher les 16 références
Voir aussi
- GAZ DIATOMIQUES
- GAZ POLYATOMIQUES
- ONDE DE CHOC
- RELAXATION, physique
- PRESSION, physique
- LIQUIDE ÉTAT
- TENSEURS
- LIBRE PARCOURS MOYEN
- PHASES ESPACE DES
- VITESSE
- COULOMB POTENTIEL DE
- COLLISION, physique
- COLLISIONS ÉLASTIQUES
- ÉQUILIBRE THERMODYNAMIQUE
- ÉQUIPARTITION DE L'ÉNERGIE
- CINÉTIQUES ÉQUATIONS
- BBGKY (Born, Bogolioubov, Green, Kirkwood, Yvon) SYSTÈME
- MOLÉCULES DIATOMIQUES
- DISTRIBUTION FONCTION DE
- LIOUVILLE ÉQUATION DE
- HIÉRARCHIE ÉQUATIONS DE LA
- MAXWELL-BOLTZMANN DISTRIBUTION DE
- GIBBS FORMULE DE
- COLLISIONS INÉLASTIQUES
- GAZ PARFAITS LOI DES
- FRÉQUENCE DE COLLISION
- HYDRODYNAMIQUE
- MOLÉCULES POLYATOMIQUES
- PLASMAS
- SECTION EFFICACE
- COLLISIONS SUPERÉLASTIQUES
- RÉGIMES, physique
- MASSE RÉDUITE
- PARAMÈTRE D'IMPACT
- THERMIQUE AGITATION
- VIBRATION MOLÉCULAIRE ÉNERGIE DE
- IONISÉS MILIEUX
- ÉNERGIE POTENTIELLE
- LOGARITHME COULOMBIEN
- GAZEUX ÉTAT
- BOLTZMANN ÉQUATION DE
- APPROXIMATION
- ÉNERGIE CINÉTIQUE
- ÉVOLUTION ÉQUATIONS D'
- TRANSPORT ÉQUATION DE