CINÉTIQUE DES FLUIDES THÉORIE
Article modifié le
Problèmes particuliers
Effets des rotations et des vibrations dans les gaz non monoatomiques
Dans tout ce qui précède, on a assimilé les molécules à des masses ponctuelles ; en d'autres termes, on a admis que le mouvement d'une molécule était complètement défini par les variables ri et wi, qu'on peut considérer comme la position et la vitesse du centre de gravité de la molécule ; on peut encore dire qu'on n'a tenu compte que de l'agitation thermique de translation des molécules. D'autre part, on a admis que les forces d'interaction étaient des forces centrales dérivant d'un potentiel ϕ(r). Il est clair que ces hypothèses s'appliquent bien aux gaz constitués de molécules monoatomiques (gaz rares, vapeurs métalliques). Si l'on considère maintenant des gaz constitués de molécules diatomiques (H2, N2, O2, ...) ou polyatomiques (CO2, H2O, ...), la description utilisée ne constitue qu'une première approximation, certes très utile, mais qui doit être corrigée sur certains points, pour tenir compte des phénomènes suivants :
– Une molécule diatomique ou polyatomique est animée d'un mouvement de rotation autour de son centre de gravité ; les énergies de rotation sont quantifiées, mais les quanta de rotation sont en général très faibles (de 10-2 à 10-5 eV) devant les énergies d'agitation thermique, de sorte que de nombreux niveaux de rotation sont excités ; il en résulte, d'après le principe de correspondance, qu'une description classique des rotations moléculaires est une assez bonne approximation (cf. mécaniquequantique).
– Une molécule diatomique ou polyatomique est animée d'un mouvement de vibration des divers atomes la constituant ; dans les molécules diatomiques, la vibration se produit selon l'axe des deux noyaux ; dans les molécules polyatomiques, il existe des modes propres de vibration qui dépendent de la structure des molécules. Les quanta de vibration sont plus élevés que ceux de rotation ; pour les molécules stables ils sont, à la température ordinaire, nettement supérieurs aux énergies d'agitation thermique ; dans ces conditions, les molécules du gaz restent toutes dans leur niveau fondamental de vibration. À haute température, les niveaux de vibration peuvent au contraire être excités, et les collisions entre molécules peuvent devenir inélastiques vis-à-vis de ce phénomène d'excitation des vibrations.
– Les molécules diatomiques ou polyatomiques n'ayant pas la symétrie sphérique, la force d'interaction entre deux molécules n'est évidemment pas une force centrale ; elle dépend de l'orientation relative des deux molécules. Ce sont de telles forces non centrales qui permettent des échanges d'énergie de rotation entre deux molécules lors d'une collision.
Si l'on se contente d'étudier l'équilibre thermodynamique, on peut décrire sans trop de difficultés l'état du gaz, en utilisant les méthodes de la mécanique statistique quantique ; pour cela, on considère chaque niveau quantifié j de vibration ou de rotation d'une molécule comme constituant une espèce distincte de particule, de densité nj (chacune de ces espèces possède une distribution maxwellienne des vitesses de translation). La répartition des molécules entre les différents états j est donnée par la formule de Gibbs quantique :
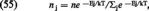
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jean-Loup DELCROIX : Professeur à l'Université de Paris-Sud Orsay. Directeur de l'Ecole Supérieure d'Electricité.
Classification
Médias
Autres références
-
AXIOMATIQUE
- Écrit par Georges GLAESER
- 2 037 mots
...surfaces, etc. ; de plus, on décrit les constructions géométriques qui symbolisent, par exemple, les phénomènes de réflexion ou de réfraction. Dans la théorie cinétique des gaz, la théorie mathématique utilisée est relative au comportement statistique d'un grand nombre de « molécules » ; les axiomes... -
CAVITATION
- Écrit par Serge BINDEL
- 842 mots
Ébullition d'un liquide sous vide, donc généralement à température ordinaire ; ce vide peut être produit statiquement (par un émetteur d'ultrasons, par exemple) mais plus fréquemment au sein d'un écoulement, notamment dans les circuits hydrauliques, dans les machines hydrauliques (pompes,...
-
CENTRIFUGATION
- Écrit par Jean LEMERLE
- 1 797 mots
- 3 médias
Lorsque la décantation de particules sous l'effet du champ de pesanteur est inefficace ou trop lente, on a alors recours au procédé de centrifugation. Pour cela, on substitue au champ de pesanteur terrestre un champ de forces centrifuges infiniment plus grand, soit de 500 000 à 1 million de fois l'accélération...
-
CHALEUR
- Écrit par Paul GLANSDORFF
- 985 mots
La première tentative d'interprétation physique assimilait la chaleur à un fluide dit subtil et indestructible dénommé le calorique, répandu partout au sein de la matière. Son passage d'un corps à un autre était notamment responsable du refroidissement du premier et de l'échauffement du second....
- Afficher les 16 références
Voir aussi
- GAZ DIATOMIQUES
- GAZ POLYATOMIQUES
- ONDE DE CHOC
- RELAXATION, physique
- PRESSION, physique
- LIQUIDE ÉTAT
- TENSEURS
- LIBRE PARCOURS MOYEN
- PHASES ESPACE DES
- VITESSE
- COULOMB POTENTIEL DE
- COLLISION, physique
- COLLISIONS ÉLASTIQUES
- ÉQUILIBRE THERMODYNAMIQUE
- ÉQUIPARTITION DE L'ÉNERGIE
- CINÉTIQUES ÉQUATIONS
- BBGKY (Born, Bogolioubov, Green, Kirkwood, Yvon) SYSTÈME
- MOLÉCULES DIATOMIQUES
- DISTRIBUTION FONCTION DE
- LIOUVILLE ÉQUATION DE
- HIÉRARCHIE ÉQUATIONS DE LA
- MAXWELL-BOLTZMANN DISTRIBUTION DE
- GIBBS FORMULE DE
- COLLISIONS INÉLASTIQUES
- GAZ PARFAITS LOI DES
- FRÉQUENCE DE COLLISION
- HYDRODYNAMIQUE
- MOLÉCULES POLYATOMIQUES
- PLASMAS
- SECTION EFFICACE
- COLLISIONS SUPERÉLASTIQUES
- RÉGIMES, physique
- MASSE RÉDUITE
- PARAMÈTRE D'IMPACT
- THERMIQUE AGITATION
- VIBRATION MOLÉCULAIRE ÉNERGIE DE
- IONISÉS MILIEUX
- ÉNERGIE POTENTIELLE
- LOGARITHME COULOMBIEN
- GAZEUX ÉTAT
- BOLTZMANN ÉQUATION DE
- APPROXIMATION
- ÉNERGIE CINÉTIQUE
- ÉVOLUTION ÉQUATIONS D'
- TRANSPORT ÉQUATION DE