THERMODYNAMIQUE Processus irréversibles linéaires
Autres couplages associés à un gradient thermique
La thermodynamique classique, en dehors de la géniale intuition de lord Kelvin, a toujours eu les plus grandes difficultés à dominer les problèmes posés par les systèmes où la température n'est pas uniforme. Dans le cadre de la thermodynamique contemporaine, nous allons constater, sur les exemples qui suivent, combien il paraît naturel de supputer l'existence de couplages entre flux et forces physiquement différents, mais de même caractère tensoriel, lorsque des gradients thermiques sont présents.
Thermodiffusion
Ce phénomène, découvert par K. Ludwig il y a plus d'un siècle, a été par la suite analysé plus complètement par C. Soret, peu après que L. Dufour eut découvert le phénomène inverse qui porte son nom.
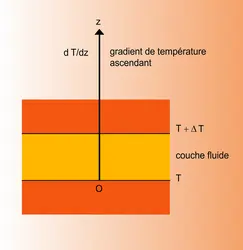
La thermodiffusion (ou effet Soret dans le cas des liquides) est en général observée sur des montages où la couche strictement horizontale de mélange fluide est soumise à un gradient de température ascendant, de façon à éliminer toute convection parasite.
Dans un mélange binaire, une solution par exemple, le gradient thermique une fois établi, la diffusion provoquant la séparation des constituants suivant la verticale obéit à la relation :
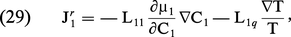
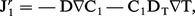
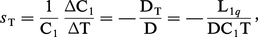
Le flux thermique simultané à Jr1 :
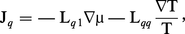
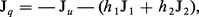
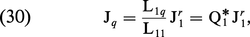
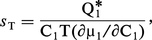
L'effet inverse, ou effet Dufour, n'est guère observable que dans les gaz, où leur mélange provoque un effet thermique (un gradient de température, par exemple). On définit, dans ce cas, un coefficient Dufour df :
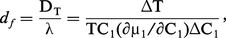
Différence de pression thermomoléculaire et effet thermomécanique
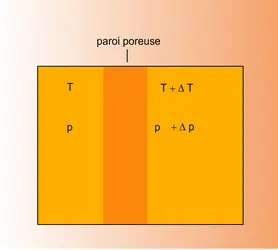
Supposons un gaz réparti entre deux compartiments séparés par une paroi poreuse, et présentant entre eux une différence de température ΔT. L'expérience montre qu'une différence de pression Δp se développe entre ces compartiments. C'est l'osmose thermique.
À partir d'une fonction dissipative calculée pour l'unité de surface de la membrane, il est facile d'établir les relations linéaires suivantes :
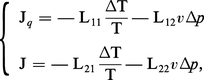
À l'état stationnaire, le gaz n'est plus transporté (J = 0) et la pression thermomoléculaire Δp est donnée par :
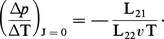
C'est typiquement un phénomène de couplage entre un transport de matière et un transport d'énergie.
Supposons que, au lieu d'une membrane, nous interposions une série d'orifices, petits devant le libre parcours moyen des molécules du gaz.[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques CHANU : professeur à l'université de Paris-VII, chaire de thermodynamique
Classification
Médias
Autres références
-
THERMODYNAMIQUE (notions de base)
- Écrit par Bernard DIU
- 6 036 mots
De nos jours, on peut définir la thermodynamique comme la science des propriétés et des processus qui mettent en jeu la température et la chaleur.
Le nom de « thermodynamique » associe les deux mots grecs thermon (chaleur) et dynamis (puissance). Le but premier de la discipline, explicitement...
-
BOLTZMANN LUDWIG (1844-1906)
- Écrit par Pierre COSTABEL
- 1 636 mots
- 1 média
À partir de ce deuxième principe, Loschmidt a présenté à Boltzmann une objection redoutable, souvent reprise depuis lors, et qui consiste à affirmer l'impossibilité de faire sortir des équations réversibles de la mécanique une interprétation des processus irréversibles de la thermodynamique. Boltzmann... -
CARNOT SADI (1796-1832)
- Écrit par Robert FOX
- 841 mots
- 1 média
Fils aîné de Lazare Carnot, « l'Organisateur de la Victoire », Nicolas Léonard Sadi Carnot est un des pionniers de la thermodynamique. Son unique publication, les Réflexions sur la puissance motrice du feu et sur les machines propres à développer cette puissance, ignorée de son temps...
-
CHALEUR
- Écrit par Paul GLANSDORFF
- 985 mots
La première tentative d'interprétation physique assimilait la chaleur à un fluide dit subtil et indestructible dénommé le calorique, répandu partout au sein de la matière. Son passage d'un corps à un autre était notamment responsable du refroidissement du premier et de l'échauffement du second....
-
CLAUSIUS RUDOLF (1822-1888)
- Écrit par Robert FOX
- 1 001 mots
Rudolf Julius Emanuel Clausius, l'un des plus grands physiciens du xixe siècle, est connu principalement pour sa contribution à l'étude de la thermodynamique. Le premier, ce savant allemand formula ce qu'on a coutume d'appeler le deuxième principe et proposa une définition claire de l'...
- Afficher les 39 références