THERMODYNAMIQUE Processus irréversibles non linéaires
Article modifié le
Thermodynamique et biologie
Dans son livre intitulé L'Ordre biologique, A. Lwoff écrit : « Un certain aspect de l'ordre est l'arrangement déterminé présent dans la constitution existante des choses. L'ordre peut être considéré aussi comme une séquence, ou une succession, dans l'espace ou dans le temps. L'ordre biologique est tout cela, et plus spécialement une séquence dans l'espace et dans le temps. » On peut se demander comment cet ordre ainsi défini se situe par rapport aux grandes lois d'organisation de la physique et, en particulier, de la thermodynamique.
Celle-ci prévoit qu'un système isolé évolue dans le temps vers le désordre. En revanche, en biologie et en sociologie, l'idée d'évolution est associée à une croissance de l'organisation et à la formation de structures de plus en plus complexes. En conséquence, on a longtemps pensé que l'organisation biologique ne pouvait être décrite à partir des lois de la physique. Actuellement, nombre de biologistes considèrent qu'il suffit d'appliquer la thermodynamique à l'ensemble « être vivant plus environnement » pour lever cette difficulté. Cependant, cette interprétation est largement insuffisante. Elle introduit différemment la notion de « système ouvert » mais n'apporte rien de plus à celle de « l'être vivant ». Elle n'explique pas en particulier comment interviennent d'une part, le hasard et d'autre part, les lois déterministes dans la formation des structures biologiques. L'analyse du rôle de la non-linéarité en thermodynamique, exposée plus haut, et qui a conduit au concept de structure dissipative a permis de répondre à ces questions.
Ordre biologique et structures dissipatives
Les systèmes biologiques sont des systèmes ouverts échangeant de la matière et de l'énergie avec le monde extérieur. Ils se caractérisent par un ordre spatial et temporel tout comme celui des structures dissipatives définies plus haut. Il convient donc d'examiner dans quelle mesure celles-ci interviennent dans l'établissement de l'ordre biologique.
La question est relativement plus simple à traiter pour l'organisation temporelle, car l'évolution du système est alors régie par un nombre réduit d'équations différentielles ordinaires tandis que l'étude des structures spatiales ou spatio-temporelles requiert l'analyse plus complexe d'équations aux dérivées partielles.
Au point de vue temporel, les phénomènes d'auto-organisation les plus communs sont, soit l'apparition d'états stationnaires multiples, soit l'évolution vers un régime d'oscillations entretenues correspondant à un cycle limite autour d'un état stationnaire devenu instable à la suite d'une bifurcation. Les exemples biologiques de tels phénomènes sont nombreux, et certains sont brièvement détaillés ci-dessous.
S'il est vrai que les phénomènes périodiques sont connus en chimie non biologique, comme l'indique la réaction de Belousov-Zhabotinsky, il faut reconnaître qu'ils sont encore plus abondants en biologie. Ils interviennent à tous les niveaux de l'organisation biologique, avec des périodes allant de la seconde (système nerveux) à l'année (systèmes écologiques). Le fonctionnement périodique de certaines cellules nerveuses, lié à leur propriété d'excitabilité, est connu depuis longtemps. Le rythme cardiaque et le rythme respiratoire sont tous deux contrôlés par le système nerveux. Des oscillations d'une période de quelques minutes sont connues dans le métabolisme cellulaire. Elles sont dues à la régulation de l'activité de certaines enzymes. D'autres oscillations, d'une période de l'ordre de l'heure, affectent la synthèse de certaines protéines et résultent de la régulation génétique. Les rythmes circadiens, d'une période proche de 24 heures, sont omniprésents. Toutefois, leur mécanisme reste encore obscur. De périodes plus longues, de l'ordre de quelques jours ou du mois, sont les cycles hormonaux contrôlant la reproduction chez les mammifères. Enfin, à une autre échelle pouvant atteindre quelques années, on connaît depuis longtemps les variations périodiques de populations animales résultant notamment des interactions entre un prédateur et sa proie.
Tous ces phénomènes rythmiques peuvent être interprétés comme l'apparition d'un ordre temporel, sous forme d'oscillations entretenues du type cycle limite, au-delà d'une instabilité de non-équilibre dans un système ouvert régi par des équations cinétiques non linéaires. Cette situation correspond fidèlement à la définition des structures dissipatives en thermodynamique. Les variables dont l'évolution est décrite par ces équations sont, selon le cas, des concentrations d'ions, de métabolites, d'enzymes ou d'hormones, voire des populations de prédateurs ou de proies. Il est remarquable que quelle que soit la nature des éléments du système considéré les interactions non linéaires entre les éléments donnent lieu à des phénomènes identiques régis par des équations différentielles assez semblables.
La raison pour laquelle les phénomènes périodiques sont aussi fréquents en biologie tient à la non-linéarité des processus de régulation, sous forme de rétroactions positives ou négatives, qui s'exercent à tous les niveaux de l'organisation biologique. À cet égard, les oscillations métaboliques sont probablement celles dont le mécanisme est le mieux connu au niveau moléculaire. Elles présentent ainsi un double intérêt, pour leur rôle dans la dynamique cellulaire et pour leur fonction de modèle de rythme biologique. Les prototypes en sont les oscillations glycolytiques dans la levure et dans le muscle, et les oscillations des adénosines monophosphates (AMP) cycliques dans les amibes Dictyostelium discoideum.
Nous examinerons successivement le mécanisme de ces deux phénomènes oscillants, de même qu'un exemple de transition entre états stationnaires multiples impliquant un processus de régulation génétique.
Cycle de la glycolyse
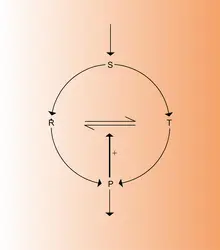
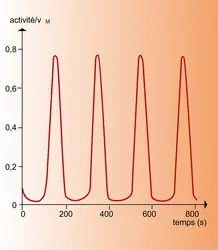
Ce cycle est l'une des voies importantes de production d'énergie cellulaire, sous forme d'adénosine triphosphate (ATP), à partir de glucose. On a observé que, dans des cellules de levures et dans les muscles, la concentration des intermédiaires glycolytiques peut présenter des oscillations entretenues dont la période est de quelques minutes (cf. rythmes biologiques, fig. 2). Parmi les différentes enzymes du cycle de la glycolyse, la phosphofructokinase semble jouer le rôle principal dans l'apparition de ce phénomène périodique. Cette enzyme est allostérique, en ce sens qu'elle est formée d'unités équivalentes possédant des sites réactionnels spécifiques pour la fixation du substrat (fructose-6-phosphate) et du produit de réaction sous forme d'adénosine diphosphate (ADP). Chaque unité existe sous deux états conformationnels T et R, le second ayant une plus grande activité catalytique et/ou une plus grande affinité pour le substrat. L'équilibre conformationnel est « concerté », autrement dit, si l'une des unités formant la molécule change de conformation, les autres unités font de même. La particularité de la phosphofructokinase tient à ce que sa régulation est autocatalytique : en effet, les produits de la réaction (ADP, fructose diphosphate) déplacent l'équilibre conformationnel en faveur de la forme active de l'enzyme. C'est la combinaison de ces deux effets qui est à l'origine des oscillations.
La réaction de la phosphofructokinase gouverne les oscillations de la chaîne glycolytique tout entière. C'est ainsi que l'on peut réduire l'étude du comportement dynamique du cycle de la glycolyse à celle de la réaction de la seule phosphofructokinase, c'est-à-dire à deux équations différentielles non linéaires pour les concentrations des variables S et P, ce qui rend possible la représentation de la . Lorsque l'on traite la cinétique de l'enzyme dans le cadre du modèle allostérique « concerté » de Monod-Wyman-Changeux, en tenant compte de la rétroaction positive exercée par le produit de réaction, on obtient les équations :


Le comportement résultant des équations cinétiques de ce schéma est étudié en partant des différentes données expérimentales disponibles. On détermine d'abord l'état stationnaire de non-équilibre admis par les équations (33). Cet état est obtenu en imposant une valeur constante au substrat et au produit, soit : (dS/dt ) = (dP/dt ) = 0. On étudie ensuite la réponse du système à de petites perturbations autour de cet état. Dans certaines conditions, précisées par cette analyse, les perturbations peuvent s'amplifier au cours du temps. L'état stationnaire est alors instable et le système évolue vers un régime d'oscillations entretenues des concentrations S et P au cours du temps. Ces oscillations correspondent à une variation périodique de l'activité enzymatique. Dans l'espace des phases (S, P), le système tend vers un cycle limite entourant l'état stationnaire instable. Ainsi, quelles que soient les valeurs initiales de S et P, le système évolue toujours vers le même régime oscillant dont l'amplitude et la période sont fixées par les conditions expérimentales et les valeurs des paramètres. Ces caractéristiques de stabilité de la période et de l'amplitude sont celles de la plupart des rythmes biologiques.
L'analyse détaillée du comportement oscillant du modèle se fait au moyen de simulations numériques sur calculateur électronique. On peut ainsi déterminer l'effet d'une variation de la vitesse d'injection de substrat (paramètre v dans les équations (33)). L'analyse du modèle montre qu'en dessous d'une vitesse critique v1, le système évolue vers un état stationnaire stable. Quand on augmente progressivement la vitesse, des oscillations du type cycle limite apparaissent quand v dépasse v1, mais les oscillations disparaissent dès qu'une seconde vitesse critique est atteinte : le système évolue alors vers un nouvel état stationnaire stable. Ce comportement est en accord avec les observations expérimentales. Un accord qualitatif et quantitatif est également obtenu pour d'autres effets dépendant d'autres paramètres, de même que pour le déphasage induit par addition d'ADP au cours des oscillations. Les oscillations glycolytiques représentent donc une structure dissipative temporelle dont l'origine est comprise en détail depuis son niveau moléculaire. Ce résultat est important, car il s'agit de réactions essentielles pour l'énergétique des cellules vivantes.
L'agrégation des acrasiales
L'agrégation des acrasiales fournit un autre exemple particulièrement approprié de structures dissipatives en biologie, car ce phénomène met en jeu au moins deux bifurcations distinctes. Les acrasiales appartiennent à une classe d'amibes dont l'espèce la plus étudiée est Dictyostelium discoideum. Ces amibes sont dites sociales parce qu'elles correspondent à une population d'individus se présentant sous les formes unicellulaire et multicellulaire à deux stades successifs de leur cycle de vie.
Au sortir de spores, les amibes croissent et se reproduisent à l'état unicellulaire. Cette situation se prolonge jusqu'à ce que la nourriture, fournie principalement par des bactéries, vienne à manquer. À ce moment, les amibes cessent de se reproduire et entrent dans une période d'interphase qui dure quelque huit heures. Vers la fin de l'interphase, les amibes commencent à s'agréger autour de certaines d'entre elles fonctionnant comme centres d'agrégation. L'agrégation se fait en réponse à des signaux chimiotactiques émis par les centres. L'agrégat ainsi formé migre jusqu'à ce que les cellules se différencient pour former une tige surmontée d'un sac contenant les spores.
L'existence d'un mécanisme de communication intercellulaire pendant l'agrégation, jointe au fait que les amibes se différencient en deux types de cellules seulement, font que les acrasiales constituent un modèle de choix dans l'étude de la biologie du développement.
Dans Dictyostelium discoideum, l'agrégation se fait de manière périodique. Les films de l'agrégation montrent l'existence d'ondes concentriques d'amibes se dirigeant vers le centre avec une périodicité de quelques minutes.
La nature du facteur chimiotactique est connue : il s'agit de l'adénosine monophosphate cyclique (cAMP), substance impliquée dans de nombreux autres processus biochimiques comme les régulations hormonales. Les centres d'agrégation émettent de façon autonome et périodique les signaux de cAMP. Les autres cellules répondent en se dirigeant vers les centres et en relayant les signaux vers la périphérie du territoire d'agrégation. L'existence d'un mécanisme de relais du signal chimiotactique permet à chaque centre de contrôler l'agrégation de quelque cent mille amibes.
L'analyse du processus d'agrégation met en évidence l'existence de deux types de bifurcations. Tout d'abord, l'agrégation même représente une structuration dans l'espace. Au départ, les amibes sont réparties de façon homogène. Lorsque certaines d'entre elles commencent à sécréter le signal chimiotactique, il se crée des fluctuations locales dans la concentration de cAMP. L'analyse d'un modèle montre que pour une valeur critique des paramètres du système (coefficient de diffusion de l'AMP cyclique, motilité des amibes, etc.), les fluctuations s'amplifient : la répartition homogène est devenue instable et les amibes évoluent vers une répartition spatiale hétérogène. Cette nouvelle répartition s'accompagne donc d'une rupture de symétrie de la distribution initiale, et correspond à l'accumulation des amibes autour de centres d'agrégation. Du point de vue de la thermodynamique, ce comportement correspond fidèlement à celui d'une structure dissipative.
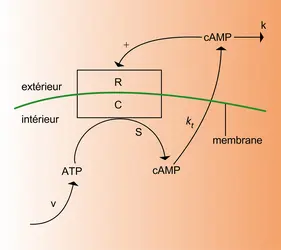
Cette analyse ne rend pas compte du caractère périodique de l'agrégation observée chez certaines espèces d'acrasiales telles Dictyostelium discoideum. Pour comprendre l'origine de la périodicité, il est nécessaire d'étudier plus en détail le mécanisme de synthèse du signal chimiotactique. Sur une base d'observations expérimentales, on peut décrire ce mécanisme par le schéma de la figure. Sur la surface des cellules se trouvent des récepteurs liant les molécules de cAMP. Ce récepteur fait face au milieu extracellulaire et est lié de façon fonctionnelle à l'enzyme assurant la transformation intracellulaire de l'ATP en cAMP, dénommée adénylate cyclase. Le cAMP ainsi synthétisé est transporté au travers de la membrane dans le milieu extracellulaire où il est dégradé par une enzyme sécrétée par les amibes : la phosphodiestérase. L'expérience montre que la liaison du cAMP extracellulaire au récepteur membranaire provoque l'activation de l'adénylate cyclase.
Sur la base de cette rétroaction positive, l'analyse d'un modèle pour l'évolution temporelle des trois variables ATP, cAMP intracellulaire et cAMP extracellulaire a permis d'unifier différents types de comportements observés au cours de l'agrégation. Deux des paramètres clés du modèle sont les activités de l'adénylate cyclase (s) et de la phosphodiestérase (k). Pour un ensemble de valeurs de s et k, le système admet un état stationnaire unique et instable. Chaque fois que les valeurs de ces deux paramètres correspondent à un point de ce domaine, l'instabilité du système provoque son évolution vers un régime d'oscillations entretenues. Ce régime correspond à la synthèse périodique de signaux de cAMP et peut être associé au fonctionnement des centres d'agrégation. Dans une région de l'espace des paramètres contiguë à la précédente, l'état stationnaire est stable mais excitable : le système est capable d'amplifier de manière pulsative de petites perturbations dans la concentration extracellulaire de cAMP. Cette propriété peut être identifiée à la capacité qu'ont les cellules de relayer les signaux de cAMP émis par les centres d'agrégation. Enfin, dans la zone extérieure aux domaines précités, le système évolue vers un état stationnaire stable et non excitable.
Des études sur le développement du mécanisme de communication par signaux de cAMP au cours de l'interphase montrent que les cellules sont tout d'abord incapables de répondre à des signaux de cAMP extracellulaire. Ensuite, progressivement elles relaient ces signaux appliqués de l'extérieur avant de pouvoir les synthétiser périodiquement de façon autonome. Toutes les amibes sont en fait capables de ce dernier type de réponse, bien que quelques-unes seulement deviennent des centres au cours de l'agrégation. La discussion qui précède suggère un chemin de développement du mécanisme de communication dans l'espace des paramètres s et k, pour expliquer la séquence des transitions successives : absence de relais – relais – oscillations, observée expérimentalement. Les centres d'agrégation seraient ainsi les cellules pour lesquelles le couple de valeurs des paramètres s et k aurait atteint le plus rapidement un point dans le domaine instable au cours de l'interphase. Le contenu de ces cellules en adénylate cyclase et en phosphodiestérase serait tel que la synthèse de cAMP ne pourrait procéder que de façon périodique.
Multiplicité d'états stationnaires en régulation génétique
La figure représente le schéma proposé par J. Monod et F. Jacob pour la régulation de la synthèse des protéines dans un système comportant deux chemins enzymatiques distincts. Le gène régulateur RG de chaque enzyme produit un répresseur non actif R qui, en se combinant avec le produit P du chemin enzymatique opposé, forme le répresseur Re ; ce dernier bloque la formation de l'enzyme E à partir du gène de structure G, par l'intermédiaire de l'ARN messager. À ce schéma il faut ajouter le fait important que le produit P, résultant de l'action de l'enzyme sur le substrat, n'a pas seulement un rôle régulateur, mais qu'il intervient également dans des réactions métaboliques schématisées par l'étape :

On écrit, pour l'ensemble formé par les deux chemins enzymatiques, des équations cinétiques régissant l'évolution dans le temps des concentrations des enzymes, des ARN messagers, des produits et des répresseurs, ainsi que des gènes, chacun dans leur état fermé (complexe par Re) ou ouvert. On a de plus la condition physique suivante : le gène est soit ouvert, soit fermé.
La vitesse du processus global est supposée déterminée par les vitesses de synthèse de l'ARN messager et de l'enzyme. Comme dans l'exemple précédent, les équations cinétiques sont traitées par ordinateur, mais cette fois pour un régime stationnaire. On commence par une valeur de F1 correspondant à l'équilibre de la réaction métabolique. Les autres paramètres du système, tels que la valeur des différentes concentrations et constantes cinétiques, sont maintenus constants. Les équations cinétiques possèdent alors une solution unique. En faisant varier F1, on s'écarte de l'équilibre et on atteint une valeur critique à partir de laquelle la solution thermodynamique devient instable, le système se plaçant alors sur une nouvelle branche de solutions stables des équations cinétiques. C'est une région à trois états stationnaires, mais le troisième état est instable.
On passe ainsi brusquement d'une branche à concentration faible en enzyme E1 et forte en enzyme E2 à une autre où la situation inverse prévaut. La conclusion importante est l'apparition d'une différentiation fonctionnelle profonde dans le système, sans qu'un changement soit intervenu dans l'information portée par le matériel génétique, et cela par suite de la non-linéarité de la cinétique et de son couplage avec l'environnement loin de l'équilibre thermodynamique. Pour certaines valeurs des paramètres, les trois états stationnaires disparaissent, la variation de la concentration de l'enzyme en fonction de F1 étant donnée par une courbe sigmoïde.
Des transitions entre états stationnaires multiples ont été invoquées dans de nombreux autres processus cellulaires, tels le changement de perméabilité des membranes biologiques au cours de l'excitation nerveuse.
Morphogenèse
L'application du concept thermodynamique de structure dissipative en biologie, s'étend également au problème de la morphogenèse, c'est-à-dire à la formation de structures spatiales au cours du développement. Ce processus a lieu chez tous les organismes, des plus simples – comme les amibes acrasiales évoquées précédemment, où la structure résulte d'une différenciation en deux types de cellules et consiste en une tige surmontée de spores – jusqu'aux plus complexes, tels les embryons. La connaissance des mécanismes contrôlant la morphogenèse n'est pas encore suffisamment complète pour permettre l'élaboration de modèles appropriés à l'étude de la dynamique de ce phénomène. Toutefois, la théorie des structures dissipatives a été appliquée pour expliquer la formation de structures spatiales régulières au cours du développement. Une application spécifique concerne la formation séquentielle de compartiments dans les disques imaginaux de la drosophile ; ces compartiments résulteraient d'une succession de bifurcations de structures spatiales à mesure que la taille des disques croît au cours du développement. À une échelle plus macroscopique encore, d'autres études suggèrent que la formation du nid et l'organisation des aires d'exploitation chez les insectes sociaux peuvent être interprétées en termes de structures dissipatives résultant des communications (interactions non linéaires) entre les insectes membres de la colonie.
Autres développements
L'analyse des processus d'auto-organisation temporelle a mis en lumière la possibilité d'oscillations non périodiques dans les systèmes physico-chimiques et biologiques. Ce type de comportement, bien que produit par des équations déterministes, possède un caractère aléatoire et, pour cette raison, est dénommé « chaos ». L'apparition de ce phénomène dans les systèmes biologiques a été discutée en écologie, de même que pour un système biochimique à régulation multiple. L'analyse de ce dernier système a mis en lumière la possibilité d'un nouveau phénomène, à savoir la coexistence de deux régimes périodiques stables. Pour un même ensemble de conditions, un système biologique pourrait donc osciller avec des périodes et des amplitudes différentes selon les conditions initiales. Ce processus illustre une fois de plus la richesse de comportement des systèmes à cinétique non linéaire fonctionnant loin de l'équilibre thermodynamique.
Stade prébiotique
À côté du rôle joué par les structures dissipatives dans le fonctionnement actuel des êtres vivants, il convient d'évoquer la possibilité de leur participation à l'évolution prébiotique.
Le rôle possible des structures dissipatives dans la synthèse abiotique des polypeptides par condensation sur des surfaces catalytiques a été étudié par A. Katchalsky et ses collaborateurs. De son côté, en supposant l'existence d'un ensemble de macromolécules biologiques au stade prébiotique, M. Eigen a montré que le système évolue vers une self-organisation par suite d'une succession d'instabilités.
Il faut distinguer au moins deux types de problèmes : d'une part, la formation de polymères d'intérêt biologique remplissant des fonctions que les monomères ne peuvent accomplir (un exemple bien connu en est la synthèse de polymères qui jouent le rôle de matrice[template]pour leur propre réplication ou pour leur synthèse d'autres macromolécules) ; d'autre part, en supposant que des populations de molécules d'intérêt biologique peuvent se répliquer, quelle sera l'évolution ultérieure d'un tel système ?
Des modèles permettent de montrer que la synthèse par réplication, par exemple celle des acides nucléiques sur template, ne devient dominante par rapport au mécanisme ordinaire de propagation en chaîne qu'à partir d'une distance critique de l'équilibre et qu'elle correspond dès lors à une première instabilité.
M. Eigen considère le second point : les phénomènes de réplication conduisent à des erreurs (un type nouveau de fluctuations) qui peuvent être soit amorties, soit amplifiées (cf. génétique, mutations). L'évolution correspond à une suite de « catastrophes » d'instabilités. Les fluctuations sont amplifiées jusqu'à l'apparition éventuelle d'un état dominé par certains types de macromolécules et pourvu d'une stabilité suffisante par rapport aux fluctuations qu'il engendre lui-même.
Pendant longtemps, le développement scientifique s'est accommodé plus ou moins implicitement de cette opinion que les lois de la physique n'avaient aucun rapport avec celles de la biologie et qu'elles étaient même incompatibles. À présent, et depuis au moins une décennie, les progrès accomplis par la thermodynamique non linéaire des processus irréversibles dans ses rapports avec les propriétés des cinétiques chimiques ont complètement retourné cette opinion. Au point même, que pour les mieux avertis, et comme en témoignent les quelques applications évoquées succinctement ci-dessus, l'adaptation des lois de la physique à la biologie se présente comme faite en quelque sorte sur mesure dès qu'on pénètre davantage l'étude de leurs mécanismes.
Accédez à l'intégralité de nos articles
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Agnès BABLOYANTZ : chef de travaux associé à l'Université libre de Bruxelles .
- Paul GLANSDORFF : professeur émérite de la faculté des sciences à l'université de Bruxelles, président d'honneur de l'Institut international du froid, membre de l'Académie royale
- Albert GOLDBETER : chef de travaux à l'université libre de Bruxelles
- Grégoire NICOLIS : professeur à l'Université libre de Bruxelles
- Ilya PRIGOGINE
: directeur des Instituts internationaux de physique et de chimie, fondés par Ernest Solvay à Bruxelles,
Ashbel Smith regental professor , université du Texas à Austin, directeur du Ilya Prigogine Center of Studies in Statistical Mechanics and Complex Systems, université du Texas à Austin
Classification
Médias
Autres références
-
THERMODYNAMIQUE (notions de base)
- Écrit par Bernard DIU
- 6 036 mots
De nos jours, on peut définir la thermodynamique comme la science des propriétés et des processus qui mettent en jeu la température et la chaleur.
Le nom de « thermodynamique » associe les deux mots grecs thermon (chaleur) et dynamis (puissance). Le but premier de la discipline, explicitement...
-
BOLTZMANN LUDWIG (1844-1906)
- Écrit par Pierre COSTABEL
- 1 636 mots
- 1 média
À partir de ce deuxième principe, Loschmidt a présenté à Boltzmann une objection redoutable, souvent reprise depuis lors, et qui consiste à affirmer l'impossibilité de faire sortir des équations réversibles de la mécanique une interprétation des processus irréversibles de la thermodynamique. Boltzmann... -
CARNOT SADI (1796-1832)
- Écrit par Robert FOX
- 841 mots
- 1 média
Fils aîné de Lazare Carnot, « l'Organisateur de la Victoire », Nicolas Léonard Sadi Carnot est un des pionniers de la thermodynamique. Son unique publication, les Réflexions sur la puissance motrice du feu et sur les machines propres à développer cette puissance, ignorée de son temps...
-
CHALEUR
- Écrit par Paul GLANSDORFF
- 985 mots
La première tentative d'interprétation physique assimilait la chaleur à un fluide dit subtil et indestructible dénommé le calorique, répandu partout au sein de la matière. Son passage d'un corps à un autre était notamment responsable du refroidissement du premier et de l'échauffement du second....
-
CLAUSIUS RUDOLF (1822-1888)
- Écrit par Robert FOX
- 1 001 mots
Rudolf Julius Emanuel Clausius, l'un des plus grands physiciens du xixe siècle, est connu principalement pour sa contribution à l'étude de la thermodynamique. Le premier, ce savant allemand formula ce qu'on a coutume d'appeler le deuxième principe et proposa une définition claire de l'...
- Afficher les 39 références
Voir aussi
- HYSTÉRÉSIS
- MORPHOGENÈSE ANIMALE
- ENZYMES ALLOSTÉRIQUES
- ACRASIALES
- COHÉRENCE, optique
- PHASE TRANSITIONS DE
- ÉQUILIBRE THERMODYNAMIQUE
- CINÉTIQUES ÉQUATIONS
- QUANTIQUE OPTIQUE
- ORDRE & DÉSORDRE, physique
- THERMODYNAMIQUE PRINCIPES DE LA
- RÉGULATION BIOLOGIQUE
- SYSTÈMES THERMODYNAMIQUES
- BÉNARD CELLULES DE
- PROTÉINES BIOSYNTHÈSE DES
- BIOÉNERGÉTIQUE
- GLYCOLYSE
- AMIBES ou AMŒBIENS
- RÉGULATION GÉNÉTIQUE
- PRÉBIOTIQUE CHIMIE
- BIFURCATION PHÉNOMÈNE DE, thermodynamique
- BRISURE DE SYMÉTRIE
- ADÉNOSINE DIPHOSPHATE (ADP)
- ADÉNYLATE CYCLASE ou ADÉNYLCYCLASE ou ADÉNYLYL CYCLASE
- PHOSPHODIESTÉRASES (PDE)
- PERTURBATION, mathématiques
- VAN DER POL ÉQUATION DE
- ÉVOLUTION ÉQUATIONS D'
- OSCILLATIONS ENTRETENUES, biologie
- PHOSPHOFRUCTOKINASE
- AGRÉGATION, biologie
- CHIMIOTACTISME
- ORDRE & DÉSORDRE, biologie
- NON-LINÉAIRE SYSTÈME
- ÉVOLUTION PRINCIPE D', thermodynamique
- FLUCTUATION, physique
- ÉTAT STATIONNAIRE