ÉNERGIE INTERNE
Articles
-
ÉNERGIE - La notion
- Écrit par Julien BOK
- 7 549 mots
- 4 médias
La thermodynamique s'intéresse aux échanges d'énergie entre systèmes macroscopiques. À l'échelle atomique, ces systèmes sont composés de particules (molécules) douées d'énergie cinétique, et aussi d'énergie potentielle mutuelle représentant l'interaction de ces particules entre elles. On appelle énergie... -
MATIÈRE (physique) - État liquide
- Écrit par Jean-Louis RIVAIL
- 3 244 mots
- 6 médias
...molécules peut se décomposer en une somme des énergies d'interaction de paire (ce qui n'est pas tout à fait vrai), la connaissance de u(r) et de g(r) permet de décrire complètement le liquide du point de vue thermodynamique. À titre d'exemple, l'énergie interne vaut, pour un liquide monoatomique :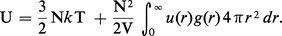
-
MATIÈRE (physique) - État gazeux
- Écrit par Henri DUBOST et Jean-Marie FLAUD
- 8 135 mots
- 7 médias
L'énergie interne (U) d'un système n'est définie qu'à une constante additive près : U0 = M0c2 (produit de la masse au repos [M0]par le carré de la vitesse de la lumière[c]dans le vide). À l'échelle moléculaire, l'énergie interne d'un gaz parfait est égale à la somme des... -
STATISTIQUE MÉCANIQUE
- Écrit par Berni J. ALDER et Bernard JANCOVICI
- 5 855 mots
- 8 médias
La tâche propre de la mécanique statistique se réduit donc au calcul de Z. On obtient ensuite, à partir de l'énergie libre (14), les autres fonctions thermodynamiques, la pression étant :


-
THERMODYNAMIQUE (notions de base)
- Écrit par Bernard DIU
- 6 036 mots
...(énergie cinétique) et leurs interactions (énergie potentielle). Cette énergie qui subsiste lorsque le système est immobile à l'échelle macroscopique est son énergie interne. Dans ces conditions de repos macroscopique, les grandeurs Ui et Ufsont les valeurs de l'énergie interne dans les états initial et final.... -
THERMODYNAMIQUE - Lois fondamentales
- Écrit par Paul GLANSDORFF et Ilya PRIGOGINE
- 3 690 mots
- 5 médias
Dans le cas particulier d'un fluide à pression p uniforme, le travail élémentaire dW se réduit au produit pdV et l'énergie totale U, à l'énergie interne E en l'absence d'énergie cinétique. Le principe de conservation de l'énergie prend alors la forme simplifiée usuelle :