HYDROXYDES
Articles
-
HYDROXYDES
- Écrit par Bertrand DREYFUS
- 182 mots
Composés chimiques contenant un ou plusieurs groupes d'ions hydroxyles (OH—). Le cation est en général un ion métallique (Na, K, Mg, Ca, Al) ou un radical organique (comme le tétraméthylammonium).
Les hydroxydes sont des bases plus ou moins fortes, les plus fortes étant celles des métaux...
-
BÉRYLLIUM
- Écrit par Jean-Paul CARRON , Robert GADEAU et Jean PERROTEY
- 5 411 mots
- 6 médias
L'hydroxyde, ou glucine hydratée, possède une variété amorphe gélatineuse contenant une quantité d'eau mal définie et deux variétés cristallines répondant bien à la formule Be(OH)2. La précipitation à froid par l'ammoniaque donne une sorte de gel, qui cristallise à chaud ou par vieillissement... -
COMPLEXES, chimie
- Écrit par René-Antoine PARIS et Jean-Pierre SCHARFF
- 4 306 mots
- 5 médias
Une valeur de q positive ou négative dans la formule générale MpHqArBs indique respectivement l'existence de complexes protonés ouhydroxydés. Dans ce dernier cas, il s'agit de phénomènes d' hydrolyse intéressant notamment les métaux de degré d'oxydation élevé, ayant un fort caractère... -
MERCURE, élément chimique
- Écrit par Guy PÉREZ et Jean-Louis VIGNES
- 2 297 mots
- 3 médias
L'hydroxyde de mercure Hg(OH)2 existe en solution aqueuse, mais n'a jamais pu être isolé ; il est amphotère, mais à caractère très faiblement basique :Le sulfure mercurique HgS fraîchement précipité est noir, son produit de solubilité est très faible (10—54), le sulfure noir...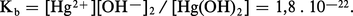
-
MÉTAUX - Métaux alcalins
- Écrit par Jean PERROTEY
- 3 023 mots
- 5 médias
Leshydroxydes alcalins, hygroscopiques et déliquescents, sont des bases fortes solubles ; à la différence des hydroxydes alcalino-terreux, peu solubles, on ne peut les déshydrater par chauffage, car ils fondent sans décomposition. La dissolution dans l'eau s'effectue avec un dégagement de chaleur important... -
MÉTAUX - Métaux alcalino-terreux
- Écrit par Jean PERROTEY
- 2 580 mots
- 3 médias
...; cela traduit une grande stabilité thermique, confirmée par des points de fusion très élevés. Ces oxydes sont utilisés comme réfractaires ; leur réduction est souvent industriellement impossible. Ils s'unissent à l'eau, de façon réversible, pour donner un hydroxyde peu soluble :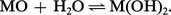
-
OXYDES ET HYDROXYDES NATURELS
- Écrit par Joseph BOLFA
- 4 092 mots
- 6 médias
La structure en feuillet des hydroxydes s'explique principalement par le caractère de l'ion (OH)-, fortement lié d'un côté au cation (liaison à dominance ionique), faiblement lié de l'autre avec les hydroxyles voisins (liaisons hydrogène ou de type Van der Waals). -
POTASSIUM
- Écrit par André HATTERER et Henri KESSLER
- 2 934 mots
L'eau attaque violemment le potassium en formant de l' hydroxyde alcalin KOH et de l'hydrogène qui donne un mélange tonnant avec l'oxygène de l'air. -
RUBIDIUM
- Écrit par Bertrand DREYFUS
- 281 mots
Élément chimique de numéro atomique 37 et de symbole Rb, le rubidium (latin rubidus, rouge foncé) doit son nom à la couleur rouge de son spectre. C'est un métal alcalin mou, d'éclat blanc argenté, découvert par voie spectroscopique par R. Bunsen (1861) et G. R. Kirchhoff dans l'eau minérale...
-
SOLUTION ÉQUILIBRES EN
- Écrit par Claude COLIN et Alain JARDY
- 9 586 mots
- 16 médias
...avec le pH de la solution si l'un des constituants du précipité possède des propriétés acides ou basiques. C'est un cas extrêmement fréquent : citons les hydroxydes, les sulfures, les oxalates, les oxinates... Cette propriété a été largement utilisée en analyse qualitative ou quantitative pour la précipitation...
Médias