SOLVATATION
Articles
-
AMINES
- Écrit par Jacques METZGER
- 3 235 mots
- 4 médias
L'intensité de la solvatation des cations ammonium primaire, secondaire et tertiaire décroît dans cet ordre du fait de la diminution du nombre des atomes d'hydrogène, sites de solvatation par l'eau. La concurrence de ces deux effets : inducteur, croissant avec le nombre des groupes alkyle, et de solvatation,... -
ÉLECTROCHIMIE
- Écrit par Jacques SIMONET
- 6 255 mots
- 10 médias
Lasolvatation, ou hydratation quand l'eau est le solvant principal, est provoquée par l'existence du champ électrique propre à l' ion, dépendant de sa taille et de sa charge. La nature de l'action du solvant sera différente, dans le cas d'ions à charge superficielle élevée (F... -
HYDROGÈNE
- Écrit par Paul HAGENMULLER
- 3 540 mots
- 6 médias
...rupture des liaisons covalentes X − H et du potentiel d'ionisation élevé de l'hydrogène, l'ion H+ n'existe que dans les solvants polaires suffisamment ionisants et dans lesquels il comporte une forte énergie de solvatation. La solvatation est facilitée en fait par la très petite taille du proton. -
IONS ÉCHANGEURS D'
- Écrit par Robert ROSSET
- 6 110 mots
- 13 médias
Pour différents cations de même charge et appartenant à une même famille du point de vue chimique, les résines sulfonate marquent une préférence pour les ions solvatés dont les rayons sont les plus petits, par exemple :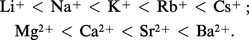
-
MOLÉCULE
- Écrit par André JULG
- 4 302 mots
...libérées s'entourent de tout un cortège de molécules du solvant, formant des agrégats de composition plus ou moins définis, variant au hasard des rencontres. On dira que les molécules provenant du cristal sont solvatées. Avec un cristal macromoléculaire, on a deux cas limites. Tout d'abord, il peut arriver... -
SOLUTION ÉQUILIBRES EN
- Écrit par Claude COLIN et Alain JARDY
- 9 586 mots
- 16 médias
La dissolution dans un solvant résulte de la solvatation des espèces par celui-ci. Le solvant peut donc jouer le rôle d'accepteur de toute particule :
-
SOLVANTS
- Écrit par Jacques DEVYNCK
- 1 796 mots
- 1 média
La mise en solution d'un composé résulte d'un ensemble complexe d'interactions entre molécules de solvant et molécules (ou ions) en solution : c'est la solvatation.

